Геморроидальная болезнь занимает ведущее место в общей структуре патологий прямой кишки и остается одной из актуальных проблем колопроктологии. Заболевание встречается в 130-145 случаях на тысячу человек [1-4].
Несмотря на наличие в арсенале проктологов множества способов консервативного и оперативного лечения, остаются стабильными частота послеоперационных осложнений и сроки госпитализации [5-7]. Согласно разноречивым взглядам проктологов, становится очевидным, что на сегодняшний день ни один из существующих методов операции не общепризнан и не оптимален, так как сопровождаются различными ранними и поздними послеоперационными осложнениями [8-10]. По данным ряда авторов, в 34-41% наблюдений после геморроидэктомии (ГЭ) имеет место интенсивный болевой синдром, в 15-26% - рефлекторные дизурические расстройства, в 2-7% - кровотечения из аноректальных ран, в 2% - гнойно-воспалительные осложнения [8-10].
После операции ГЭ вторым этапом ведение аноректальных ран относится к сложным аспектам проктологии. Этому способствуют выполнение ГЭ на фоне существующего изначально хронического воспаления и неизбежная бактериальная контаминация аноректальных ран, приводящих к замедлению процессов заживления и длительной утрате трудоспособности оперированных больных [5; 7; 9].
Клинико-лабораторными исследованиями установлено, что при хроническом геморрое постепенно развивается дисбаланс кишечного микробиоценоза (КМБ) со снижением бифидофлоры и противоположно этому ростом условно патогенной флоры, который негативно влияет на течение послеоперационного периода и способствует развитию специфических осложнений [2; 4; 7; 10]. В этой связи необходима разработка послеоперационной тактики ведения анальных ран после ГЭ с учетом дисбаланса КМБ.
Цель работы: повышение эффективности комплексного лечения аноректальных ран после ГЭ на основе оптимизации оперативной техники и разработки способа коррекции нарушений КМБ.
Материал и методы исследования
В исследование был включен 631 пациент с геморроем 3-4 стадии, находившийся на стационарном лечении в отделении проктологии Ошской межобластной объединенной клинической больницы. Все пациенты были распределены на 2 группы. Первая, основная группа составлена из 221 больного, которым выполнен модифицированный нами метод ГЭ по Миллигану-Моргану во второй модификации ГНЦ колопроктологии МЗ РФ. Больным этой группы также проведена коррекция КМБ жидким бифидумбактерином (ЖББ). В этой группе мужчин было 167 (74,4%) человек, а женщин - 54 (25,6%). Возраст больных от 15 до 75 лет (средний возраст 40,5±2,1 года).
Контрольная группа составлена из 410 пациентов, которым произведена традиционная ГЭ по Миллигану-Моргану во второй модификации ГНЦ колопроктологии МЗ РФ. Мужчины в данной группе составили 292 (71,2%) человек, женщины – 118 (28,8%). Возраст больных от 16 до 78 лет (средний возраст 39,3±2,3 года).
Всем больным обеих групп было проведено общепринятое клиническое обследование: сбор и анализ клинико-анамнестической информации, объективный и проктологический осмотры, лабораторно-инструментальные обследования. Проктологическое исследование включало ревизию аноректальной зоны в коленно-локтевом положении, пальцевой осмотр прямой кишки, ректороманоскопию, сфинктероманометрию и ректальную термометрию. Для объективного анализа эффективности разработанного способа коррекции дисбаланса КМБ ЖББ проводили такие специальные методы обследования, как оценку течения раневого процесса (динамика раневой воспалительной реакции, местные показатели, интенсивность репарации), микробиологические и цитологические исследования.
Также 631 пациент разделен на 3 группы в зависимости от питания (рис. 1).
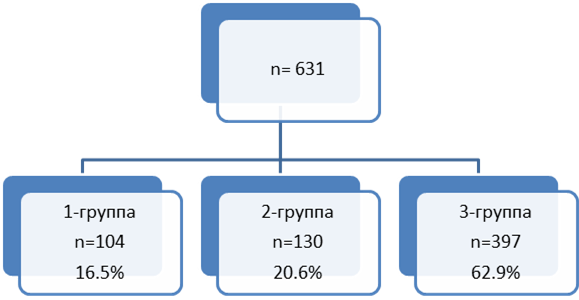
Рис. 1. Распределение больных в зависимости от особенностей питания
Методика модифицированного нами способа ГЭ по Миллигану-Моргану заключается в следующем: вначале иссекаются внутренние геморроидальные узлы по Миллигану-Моргану во второй модификации ГНЦ колопроктологии МЗ РФ, затем циркулярно удаляются наружные узлы, которые при 3-4 стадии в основном сливаются между собой. Образовавшаяся рана ушивается наглухо. Преимущества способа заключаются в следующем: сохраняется целостность зубчатой линии, раны слизистой оболочки анального канала не имеют связи с циркулярной раной кожи перианальной области.
Комплексный метод коррекции КМБ с использованием ЖББ заключался в следующем: в день госпитализации у пациента проводили исследование кала на наличие дисбактериоза. В первый день перорально назначали первую (30 доз), вторую (20 доз) и третью порции (10 доз) ЖББ. В процессе подготовки к ГЭ после 4 очистительных клизм с интервалом 4-5 часов, а также дополнительно за 3 часа до операции ректально вводили по 20-30 доз ЖББ. После операции через установленную при завершении ГЭ газоотводную трубку вводили 20 доз ЖББ 2 раза в день в течение первых двух суток. В последующем в течение послеоперационного периода назначали внутрь по 5 доз препарата 3-4 раза в сутки и по 2-2,5 дозы в виде микроклизм до заживления раны аноректальной области. Назначение ЖББ проводилось под контролем оценки КМБ.
Результаты исследования и их обсуждение
Анализ результатов комплексного лечения показал, что в послеоперационном периоде интенсивность и продолжительность местного болевого синдрома, особенно во время акта дефекации, была разной в основной и контрольной группах. У больных основной группы болевой синдром встречался в 42 (19,0%) наблюдениях, а в контрольной группе – в 139 (34,0%) случаях. Это обусловлено меньшей или большей степенью выраженности местного воспалительного процесса в области послеоперационных аноректальных ран, что констатируется результатами проведенной ректальной термометрии на 3, 5 и 7-е сутки после ГЭ у 68 (30,8%) больных основной группы и у 101 (24,6%) контрольной группы (табл. 1).
Таблица 1
Показатели ректальной термометрии (M±m), 0C
|
Послеоперационные сутки |
Группы исследования |
|
|
Основная (n =68) |
Контрольная (n =101) |
|
|
3 |
36,8 ± 0,1 |
37,3 ± 0,2 |
|
5 |
37,2 ± 0,2 |
38,3 ± 0,3 |
|
7 |
36,9 ± 0,1 |
37,4 ± 0,1 |
На 3-4-е сутки послеоперационного периода затрудненная дефекация наблюдалась у 28 (12,7%) пациентов основной группы и у 98 (23,9%) больных группы контроля (р<0,05).
В 6 (2,7%) наблюдениях основной группы и 38 (9,2%) наблюдениях контрольной группы отмечались рефлекторные дизурические расстройства по типу задержки (р<0,05).
Сроки стационарного пребывания пациентов в стационаре также существенно отличались исследуемых группах. Так, этот показатель в основной группе составил 10,7±1,1 койко-дня, а в контрольной группе – 13,9±1,09 койко-дня (р<0,05).
Исследование КМБ у больных с геморроем показал, что климато-географические условия не играют роли в развитии дисбактериоза, основной причиной оказался образ питания пациентов, в частности наличие в каждодневном пищевом рационе кисломолочной продукции. Частота развития нарушения КМБ у больных 3 групп представлена в таблице 2.
Таблица 2
Частота дисбактериоза в зависимости от регулярности употребления кисломолочных продуктов
|
Группы исследования |
Число наблюдений |
Из них дисбактериоз |
|
|
Абс. число |
% |
||
|
I группа - регулярно |
104 |
5 |
4,8* |
|
II группа - не регулярно |
130 |
118 |
91,1 |
|
III группа - не употребляли |
397 |
384 |
96,7 |
|
Всего |
631 |
507 |
80,3 |
Примечание: * - достоверность различий при р<0,05.
Как видно из таблицы 2, при регулярном употреблении кисломолочных продуктов нарушение КМБ достоверно развивается реже (4,8%), чем при нерегулярном употреблении (91,1%) или при отсутствии в пищевом рационе кисломолочных смесей. Следует отметить, что во II группе в копрограмме патогенных микробов (гемолитическая кишечная палочка, протей и грибы рода Candida) не обнаружено. А в III группе из 397 обследованных больных нарушения КМБ установлены в 384 (96,7%) случаев. У них патогенные микроорганизмы семейства кишечных были обнаружены в 30 (7,6%) наблюдениях (табл. 3).
Таблица 3
Микрофлора толстой кишки у пациентов с хроническим геморроем до операции (n=631)
|
Микрофлора |
Норма |
Абс. |
В % |
|
Патогенные микробы семейства кишечных |
- |
30 |
4,76 |
|
Снижение общего количества кишечной палочки |
300-400 млн/г |
301 |
47,7 |
|
Кишечная палочка со слабыми ферментативными свойствами |
до 10 % |
180 |
28,57 |
|
Лактозонегативные энтеробактерии |
до 5% |
261 |
41,3 |
|
Гемолизирующая кишечная палочка |
- |
225 |
35,7 |
|
Кокки в общей сумме микробов |
25% |
270 |
42,85 |
|
Процентное отношение гемолизирующего стафилококка ко всем коккам |
0 |
150 |
23,8 |
|
Снижение бифидобактерии ниже 107 |
выше 107 |
466 |
73,8 |
|
Микробы рода протея |
- |
225 |
35,7 |
|
Грибы рода кандида |
- |
375 |
59,52 |
Таким образом, у более 80% пациентов основной и контрольной групп выявленные изменения в КМБ напрямую зависят от ингредиенции в пищевом рационе кисломолочных продуктов. Перед хирургическим лечением хронического геморроя очень важно и необходимо учитывать характер питания пациентов, в частности регулярное употребление кисломолочных продуктов, что позволяет установить у больных нарушения в КМБ и подтверждает необходимость включения в комплекс лечения ЖББ.
Сравнительный анализ динамики воспалительной раневой реакции после ГЭ показал положительную тенденцию в 56,9% наблюдениях основной группы, а неудовлетворительная динамика отмечена в 5,9% случаях. В контрольной группе существенная положительная динамика воспалительной раневой реакции констатирована лишь в 8,7% случаев, у 52,8% больных установлена неудовлетворительная (р<0,05) (рис. 2).

Рис. 2. Динамика воспалительной раневой реакции
Достоверная разница показателей в двух исследуемых группах была зарегистрирована также и при анализе регенерационных процессов. В основной группе активная регенерация наблюдается в 49,8% случаев, а в контрольной группе у 46,1% больных она оказалась замедленной. Достоверных различий у пациентов в зависимости от вида проведенных хирургических операций не отмечено (р>0,05).
Анализ третьей фазы раневого процесса показал заживление аноректальных ран с формированием рубца в течение 17,4±1,9 дня после ГЭ в основной группе, в то время как в группе контроля этот показатель составил 24,5±1,9 дня (р<0,05).
Проведена оценка фагоцитарной активности лейкоцитов в исследуемых группах. В данном плане реакция оценивалась как активная (+) при визуализации более 50% лейкоцитов с внутриклеточным расположением фагированных микробов. 20-50% фагоцитируюших клеток соответствовало удовлетворительному фагоцитозу (±), наряду с частично или полностью переваренной микрофлорой встречалась также и не переваренная флора. Микробный фагоцитоз считали слабовыраженным (-) в том случае, если он наблюдался в менее чем в 20% нейтрофилов и микробная флора была не переваренной или с признаками частичного переваривания.
В основной группе активная фагоцитарная реакция наблюдалась в 160 (72,4%) случаях, тогда как в контрольной - только у 44 (10,6%) пациентов (р<0,05) (рис. 3).

Рис. 3. Результаты исследования активности фагоцитарной реакции
Цитологическое изучение интенсивности регенерации показало активную репарацию в 41,2% наблюдений в основной группе и в 12,5% – контрольной (р<0,05).
Результаты клинического и цитологического исследования верифицировались данными микробиологического обследования. До операции у всех пациентов основной и контрольной групп при данном исследовании мазка анального канала высевались различного рода микроорганизмы, в которых в 41,3% случаев доминировали энтерококки.
В результате коррекции нарушения КМБ в послеоперационном периоде на основе применения ЖББ нам удалось создать более благоприятные условия для репарации аноректальных ран. У больных основной группы уже на третьи сутки не обнаружен рост золотистого стафилококка, а фекальные стрептококки встречались в раневом отделяемом 38,9% больных (табл. 4).
Таблица 4
Микрофлора раневого экссудата в различные сроки после ГЭ
|
Микрофлора |
3-и сутки после операции |
7-е сутки после операции |
||
|
основная группа абс. (%) |
контрольная группа абс. (%) |
основная группа абс. (%) |
контрольная группа абс. (%) |
|
|
Эшерихии |
62 (28,4) |
150 (36,5) |
54 (24,5) |
118 (28,8) |
|
Протеи |
- |
- |
- |
35 (8,5) |
|
Синегнойные палочки |
- |
- |
- |
47 (11,5) |
|
Фекальные стрептококки (энтерококки) |
86 (38,9*) |
268 (65,4) |
60 (27,1*) |
244 (59,6) |
|
Золотистые стафилококки |
- |
35 (8,5) |
- |
32 (7,8) |
|
Бактероиды |
35 (15,7) |
90 (22,1) |
30 (13,7) |
59 (14,4) |
|
Гемолитические стрептококки |
6 (2,9*) |
47 (11,5) |
8 (3,9) |
16 (3,8) |
|
Ассоциации микроорганизмов |
15 (6,8*) |
162 (39,5) |
4 (1,8*) |
142 (34,6) |
|
Нет роста |
41 (18,6) |
- |
30 (13,7) |
- |
Примечание: * - достоверность различий при р<0,05.
В контрольной группе у 8,5% больных обнаружен рост золотистого стафилококка и у 65,4% - энтерококка. Подобная ассоциация двух и более видов микробов у больных основной группы имела место лишь в 6,8% наблюдениях, а в контрольной – в 39,5% (р<0,05).
В наблюдениях контрольной группы на 7-е сутки после ГЭ прослежена динамика роста частоты встречаемости ряда микроорганизмов по сравнению с основной группой. У больных основной группы даже через 7 суток после операции золотистый стафилококк, протей и синегнойная палочка отсутствовали. В контрольной группе отмечался рост протея в 8,5% случаях, синегнойной палочки в 11,5% наблюдениях и золотистого стафилококка в 7,8% случаях, при этом необходимо иметь в виду, что перед операцией и на 3-и сутки послеоперационного периода протей и синегнойная палочка не были обнаружены.
В основной группе послеоперационные осложнения воспалительного характера развились у 15 (6,7%), а в контрольной группе - у 83 (20,1%) (р<0,05). Нагноение послеоперационной аноректальной раны в основной группе установлено у 4 (1,8%) больных, а в контрольной группе - у 47 (11,5%) (р<0,05) (табл. 5).
Таблица 5
Послеоперационные раневые воспалительные осложнения
|
Осложнения |
Основная группа |
Контрольная группа |
||
|
абс. |
% |
абс. |
% |
|
|
Нагноение |
4 |
1,8 |
47 |
11,5* |
|
Инфильтрат |
6 |
2,7 |
16 |
3,8* |
|
Отек и гиперемия |
5 |
2,2 |
20 |
4,8* |
|
Всего: |
15 |
6,7 |
83 |
20,1* |
Примечание: * - достоверность различий при р<0,05.
Необходимо отметить, что в основной группе минимизация послеоперационных воспалительных осложнений обусловлена внедрением в комплексное лечение ЖББ, что способствовало снижению бактериальной контаминации послеоперационных ран аноректальной области.
На фоне комплексного лечения ЖББ у больных основной группы после операции были получены сравнительно лучшие результаты, чем в контрольной группе. Снижение бактериальной контаминации и активизация фагоцитарной реакции нейтрофилов позволили добиться сокращения длительности первой фазы раневого процесса и, соответственно, более быстрого развития грануляций.
Сроки окончательного заживления аноректальных ран у больных основной группы составили в среднем 17,4±1,9 дня, что достоверно отличается от аналогичного показателя в контрольной группе – 24,5±1,9 дня (р<0,05).
Нами проведено сравнительное изучение отдаленных результатов оперативного лечения геморроя. Отдаленный результат в сроки от 6 месяцев до 2 лет прослежен у 126 (57,0%) пациентов основной группы и у 243 (60,0%) – контрольной группы. На боли при акте дефекации жаловались 28 (11,5%) больных контрольной группы и 3 (2,4%) пациента основной группы. В контрольной группе стриктура анального канала развилась в 11 (4,5%) случаях, а в основной группе – у 1 (0,8%). Анальная трещина установлена у 9 (3,7%) пациентов контрольной группы и у 2 (1,5%) – основной группы. Среди больных контрольной группы у 7 (2,9%) обнаружена недостаточность анального жома 1 степени. Эти 7 больных были прооперированы по поводу хронического смешанного геморроя 3-4 стадии. В основной группе такого осложнения не зафиксировано.
Все вышеизложенные сравнительные результаты демонстрируют преимущества предложенного комплексного способа оперативного лечения геморроидальной болезни. Частота послеоперационных осложнений в отдаленном периоде составила 4,8% в основной группе и 22,9% в контрольной группе (р<0,05).
Выводы
Состояние КМБ у больных с геморроем имеет тесную связь с употреблением кисломолочных продуктов, содержащих бифидо- и лактобактерии. При регулярном употреблении кисломолочной продукции частота дисбактериоза составляет 4,8%, нерегулярный прием этих продуктов повышает частоту развития дисбактериоза до 91,1%, а при полном исключении из пищевого рациона кисломолочных продуктов дисбактериоз встречается в 96,7% наблюдений.
Разработанный способ коррекции КМБ на основе применения ЖББ в комплексном оперативном лечении геморроя достоверно (р<0,05) снижает количество патогенной энтеральной микрофлоры, частоту послеоперационных воспалительных осложнений с 20,1% до 6,7%, в частности нагноения аноректальных ран с 11,5% до 1,8%.
Модифицированный метод ГЭ по Миллигану-Моргану во второй модификации ГНЦ колопроктологии МЗ РФ с коррекцией КМБ обеспечивает благоприятное течение послеоперационного периода, значительно минимизирует сроки стационарного лечения и частоту специфических осложнений в ближайшем и в отдаленном послеоперационном периоде, что имеет большое клиническое и социально-экономическое значение.
Библиографическая ссылка
Исмаилов Н.Н., Калматов Р.К., Мирзакулов Д.С. КОМПЛЕКСНОЕ ЛЕЧЕНИЕ АНОРЕКТАЛЬНЫХ РАН ПОСЛЕ ГЕМОРРОИДЭКТОМИИ // Современные проблемы науки и образования. 2017. № 6. ;URL: https://science-education.ru/ru/article/view?id=27143 (дата обращения: 02.07.2025).



