Спаечная болезнь брюшины может осложняться острой и хронической кишечной непроходимостью. В случае экстренного поступления таких больных важным является определение жизнеспособности кишки, т.е. момента начала нарушения кровоснабжения слизистой оболочки кишки как наиболее обновляемой части кишечной трубки [1].
Несомненным достижением последних лет в хирургии органов брюшной полости стало понимание того, что использование лапароскопических технологий является профилактическим средством в развитии спаечной болезни брюшины. В то же время до сих пор остаются сомнения в возможностях использования данного метода при хирургическом лечении непосредственно хронической спаечной болезни брюшины [2].
С другой стороны, развитие минимально инвазивной техники привело к широкому распространению лапароскопических операций в абдоминальной хирургии. Первый ретроспективный анализ показал преимущества минимально инвазивных методик: уменьшение болевого синдрома, снижение риска развития осложнений, в первую очередь послеоперационного пареза кишечника, сокращение сроков госпитализации, короткий период реабилитации. С точки зрения технического выполнения лапароскопический контроль за ходом операции позволяет лучше видеть операционное поле, более тонко идентифицировать степень жизнеспособности органа при завороте, асептично и менее травматично проводить рассечение спаек, мобилизацию и пересечение органа [3-5].
Цель исследования: изучение возможности рентгеновской компьютерной томографии (РКТ) в диагностике хронической спаечной болезни брюшины (ХСББ) и выборе способа ее хирургического лечения.
Материал исследования
Под нашим наблюдением был 51 больной с хронической спаечной болезнью брюшины (ХСББ), находившийся на стационарном лечении в хирургическом отделении ГКБ № 13 г. Уфы, с 2012 по 2016 год. У всех больных ХСББ сочеталась с желчнокаменной болезнью.
Возраст больных варьировал от 31 года до 70 лет, средний возраст пациентов составил 44,3 ± 5,3 года, 28 (54,9%) больных были старше 60 лет. Мужчин было 31 (60,8%), женщин - 20 (33,9%). Все больные были разделены на 2 группы. В 1-й группе (25 чел. - 49,0%) в диагностической комплекс была включена РКТ, 2-я группа (26 больных – 51,0%) обследовалась традиционно, без РКТ. Рентгеновская компьютерно-томографическая диагностика осуществлялась на аппарате Aquilion RXL (Toshiba, Япония), для построения виртуальной модели применялось программное обеспечение VitreaAdvanced. Видеоэндоскопические вмешательства выполнялись на стойке «Карл Шторц», с использованием инструментов той же фирмы и отечественного набора фирмы «Эндомедиум».
После выполнения лапаротомии первым этапом выполняли рассечение спаек, в том числе осуществляли доступ к подпеченочному пространству, вторым этапом была холецистэктомия. Важнейшим этапом видеолапароскопической операции при ХСББ является введение лапароскопа (первого троакара), поскольку крайне велик риск повреждения полого органа. Даже в «открытой» хирургии встречаются факты случайного вскрытия просвета толстой кишки, приводящие к тому, что операция из «чистой» превращается в «грязную». Техника введения первого троакара несколько отличается у больных, ранее перенесших оперативные вмешательства из нижнего лапаротомного доступа или из доступа Волковича. В основной группе при проведении РКТ был выявлен спаечный процесс выше послеоперационного рубца и припаянные петли тонкой кишки, что заставило открыто вводить первый троакар выше пупка.
Для проведения лапароскопического лечения ХСББ необходим специальный инструментарий, в частности оптический троакар viziport «Autosuture», позволяющий послойное проведение троакара в брюшную полость под визуальным контролем.
В основной и контрольной группах, после введения видеолапароскопа, проводилась обзорная лапароскопия, уточнялся характер, тяжесть и распространенность спаечной болезни брюшины, возможность выполнения лапароскопического варианта оперативного вмешательства (лапароскопической холецистэктомии).
Следующим этапом вводились пятимиллиметровые троакары в третьей и четвёртой стандартных точках для выполнения лапароскопической холецистэктомии, через которые были проведены манипуляторы для осуществления адгезиовисцеролиза. Вначале проводилось освобождение брюшной стенки от висцеро-париетальных сращений, следующим этапом - от висцеро-висцеральных спаек. Рассечение спаек осуществляли от каудального конца, поэтапно осуществляем ревизию тонкой, а затем – толстой кишки.
В связи с ограниченными ресурсами, для резекционных способов лечения широко применялась техника би-биполярной коагуляции по Мельникову.
После выделения околопупочной области в первой стандартной точке устанавливается четвертый двенадцатимиллиметровый троакар. Через него вводятся дополнительные необходимые для завершения адгезиовисцеролиза инструменты.
Из технических приемов широко применяли оттеснение кишки, а не ее тракцию и захваты, даже при применении ретракторов с широкими браншами. В нашей клинике мы не использовали назогастральную интубацию тонкой и толстой кишки при ХСББ. Еще одной технической особенностью является широкое применение нами для перитонизации десерозированных участков разработанной клеевой композиции. Также старались меньше применять электрокоагуляцию для превенции электроожоговых осложнений.
Статистический анализ проводили с помощью Statistica 12 Trial, в том числе с вычислением критерия Chi-square с поправкой Йетса, в ряде случаев осуществлялась аппроксимация переменных.
Результаты. В основной группе при РКТ оценивались следующие параметры: наличие жидкости в брюшной полости, диаметр, толщина и структура стенки кишки, содержимое кишечника, рендеринг дилатированных петель кишечника, локализация выявленных изменений. Данное обследование позволяло оптимизировать точки доступа для видеолапароскопии.
Хирургическое лечение ХСББ осуществляли как этап оперативного лечения желчнокаменной болезни. У всех больных в анамнезе были различные оперативные вмешательства на органах брюшной полости (табл. 1), мы их разделили на две группы: 1-я группа - «верхние доступы», после грыжесечения по поводу пупочной грыжи, ушивания перфоративной язвы двенадцатиперстной кишки, среднесрединной лапаротомии после травмы органов брюшной полости. Вторая группа – «нижние доступы», которые включали рубцы на передней брюшной стенке при послеоперационной вентральной грыже после аппендэктомии, доступ Волковича-Дьяконова, послеоперационную вентральную грыжу после нижнесрединной лапаротомии. Такое распределение было в связи с особенностями оперативного вмешательства.
Таблица 1
Распределение больных по видам перенесенных ранее операций на органах брюшной полости
|
Основная группа (n=25) |
Контрольная группа (n=26) |
|||
|
Абс. |
% |
Абс. |
% |
|
|
Верхние доступы |
||||
|
Грыжесечение по поводу пупочной грыжи |
4 |
16,0 |
3 |
11,53 |
|
Ушивание перфоративной язвы двенадцатиперстной кишки |
3 |
12,0 |
4 |
15,38 |
|
Среднесрединная лапаротомия после травмы органов брюшной полости |
5 |
20,0 |
5 |
19,23 |
|
Нижние доступы |
||||
|
Послеоперационная вентральная грыжа после аппендэктомии |
5 |
20,0 |
4 |
15,38 |
|
Доступ Волковича-Дьяконова |
4 |
16,0 |
5 |
19,23 |
|
Послеоперационная вентральная грыжа после нижнесрединной лапаротомии |
4 |
16,0 |
5 |
19,23 |
|
Всего |
25 |
100,0 |
26 |
100,0 |
В основной группе у больных с «верхним доступом» (12 пациентов - 48,0%) при РКТ был выявлен спаечный процесс в области послеоперационного рубца, что потребовало введения троакара в левой подреберной области.
В контрольной группе («верхний доступ»), при ультразвуковом исследовании, в двух случаях (7,7%) не было выявлено конгломерата в области послеоперационного рубца, что привело к перфорации тонкой кишки, потребовало лапароскопического ушивания раны интракорпоральным ручным швом и удлинило оперативное вмешательство.
В контрольной группе при ультразвуковом исследовании у 8 (30,76%) больных определялся выраженный спаечный процесс, фиксированные к передней брюшной стенке петли кишечника, в связи с этим им был наложен пневмоперитонеум иглой Вериша в левой подреберной точке, а первый (10 мм) троакар для лапароскопа был введен во второй типичной (субксифоидальной) точке.
В основной группе резекция большого сальника потребовалась у 5 (20,0%) больных, в контрольной – у 6 (23,07%) пациентов.
На наш взгляд, достоинствами лапароскопического лечения ХСББ являются:
1. Прецизионность выполнения адгезиовисцеролиза.
2. Наличие пневмоперитонеума, позволяющего осуществлять тракцию париетовисцеральных сращений.
3. Оптическое увеличение зоны препаровки тканей в системе «видеокамера – монитор».
4. Применение манипуляторов существенно меньших размеров, в отличие от используемых в «открытой» абдоминальной хирургии.
Все вышеперечисленное в значительной степени позволяет уменьшить степень хирургической агрессии. Однако при массивном спаечном процессе, фиброзной плотности сращений, мы предпочитали конверсию. В основной группе случаев конверсии не было, в группе сравнения – переход на открытую операцию был у 5 (19,23%) больных.
По завершении этого этапа операции лапароскоп переводился в первую точку и выполнялся этап лапароскопической холецистэктомии.
Группу «нижнего доступа» составили 13 (52,0%) больных основной группы и 14 (53,84%) пациентов группы сравнения (табл. 1). В этих случаях последовательность хирургических манипуляций была несколько другой. Первым этапом выполнялось типичное («открытое») грыжесечение, в связи с тем что у значительного числа пациентов этой группы были сопутствующие сердечно-легочные заболевания (гипертоническая болезнь – 6 (22,22%), ишемическая болезнь сердца – 5 (18,51%), хронические обструктивные заболевания легких - 4 (14,81%), варикозная болезнь - 3 (11,11%) и пр.), открытый доступ не расширяли, а проводили лапароскопическую холецистэктомию, т.е. применяли технологию безгазового метода с мануальным ассистированием. Таким образом, существенно снижалась степень хирургической агрессии.
Десятимиллиметровый порт устанавливался на 5 см выше и левее относительно каудального конца лапаротомного отверстия, под контролем зрения. Далее осуществлялась экспозиция подпеченочного пространства путем подтягивания за брюшную стенку, за швы – держалки. Левой рукой осуществлялась экспозиция, а ревизия, мобилизация желчного пузыря и прочие действия в области треугольника Кало выполнялись эндодиссектором, установленным из второго порта. Ассистент проводил подтягивание за держалки, а также осуществлял тракцию области дна желчного пузыря эндограспером.
Достоинствами такого метода является открытая коагуляция, аспирация экссудата через обычный вакуум-отсос, удаление желчного пузыря через лапаротомную рану, что несколько сокращает время на погружение удаляемого органа в эвакуатор, и, таким образом, исключается возможность разрыва желчного пузыря и распространение содержимого по брюшной полости.
Этап грыжесечения заканчивали ненатяжной, протезирующей герниопластикой с установкой полипропиленового протеза.
Из особенностей выполнения эндовидеохирургической операции при сочетании ХСББ и желчнокаменной болезни необходимо отметить постоянное варьирование положениями больного на столе, от положения Тренделенбурга до позиции Фовлера при выполнении этапа холецистэктомии. Упомянутые выше технологии позволили избежать троакарного ранения. Нередко применяли точки для манипуляторов в подвздошных областях и мезогастральной области в основной группе в зависимости от данных рентгентомографического обследования (рис. 1, 2).
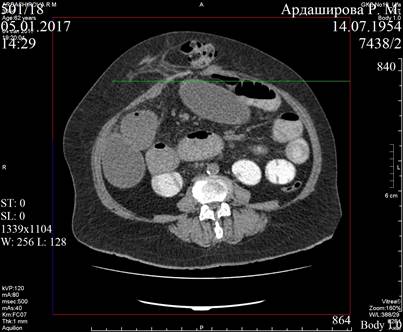
Рис. 1. Рентгентомография у больной с послеоперационной вентральной грыжей
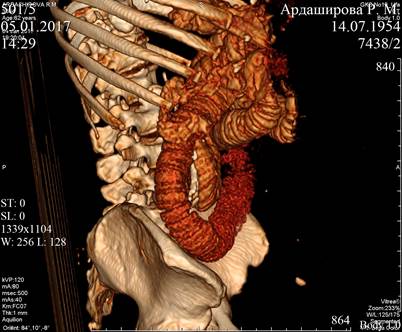
Рис. 2. 3D-реконструкция у больной с вентральной грыжей
В послеоперационном периоде в группе сравнения наблюдались следующие осложнения (табл. 2).
Таблица 2
Ранние послеоперационные осложнения у больных основной и контрольной групп
|
Основная группа (n=25) |
Контрольная группа (n= 26) |
|||
|
Абс. |
% |
Абс. |
% |
|
|
Нагноение троакарной раны |
1 |
4,0 |
1 |
3,84 |
|
Поддиафрагмальный абсцесс |
0 |
1 |
3,84 |
|
|
Межпетельный абсцесс |
0 |
1 |
3,84 |
|
|
Инфаркт миокарда |
0 |
1 |
3,84 |
|
|
Госпитальная пневмония |
1 |
4,0 |
1 |
3,84 |
|
Ишемический инсульт |
0 |
1 |
3,84 |
|
|
Тромбоэмболия легочной артерии |
0 |
1 |
3,84 |
|
|
Всего |
2 |
8,0 |
7 |
26,92 |
|
Умерло |
0 |
0 |
1 |
3,23 |
Из представленной таблицы видно, что в основной группе было статистически достоверно (Р < 0,05) снижено общее количество ранних послеоперационных осложнений, не было поддиафрагмальных и межпетельных абсцессов, всего 2 (8,0%) осложнения. Из общесоматических осложнений не встретились инфаркт миокарда, ишемический и геморрагический инсульты, а также тромбоэмболия лёгочной артерии. Соответственно, в группе сравнения данные осложнения встретились по одному случаю 7 (26,92) осложнений (Chi-square - 0,1363, поправка Йетса 0,2600).
В основной группе был 1 (4,0%) случай нагноения троакарной раны, аналогичное осложнение было в контрольной, также 1 (3,84%), оба пациента вылечены консервативно и физиотерапевтическими процедурами (Р < 0,05).
Послеоперационная пневмония также встретилась в обеих группах больных по одному случаю (в основной группе - 4,0% и 3,84% - в контрольной), что потребовало эндоскопической санации трахеобронхиального дерева и соответствующей антибактериальной терапии.
Причиной 1 (3,84%) случая смерти в группе контроля явилась тромбоэмболия легочной артерии.
Для подтверждения снижения степени хирургической агрессии при применении рентгентомографического исследования у больных ХСББ нами сравнены стандартные показатели у 25 пациентов основной группы и 26 больных в группе сопоставления. Была осуществлена рандомизация исследуемых групп по возрасту и полу (табл. 3).
Таблица 3
Оценка степени хирургической агрессии в основной и контрольной группах
|
Средняя длительность операции (мин.) |
Ранние послеоперационные осложнения (%) |
Послеоперационная летальность (%) |
Средний послеоперационный койко-день (сут.) |
|
|
Основная группа (n=25) |
124 ± 10,2 |
8,0 |
0 |
16 ± 2,3 |
|
Группа сравнения (n=26) |
176 ± 15,6 |
26,92 |
3,84 |
24 ± 3,6 |
Cредняя длительность операции в основной группе была статистически достоверно меньше (124 ± 10,2 мин.), чем в группе сравнения (176 ± 15,6 мин.) (Р < 0,05).
Ранние послеоперационные осложнений в основной группе были у 2 (8,0%), тогда как в группе контроля у 7 (26,92%) (Chi-square - 0,1363, поправка Йетса 0,2600).
Кроме того, в основной группе не было послеоперационной летальности, тогда как в группе сопоставления умер один больной (3,84%).
Среднее пребывание больных основной группы после операции было заметно меньше (16 ± 2,3 сут.), чем в группе сравнения - 24 ± 3,6 сут. (Р > 0,05).
Выводы. Применение РКТ в диагностике ХСББ имеет значительные перспективы, так как позволяет локализовать фиксированные кишечные петли, оценить жизнеспособность кишки, вследствие чего существенно снижается степень хирургической агрессии. Применение РКТ при хирургическом (видеолапароскопическом) лечении ХСББ существенно снижает частоту ранних послеоперационных осложнений и летальность.
Библиографическая ссылка
Нуртдинов М.А., Суфияров И.Ф., Ямалова Г.Р., Хабиров Р.Р. О РОЛИ РЕНТГЕНОТОМОГРАФИЧЕСКОГО ИССЛЕДОВАНИЯ В ЛАПАРОСКОПИЧЕСКОМ ЛЕЧЕНИИ СПАЕЧНОЙ БОЛЕЗНИ БРЮШИНЫ ПРИ СОЧЕТАНИИ С ЖЕЛЧНОКАМЕННОЙ БОЛЕЗНЬЮ // Современные проблемы науки и образования. 2017. № 3. ;URL: https://science-education.ru/ru/article/view?id=26417 (дата обращения: 02.07.2025).



