Применение любых активных форм кислорода (АФК) в биологии и медицине с саногенетическими целями неизбежно сталкивается с проблемой интенсификации свободно-радикального окисления (СРО), активации процессов перекисного окисления липидов (ПОЛ) биологических мембран, направленных на адаптивное в условиях гиперметаболизма повышение клеточной проницаемости. Поэтому использование окислительных методов терапии неразрывно связано с необходимостью исследования процессов липопероксидации, так как изменение баланса про- и антиоксидантных систем организма является одним из диагностических критериев тяжести патологического состояния, характеризуя формирование и прогрессирование окислительного стресса [1, 2, 9]. Однако при чрезмерной гиперстимуляции окислительного метаболизма может происходить не только модификация клеточной стенки, но и её альтерация, приводящая к повышению микроваскулярной проницаемости и системному поражению органов и тканей [1, 2]. В этой связи актуальна проблема изучения механизмов СРО при использовании разных концентраций АФК в условиях их хронического воздействия на организм млекопитающих.
Целью данной работы явилось изучение влияния разных доз озона (0,6; 2,0 и 8,0 мкг) на про- и антиоксидантные системы крови интактных крыс при длительном его применении.
Материалы и методы
Эксперимент выполнен на 50 крысах-самцах линии Wistar, содержащихся в стандартных условиях вивария в клетках при свободном доступе к пище и воде на рационе питания, согласно нормативам ГОСТа «Содержание экспериментальных животных в питомниках НИИ». Животных разделили на 5 групп. Продолжительность эксперимента составила 30 суток, в течение которых животным 1-ой группы (n=10) ежедневно внутрибрюшинно вводили 1 мл 0,9 % раствора NaCl с насыщающей концентрацией озона в кислород-озоновой смеси от озонатора «Медозонс-Систем – 3000 мкг/л и дозой О3 – 0,6 мкг на одно животное. Для животных 2-ой группы (n=10) насыщающая концентрация озона составила 10000 мкг/л и доза О3 – 2 мкг; 3-ей группы (n=10) – 40 000 мкг/л с вводимой дозой озона 8 мкг. Концентрацию О3 в физиологическом растворе определяли с помощью анализатора озона в жидких средах ИКОЖ-5 (сертификат соответствия RU.С. 31.001.А № 29545-05, г. Киров). Крысы 4-й группы (n=10) представлены здоровыми интактными животными без манипуляций (контроль 1), в 5-ой группе (контроль 2, n=10) животным проводили инъекции 1 мл 0,9 % раствора NaCl, насыщенного кислородом (кислород газообразный особой чистоты, марка 5,0, ТУ 2114-004-76237928-2013, объемная доля кислорода 99,999 %). Через 30 суток животных выводили из эксперимента путем декапитации под комбинированным наркозом (золетил (60 мг/кг) + ксила (6 мг/кг)).
Для исследований баланса про- и антиоксидантных систем использовали кровь, стабилизированную цитратом натрия (1:9). В плазме крови и эритроцитах изучали активность процессов СРО с помощью метода индуцированной биохемилюминесценции на биохемилюминометре БХЛ-06 (Н. Новгород). Оценивали следующие параметры хемилюминограммы: tg 2α – показатель, характеризующий скорость спада процессов СРО в плазме и свидетельствующий об общем антиоксидантном потенциале (АОА); S – светосумма хемилюминесценции за 30 сек. – отражает потенциальную способность биологического объекта к ПОЛ. Интенсивность ПОЛ определяли по уровню содержания вторичного продукта СРО – малонового диальдегида (МДА) в плазме и эритроцитах методом M.Uchiyama, M.Mihara [12], так как образующиеся в результате липопероксидации такие метаболиты, как альдегиды, кетоны, кислоты являются токсичными для организма. Карбонильные продукты подавляют синтез ДНК, вызывают внутри- и межмолекулярные сшивки полипептидов, модифицируют агрегацию тромбоцитов [2]. Среди ферментов, представляющих первое звено антиоксидантной защиты, исследовали супероксиддисмутазу (СОД), которая переводит супероксидный радикал в электронейтральную форму Н2О2. Активность СОД определяли в гемолизате отмытых эритроцитов (1:10) по ингибированию образования продукта аутоокисления адреналина [5]. Расчет удельной активности фермента осуществляли по концентрации белка, исследовавшегося модифицированным методом Лоури [7]. Результаты исследований обрабатывали с использованием программы Statistica 6.0. Значимость различий между показателями определялась с помощью t-критерия Стьюдента. Статистически значимыми считались различия при р<0,05.
Результаты и обсуждение
По данным биохемилюминесценции полученные результаты свидетельствовали о снижении про- и антиокидантного баланса в плазме крови животных контрольной серии с применением кислороднасыщенного физиологического раствора (рис. 1, 2).
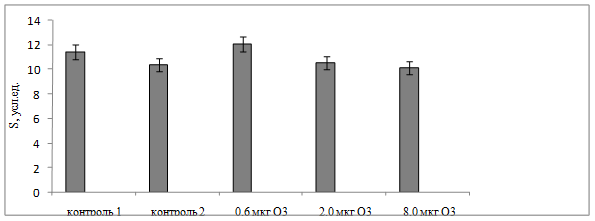
Рис. 1. Динамика изменения светосуммы хемилюминесценции в плазме крови крыс при воздействии различных доз АФК в условиях хронического эксперимента
При этом незначительное уменьшение светосуммы хемилюминисценции на 9 % по сравнению с показателем интактных животных (рис. 1) сопровождалось падением АОА на 20% (р=0,038) по сравнению с животными 1 контрольной группы (рис. 2).
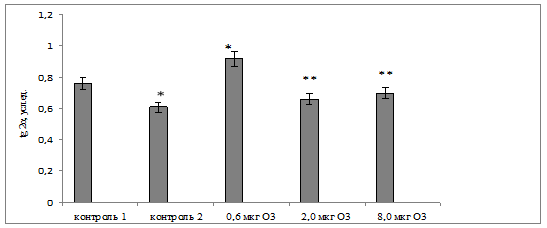
Рис. 2. Динамика изменения показателя tg2α в плазме крови крыс при воздействии различных доз АФК в условиях хронического эксперимента
Примечание: * – различия статистически значимы по сравнению с контролем 1 (p<0,05); ** – различия статистически значимы по сравнению с 0,6 мкг О3 (p<0,05).
Одновременно у крыс второй контрольной группы выявлено снижение cветосуммы хемилюминисценции в эритроцитах на 19 % (р=0,032) по сравнению с интактными животными (рис. 3), что может привести в условиях длительной кислородной интоксикации к нарушениям в биологических мембранах, связанным с изменением их проницаемости, ионного транспорта и физико-химических свойств мембранных белков и липидов, изменением активности мембранно-связанных ферментов, уменьшением электрической стабильности липидного бислоя мембран [6].
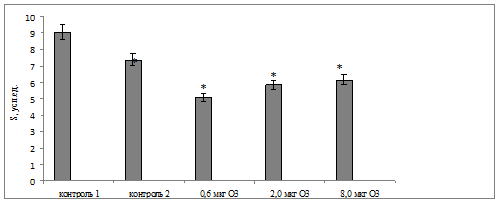
Рис. 3. Динамика изменения светосуммы хемилюминесценции в эритроцитах крыс при воздействии различных доз АФК в условиях хронического эксперимента
Примечание: * – различия статистически значимы по сравнению с контролем 1 (p<0,05).
Снижение общего уровня про- и антиоксидантного баланса на фоне длительного воздействия кислороднасыщенного физиологического раствора подтверждали также данные определения МДА и СОД. Полученные результаты выявили статистически значимое уменьшение концентрации МДА в плазме крови и эритроцитах соответственно на 53 % (р=0,034) и 61 % (р=0,021) после применения кислороднасыщенного физиологического раствора по сравнению с интактными животными (рис. 4). Удельная активность СОД во 2-ой контрольной группе уменьшилась на 26 % (р=0,028) по сравнению с контролем 1 (рис. 5).
Таким образом, изменения про- и антиоксидантного статуса под влиянием кислороднасыщенного физиологического раствора при длительном его применении свидетельствовали об уменьшении окислительного потенциала на системном уровне (кровь) и могли быть одной из причин ослабления сопротивляемости организма, снижения его иммунореактивности [11].
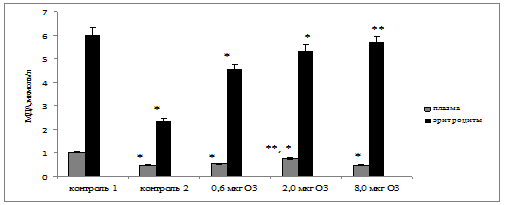
Рис. 4. Концентрация малонового диальдегида в крови крыс при воздействии различных доз АФК в условиях хронического эксперимента
Примечание: * – различия статистически значимы по сравнению с контролем 1 (p<0,05); ** – различия статистически значимы по сравнению с 0,6 мкг О3 (p<0,05).
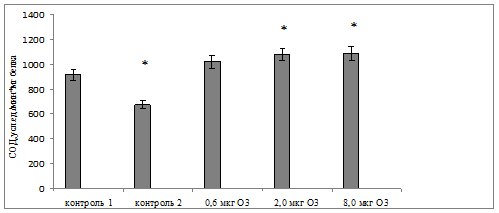
Рис. 5. Удельная активность супероксиддисмутазы в эритроцитах крови крыс при воздействии различных доз АФК в условиях хронического эксперимента
Примечание: * – различия статистически значимы по сравнению с контролем 1 (p<0,05).
Хроническое системное воздействие (в течение 30 суток) на животных АФК с существенно большим, чем у кислорода окислительно-восстановительным потенциалом – озоном при использовании его низкой дозы (0,6 мкг), незначительно стимулируя прооксидантный потенциал плазмы крови до +5 % (р=0,098) (рис. 1), снижало светосумму хемилюминисценции эритроцитов, свидетельствуя о повышении их перекисной резистентности на 44 % (р=0,022) (рис. 3). При этом выявлено возрастание АОА плазмы на 21 % (р=0,008) по сравнению с интактными животными (рис. 2). Под влиянием низкой дозы озона (0,6 мкг) активность СОД в эритроцитах увеличилась на 11 % (р=0,061) (рис. 5). Суммарное возрастание антиоксидантных свойств плазмы и эритроцитов препятствовало развитию оксидативного стресса, что сопровождалось снижением промежуточного продукта ПОЛ – МДА на 46 % (р=0,004) в плазме крови и на 25 % (р=0,025) в эритроцитах (рис. 4). Известно, что О3 способствует синтезу и активации каталитических свойств ферментов антирадикальной защиты: глутатионпероксидазы, каталазы и СОД [4, 8].
Хроническое воздействие большего количества АФК (дозы озона 2,0 и 8,0 мкг) по данным биохемилюминисцентного анализа сопровождалось снижением общего уровня прооксидантной активности. Об этом свидетельствовало уменьшение светосуммы хемилюминисценции в плазме крови на 8 % (р=0,064) и 11 % (р=0,084) соответственно (рис. 1), а в эритроцитах показатель S был снижен на 35 % (р=0,021) при воздействии О3 в дозе 2,0 мкг и на 32 % (р=0,034) при использовании 8,0 мкг О3 по сравнению с контрольной группой 1 (рис. 3). Высокие дозы озона (2,0 и 8,0 мкг) вызвали снижение общей антиоксидантной активности в плазме крови на 28 % (р=0,023) и 24 % (р=0,031) соответственно по сравнению с применением низких доз озона (0,6 мкг), что свидетельствовало об истощении, скорее всего, неферментативного звена антиоксидантной защиты (рис. 2). На этом фоне, в отличие от хронических воздействий чистым кислородом, при использовании больших доз О3 (2,0 и 8,0 мкг) удельная активность СОД в эритроцитах увеличилась на 18 % (р=0,041) и 19 % (р=0,035) соответственно (рис. 5). Это создавало условия для обрыва процессов ПОЛ. Концентрация МДА в плазме крови уменьшилась на 26 % (р=0,041; доза О3 – 2,0 мкг) и 54 % (р=0,023; доза О3 – 8,0 мкг) по сравнению с показателями животных первой контрольной группы, в эритроцитах – на 12 % (р=0,040) и 6 % соответственно (рис. 4).
Таким образом, хроническое парентеральное введение кислороднасыщенного физиологического раствора животным в течение 30 суток оказало ингибирующее действие на про- и антиоксидантный статус крови. Подобное снижение интенсивности окислительных процессов установлено также для токсического действия кислорода в исследованиях гипероксии, связанной с вдыханием кислорода под повышенным давлением [1]. Пусковые механизмы действия гипербарического кислорода на клетку (организм) реализуются через прямое (посредством включения кислорода в электрон-транспортные сети митохондрий), опосредованное (через свободнорадикальные механизмы) и рефлекторное (через рецепторы) влияние [1, 6]. Длительное применение озонированного физиологического раствора в диапазоне высоких доз озона (2,0 и 8,0 мкг) у крыс, не увеличивая АОА, оказывало стимулирующее действие на активность СОД, что могло снижать прооксидантные физиологические возможности АФК в организме животных. В условиях моделирования хронического воздействия АФК наиболее оптимальным оказалось применение низких доз озона в физиологическом растворе (0,6 мкг), которые, поддерживая активность процессов ПОЛ несколько выше уровня, чем у интактных животных, оказали модулирующее действие как на СОД, так и в целом на АОА крови. Данные литературы о влиянии О3 на каталитические свойства СОД и содержание МДА также подтверждают дозозависимый характер ответных реакций биологических систем на низкие и высокие дозы озона [10, 13]. Ранее установлено, что длительное использование низких доз озона способствовало умеренной физиологической активации оксидоредуктаз, тогда как дозы О3, превышающие 2,0 мкг, приводили к нарастанию тканевой гипоксии и накоплению в печени токсических продуктов [10].
Заключение
Результаты проведенного исследования позволяют констатировать, что длительное субхроническое воздействие кислороднасыщенным физиологическим раствором снижает в целом про- и антиоксидантный баланс в организме животных. Применение в аналогичных условиях низких доз (0,6 мкг) одной из активных форм кислорода, озона, сопровождается минимально инициирующим влиянием на ПОЛ в крови с преимущественным защитным антиоксидантным действием как на системном уровне (кровь), так и на клеточном (эритроциты). Использование более высоких доз озона (2,0 и 8,0 мкг), также стимулирующих СОД, сопровождается при этом уменьшением влияния О3 на окислительно-восстановительные процессы в организме, о чём свидетельствовали сниженные показатели хемилюминограмм и концентрации МДА в крови.
Библиографическая ссылка
Соловьева А.Г., Перетягин П.В. ИЗМЕНЕНИЕ ПОКАЗАТЕЛЕЙ ОКИСЛИТЕЛЬНОГО МЕТАБОЛИЗМА КРОВИ ПРИ ХРОНИЧЕСКОМ ВОЗДЕЙСТВИИ РАЗЛИЧНЫХ ДОЗ АКТИВНЫХ ФОРМ КИСЛОРОДА В ЭКСПЕРИМЕНТЕ // Современные проблемы науки и образования. 2016. № 2. ;URL: https://science-education.ru/ru/article/view?id=24432 (дата обращения: 24.01.2026).



