Однако в определённых условиях (передозировке, индивидуальной непереносимости) при применении цефоперазона могут возникать различные осложнения со стороны многих органов и систем организма, вплоть до анафилактического шока [6].
Поэтому для установления причин интоксикации лиц, принимавших цефоперазон, решающее значение принимают результаты химико-токсикологического исследования. В то же время, в хирургической практике, нередко возникает потребность проведения аналитического мониторинга концентрации препарата в биологических средах [10].
В литературе наиболее часто встречается информация об использовании ВЭЖХ при анализе цефоперазона [9]. Но в отечественной литературе отсутствуют данные об использовании для количественного анализа цефоперазона в биологических объектах капиллярного электрофореза.
Капиллярный электрофорез находит все более широкое применение в анализе лекарственных средств, в том числе в биологических средах [2,3,7]. Метод характеризуется доступностью для аналитических лабораторий (выпускаются отечественные сертифицированные системы «Капель – 105», «Капель – 105М» фирмы «Люмекс», г. Санкт-Петербург). Из достоинств данного метода необходимо также отметить отсутствие необходимости использования дорогостоящих и высокотоксичных растворителей и малый объём пробы вводимой в кварцевый капилляр (2 – 10 нл). Эффективное решение вопросов количественного определения лекарственных веществ в биологических объектах во многом зависит от важного этапа пробоподготовки (изолирования из объектов, очистки и концентрирования исследуемых соединений).
При разработке методики количественного определения исследуемого соединения в моче с использованием капиллярного электрофореза («Капель-105»), учитывая достаточно большую лабильность цефоперазона при длительном процессе пробоподготовки и содержания значительного количества соэкстрактивных веществ в исследуемых пробах, было предпринято уменьшение объема исследуемой пробы мочи до 0,1 мл. Жидкостно-жидкостное экстракционное концентрирование проводили в экспрессных условиях, исключая процесс упаривания полученного экстракта, с последующим реэкстрагированием исследуемого компонента в рабочий электролит, разбавленный в 10 раз водой. При этом, перевод исследуемого соединения в рабочий электролит, разбавленный в 10 раз, позволяет в процессе электрофореза в кварцевом капилляре дополнительно осуществлять концентрирование пробы за счет приема «стекинга». Концентрирование образца происходит в тот момент, когда заряженные аналиты пересекают границу, которая отделяет зону низкой проводимости раствора и высокой – ведущего электролита. Заряженные аналиты внутри зоны образца движутся с более высокой скоростью, за счет возникновения относительно более высокого электрического поля и, замедляясь на границе с зоной ведущего электролита, концентрируются.
Целью исследования явилось изучение возможности определения цефоперазона в моче капиллярным электрофорезом, с использованием отечественной системы капиллярного электрофореза «Капель – 105».
Материалы и методы исследования
Электрофорез цефоперазона проводили в системе капиллярного электрофореза «Капель-105», содержащий кварцевый капилляр с внутренним диаметром 75 мкм, длиной 65 см, встроенный УФ-спектрофотометрический детектор с изменяемой длиной волны от 190 до 380 нм. Запись и обработка данных проводилась с использованием программного обеспечения «Мультихром для Windows» (ЗАО «Амперсенд», Россия).
Условия электрофореза: рабочий электролит (РЭ) - буферный раствор Бриттона-Робинсона (pH 9,0); растворитель пробы (РП) – РЭ, разбавленный в 10 раз водой; ввод пробы - давлением (30 мБар х15 с); положительный электрод со стороны введения РЭ (напряжение: +20 кВ); детектирование в УФ области спектра, 230 нм.
Последовательная промывка капилляра между анализами осуществлялась: по полной схеме (между первым и четвертым анализами): 0,5 М раствором хлористоводородной кислоты – 10 мин, водой очищенной – 10 мин, 0,5 М раствором натрия гидроксида – 10 мин, водой очищенной – 10 мин, РЭ – 10 мин; проведение холостого электрофореза – 15 мин (положительный электрод со стороны введения РЭ, напряжение: +20 кВ); по короткой схеме (между вторым и третьим анализами): РЭ – 10 мин, проведение холостого электрофореза в тех же условиях, как и по полной схеме.
Запись и обработка данных анализа проводилась с помощью программного обеспечения «Мультихром для Windows».
С целью идентификации цефоперазона на электрофореграмме (ЭФГ), нами рассчитано наблюдаемое время миграции, в минутах (tm).
Методика количественного определения цефоперазона в моче («Капель-105»)
При разработке методики количественного определения цефоперазона готовили градуировочные растворы с содержанием 0,5; 1,0; 5,0; 10,0; 15,0; 20,0 мкг вещества в 1 мл РП. Проводили электрофорез полученных растворов в приведенных выше условиях:
Фотометрические сигналы (площади пиков) использовали для построения калибровочного графика (таблица 1, рис. 1).
Таблица 1
Зависимость фотометрического сигнала от концентрации цефоперазона («Капель – 105», РЭ – буферный раствор Бриттона – Робинсона, рН 9,0)
|
№ п/п |
Цефоперазон, мкг/мл |
Фотометрический сигнал, mAU*сек |
|||
|
mAU*сек |
mAU*сек |
mAU*сек |
mAU*сек ср. |
||
|
1. |
0,5 |
0,091 |
0,094 |
0,118 |
0,101 |
|
2. |
1,0 |
0,209 |
0,203 |
0,206 |
0,206 |
|
3. |
5,0 |
1,143 |
1,168 |
1,152 |
1,154 |
|
4. |
10,0 |
2,257 |
2,318 |
2,367 |
2,314 |
|
5. |
15,0 |
3,443 |
3,266 |
3,281 |
3,333 |
|
6. |
20,0 |
4,311 |
4,476 |
4,325 |
4,370 |
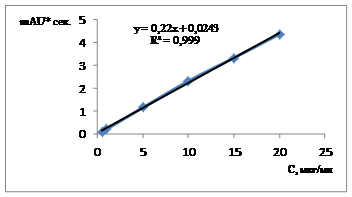
Рис.1. Калибровочный график для количественного определения цефоперазона методом капиллярного электрофореза («Капель-105»)
Результаты исследования показали, что в диапазоне от 0,5 до 20,0 мкг/мл наблюдается линейная зависимость фотометрического сигнала от концентрации цефоперазона. Коэффициент корреляции (R2) составил 0,999, что подтверждает линейность методики. Полученные данные были математически обработаны методом наименьших квадратов и в результате получено линейное уравнение: у = 0,22 х + 0,0243.
Количественное определение цефоперазона в моче.
При разработке методики количественного определения цефоперазона в моче предварительно было изучено влияния рН среды, природы и объема экстрагента, и кратности экстрагирования на степень извлечения вещества из водных растворов. Результаты исследования показали, что максимальное количество цефоперазона экстрагируется органической системой (хлороформ – изобутанол, 3:1) при рН 2,0 и кратности экстрагирования равной 3 [4].
Методика: к 0,1 мл мочи, содержащей определенное количество цефоперазона, добавляли 0,2 мл буферного раствора Бриттона – Робинсона, рН 2,0, и подвергали экстракции органической системой (хлороформ – изобутанол, 3:1), (1мл х 3). Эмульсию разрушали центрифугированием (6000 об/мин., 10 минут), органическую фазу отделяли и осуществляли реэкстрагирование 1 мл РП в течение 10 минут. Смесь центрифугировали (6000 об/мин., 10 минут). Реэкстракт отделяли и осуществляли дегазацию с использованием центрифуги («MiniSpin plus», 10 000 об/мин, 5 минут). Анализ полученных реэктрактов проводили в системе КЭ «Капель-105» в приведенных выше условиях.
Результаты представлены в таблице 2.
Таблица 2
Количественное определение цефоперазона в моче методом капиллярного электрофореза («Капель-105»)
|
№ п\п |
Цефоперазона в 0,1 мл мочи, мкг |
Определено цефоперазона |
Метрологические характеристики |
|
|
мкг |
% |
|||
|
1. |
20,0 |
14,70 |
73,50 |
S = 3,28 СV% = 4,43
S
ε% = 5,51 |
|
2. |
20,0 |
14,20 |
71,00 |
|
|
3. |
20,0 |
15,50 |
77,50 |
|
|
4. |
Контрольный опыт |
- |
- |
|
|
5. |
10,0 |
5,68 |
56,80 |
S = 2,25 СV% = 3,92
S
ε% = 4,87 |
|
6. |
10,0 |
5,98 |
59,80 |
|
|
7. |
10,0 |
5,54 |
55,40 |
|
|
8. |
Контрольный опыт |
- |
- |
|
|
9. |
5,0 |
2,57 |
25,70 |
S = 1,27 СV% = 4,97
S
ε% = 6,18 |
|
10. |
5,0 |
2,66 |
26,60 |
|
|
11. |
5,0 |
2,41 |
24,10 |
|
|
12. |
Контрольный опыт |
- |
- |
|
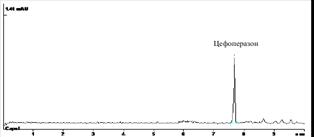
Результаты, представленные в таблице 2 показали, что количественное определение цефоперазона в модельных смесях мочи на трех уровнях концентрации, отражает удовлетворительную сходимость результатов в пределах рекомендуемой аналитической области. Рассчитанное стандартное отклонение среднего результата находится в пределах критерия приемлемости. При этом условия пробоподготовки биологической жидкости позволяют устранить влияние балластных веществ и эффективно осуществить УФ-спектрофотометрическую детекцию (рисунок 2).

А Б

В Г
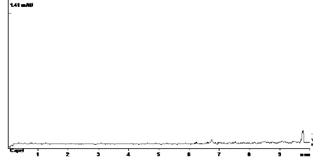
Рис.2.ЭФГ цефоперазона, выделенного из мочи при внесении 20 (А), 10 (Б), 5 (В) мкг вещества в 0,1 мл биожидкости; Г – ЭФГ после пробоподготовки контрольного образца мочи, 1 мл (blank); («Капель-105»)
Таким образом, разработанная методика на базе отечественной электрофоретической системы («Капель – 105») применима для количественного определения цефоперазона в моче, и может быть рекомендована для проведения анализа в химико-токсикологических лабораториях.
Выводы:
1. Разработана экспрессная методика определения цефоперазон в моче (объем пробы – 0,1 мл) на основе прямой экстракции органической системы (хлороформ – изобутанол в соотношении 3:1) с последующей реэкстракцией вещества в рабочий электролит, разбавленный водой, и электрофоретического исследования на приборе «Капель-105».
2. Показано, что по разработанной методике пробоподготовки, балластные вещества мочи не мешают фотометрическому определению.
3. Проведена валидационная оценка методики определения цефоперазона в моче. При статистической обработке полученные результаты находятся в пределах критериев приемлемости.
Рецензенты:Гейн В.Л., д.х.н., профессор, заведующий кафедрой общей и органической химии ФОО ГБОУ ВПО «Пермская государственная фармацевтическая академия» Минздрава России, г. Пермь;
Ярыгина Т.И., д.фарм.н. профессор, профессор кафедры фармацевтической химии ФОО ГБОУ ВПО «Пермская государственная фармацевтическая академия» МЗ РФ, г. Пермь.
Библиографическая ссылка
Крючков В.Б., Фомин А.Н., Смирнова А.В., Каджоян Л.В. ЭКСПРЕССНЫЙ ВАРИАНТ ОПРЕДЕЛЕНИЯ ЦЕФОПЕРАЗОНА В МОЧЕ КАПИЛЛЯРНЫМ ЭЛЕКТРОФОРЕЗОМ // Современные проблемы науки и образования. 2015. № 2-2. ;URL: https://science-education.ru/ru/article/view?id=22952 (дата обращения: 04.07.2025).



