Общепринятой является точка зрения о том, что хроническая венозная недостаточность (ХВН) развивается на фоне повреждения венозных клапанов после тромбоза вен нижних конечностей. Однако, патогенез ХВН точно не известен [5,10]. Поэтому, для улучшения клинических результатов необходимо более полное и глубокое исследование патогенетических механизмов развития и течения хронической венозной недостаточности, что позволит выработать новые медицинские технологии в ранней диагностики и лечение этих заболеваний [2,6].
Цель работы: исследовать метаболические нарушения при хронической венозной недостаточности нижних конечностей у женщин.
Для реализации поставленной цели нами было обследовано 34 женщины с посттромбофлебитическим синдромом (ПТФС) и 51 женщина с варикозной болезнью. Группу сравнения составили 30 здоровых женщин. Пациентки основных групп находились на стационарном лечении в сосудистом отделении ГБУЗ РМ «Республиканская клиническая больница № 4» г. Саранска.
Все обследуемые пациентки получали терапию, включающую дезагреганты, препараты, улучшающие микроциркуляцию, и антибиотики. При ПТФС применялись антикоагулянты, всем больным с варикозной болезнью выполнена флебэктомия. Результаты лечения оценивали на 3-и и 8-е сутки (в конце терапии).
Критериями включения в исследование служили женщины с заболеваниями вен нижних конечностей (посттромбофлебитический синдром, варикозная болезнь); пациентки с 3-ей или 4-ой степенью ХВН при варикозной болезни; добровольное согласие пациентов на участие в исследовании и использование результатов их обследования. Из исследования исключались мужчины с заболеваниями вен нижних конечностей; пациентки с посттромбофлебитическим синдромом, которые принимали до включения в исследование лекарственные препараты, направленные на повышение тонуса вен, улучшение лимфодренажной функции и микроциркуляторных расстройств.
Интенсивность метаболических нарушений определяли по накоплению малонового диальдегида (МДА) плазмы и эритроцитов (Колясова О.Е., Маркина А.А., Федорова Т.Н., 1984). Об антиоксидантной активности крови судили по уровню в ней каталазы (Бурлакова Е.Б., Архипова Г.В., Голощапов А.Н., 1982). Гидрофобный компонент эндогенной интоксикации (ЭИ) оценивали, определяя общую и эффективную концентрацию альбумина (ОКА и ЭКА) флуоресцентным методом на анализаторе АКЛ-01 с помощью набора реактивов «Зонд - альбумин». Рассчитывали индекс токсичности (ИТ) по формуле: ИТ = (ОКА/ЭКА) - 1 и резерв связывания альбумина (РСА) по формуле: РСА = ЭКА/ОКА (Грызунов Ю.А., Добрецов Г.Е., 1994). Оценивали содержание общих и свободных SH-групп по методу В.Ф. Фаломеева (1981г); исследование проводили не позднее 3 часов после забора и центрифугирования крови. Рассчитывали индекс детоксикации (ИДТ) по формуле: ИДТ = SH свободные/SH общие; коэффициент МДАпл/Капл, который свидетельствует о сдвиге реакций ПОЛ в прооксидантную или антиоксидантную сторону. Рассчитывали модифицированный лейкоцитарный индекс интоксикации (ЛИИм) по В.К. Островскому и соавт. (1983).
Статистическая обработка полученных результатов проведена с использованием t-критерия Стъюдента. Вычисления производились на персональном компьютере Pentium III с помощью программы «Medstat» (автор В.А. Акимов (С) Copyright 1993) и программы «Primer of Biostatistics 4.03» (Copyright 1998). Данные считались достоверными при уровне значимости p<0,05 (Закс Л., 1976; Поляков И.В., Соколова Н.С., 1975).
Корреляционный анализ параметрических данных проводился по методу Пирсона с использованием программы «Microsoft Excel» и таблицы минимальных значений коэффициентов корреляции Пирсона. При ±1>r>±0,7 отмечалась сильная, при ±0,69>r>±0,3 - средняя, при ±0,29>r>±0 - слабая прямая или обратная корреляционная связь.
Степень достоверности различий рассчитывали по отношению к группе сравнения (p), по отношению к соответствующему значению до лечения (pl).
Результаты исследований. Клинически эндогенная интоксикация при хронической венозной недостаточности проявлялась слабостью и недомоганием. Одновременно с этим происходило увеличение ЛИИм на 41,7% относительно группы сравнения при ПТФС и 58,3% при варикозной болезни.
При ХВН почти на четверть увеличивалось содержание МДА плазмы и эритроцитов, а уровень каталазы плазмы снижался на 13,7% (p<0,05) относительно группы сравнения у пациенток с ПТФС и на 23,3% (р<0,05) при варикозной болезни.
Консервативное лечение ПТФС приводило к недостоверному снижению уровня МДА плазмы и эритроцитов уже к 3-м суткам на 19,8% (p1>0,05) и 9,4% (p1>0,05). К 8-м суткам МДА плазмы, продолжая снижаться на 23,1% (p1<0,05) от исходного, достиг уровня, характерного для здоровых женщин. МДА эритроцитов к концу лечения, наоборот, несколько повысился, но остался ниже исходного показателя на 7,8% (p1>0,05), хотя и был выше, чем в группе сравнения. Согласованно с динамикой вторичных продуктов ПОЛ изменялась активность каталазы плазмы. Активность фермента несколько увеличилась к третьим суткам на 13,4% (p1<0,05), далее снизилась, превышая исходное значение на 12,2% (p1<0,05) и практически не отличалась от показателя у здоровых женщин (рис.1).
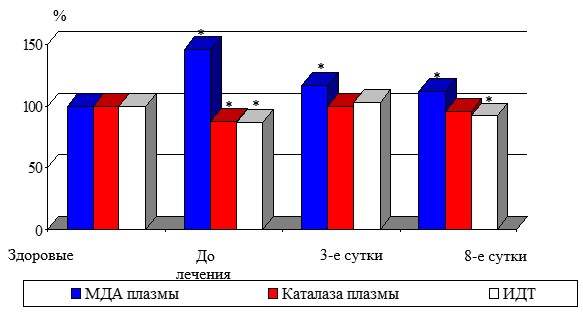
Рис. 1. Динамика показателей ПОЛ и АОС при посттромбофлебитическом синдроме
Примечание: * - достоверность показателя по отношению к группе сравнения (p<0,05)
Динамические изменения в системе ПОЛ-АОС при варикозной болезни на фоне терапии заключались в следующем: происходило недостоверное снижение уровня МДА плазмы к 3-м суткам на 5,5% (р1>0,05), а к 8-му дню - на 16,7% (р1<0,05), что было на уровне показателя в группе сравнения. МДА эритроцитов несколько уменьшился в процессе лечения на 6,9% (p1>0,05), что было на 17,1% (p>0,05) выше, чем в группе сравнения. Снижение вторичного продукта липопероксидации служит хорошим прогностическим признаком эффективности лечения. Активность каталазы увеличилась к 3-м суткам на 14,6% (р1<0,05), к 8-му дню - на 21,7% (p1<0,05). По сравнению с показателем, у здоровых женщин активность каталазы плазмы после лечения в третьей группе была практически на том же уровне (рис. 2). Отношение МДА/КА до лечения составило 3,95±0,14 усл.ед., что было на 19% выше контрольного показателя (p<0,05). На 8-ые сутки после флебэктомии коэффициент снизился на 24% (p1>0,05), что было на 9,6% (p<0,05) меньше, чем в группе сравнения.
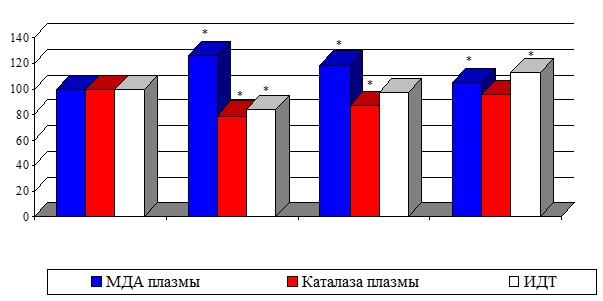
Рис. 2. Динамика показателей ПОЛ - АОС при варикозной болезни
Примечание: * - достоверность показателя по отношению к группе сравнения (p<0,05)
При анализе содержания тиоловых групп у пациенток с ПТФС выявлено снижение показателя общих SH-групп крови на 7,2% (p<0,05) относительно здоровых женщин. В свою очередь, свободные SH-группы достоверно не отличались от величины в группе сравнения. Однако наблюдалось уменьшение ИДТ по сравнению со здоровыми женщинами. Наиболее значимое повышение суммарных SH-групп было отмечено в первые трое суток терапии. К 8-м суткам темп прироста значительно уменьшился и составил в общем 8,4% (р1<0,01). Уровень свободных SH-групп уменьшился к третьим суткам лечения на 2,4% (p1>0,05). Но в дальнейшем произошло увеличение их концентрации в крови на 5,4% (p1<0,01) по сравнению с исходным показателем. ИДТ вырос к 3-м суткам почти на 18,2% (р1<0,05), но к окончанию терапии произошло некоторое снижение показателя и он стал равным индексу у здоровых женщин.
При варикозной болезни отмечалась тенденция к снижению общих и в меньшей мере свободных тиоловых групп по сравнению с группой сравнения. Эти изменения, больше чем в других обследованных группах, приводили к уменьшению индекса детоксикации на 15,8% (р<0,05). Снижение количества тиоловых групп является показателем уменьшения неспецифической резистентности организма [1].
В результате лечения к 8-м суткам после флебэктомии произошло увеличение концентрации общих тиоловых групп на 5,1% (p1>0,05) и снижение уровня свободных SH-групп на 12,2% (p1<0,05). Возможно, именно этот механизм дезактивации гидроперекисей имеет место при лечении варикозного расширения вен. Положительные сдвиги в системе ПОЛ-АОС привели к повышению индекса детоксикации на 15,6% (р1<0,01) на третьи сутки лечения и на 34,4% (р1<0,01) - на восьмые. При этом ИДТ стал выше, чем в контрольной группе, на 13,2% (р<0,05).
Нами не отмечено достоверного изменения ОКА в крови пациенток с посттромбофлебитическим синдромом, однако ЭКА была снижена почти на четверть. Резерв связывания альбумина (РСА) отражает долю центров альбумина, не блокированных метаболитами или токсинами. В группе пациенток с посттромбофлебитическим синдромом он был снижен на 22,7% (р<0,01). Индекс токсичности, отражающий взаимосвязь между выработкой и элиминацией токсичных продуктов, увеличился значительно, почти на 88,2% (р<0,001) по сравнению со здоровыми женщинами. Это свидетельствует о выраженном эндотоксикозе у данной категории больных.
Проводимая терапия посттромбофлебитического синдрома не оказывала значительного воздействия на общую концентрацию альбумина. ЭКА выросла к 3-м суткам на 9,6%, а к 8-м - на 20,8% (р1<0,05). Резерв связывания альбумина в начале лечения увеличился на 11,8%, а к концу терапии - на 17,6% (р1<0,05) по сравнению с исходным показателем, при этом остался ниже, чем в группе сравнения на 9,1% (p<0,05). Индекс токсичности был ниже исходного уровня на 30,2% (р1<0,01), что превышало показатель в группе сравнения на треть.
У пациенток с варикозной болезнью больше, чем в других группах, происходило накопление белковых катаболитов. Так, креатинин повысился на 14,0% (р<0,05), а мочевина - на 17,0% (р<0,05). В результате лечения с 3 суток происходило статистически значимое увеличение общего белка крови, которое к концу терапии достигло 8,1% (р1<0,05), при этом уровень его не отличался от контрольного показателя. Снижение креатинина и мочевины на 19,6% и 16,8% (р1<0,05), соответственно, также можно расценить как показатель уменьшения уровня интоксикации.
У пациенток с варикозной болезнью происходило уменьшение ОКА на 7,5% (р<0,05) и ЭКА на 25,0% (р<0,01). Резерв связывания альбумина изменялся меньше, чем при посттромбофлебитическом синдроме, - на 18,2% (р<0,01), а индекс токсичности возрастал в 1,68 раза. На 8-ые сутки после флебэктомии также изменялась связывающая способность альбумина: ОКА выросла на 7,0% (p1<0,05) и достоверно не отличалась от показателя в контрольной группе. Более значимый прирост ЭКА на 17% (р1<0,05) к 8-му дню не привел к нормализации показателя до уровня их у здоровых женщин. Полученные данные могут указывать на вовлечение альбуминовой фракции в процесс заживления послеоперационной раны.
Резерв связывания альбумина в ходе лечения также изменился и к 8-м суткам увеличился на 5,6 % (p1<0,05). Снижение индекса токсичности на 9,3% (p1<0,05) к 8-му дню не достигло уровня показателя в группе сравнения, превысив его в 1,5 раза.
Таким образом, консервативное лечение посттромбофлебитического синдрома, протекавшего в течение длительного времени, не приводит к полному устранению метаболических нарушений, о чем свидетельствуют повышенные уровни продуктов ПОЛ, сниженный резерв связывания альбумина и высокий индекс токсичности. В тоже время увеличение индекса детоксикации указывает на переход патологического процесса в стадию компенсации. Хирургическое лечение варикозной болезни нижних конечностей способствует коррекции метаболических нарушений, что свидетельствуют полученные результаты.
Рецензенты:
Мосина Л.М., д.м.н., профессор кафедры госпитальной терапии медицинского института ФГБОУ ВПО «Мордовский государственный университет им. Н. П. Огарева», г. Саранск;
Бякин С.П., д.м.н., профессор кафедры госпитальной хирургии медицинского института ФГБОУ ВПО «Мордовский государственный университет им. Н. П. Огарева», г. Саранск.
Библиографическая ссылка
Шулаткина А.В., Козлов С.А. МЕТАБОЛИЧЕСКИЙ ДИСБАЛАНС ПРИ ХРОНИЧЕСКОЙ ВЕНОЗНОЙ НЕДОСТАТОЧНОСТИ НИЖНИХ КОНЕЧНОСТЕЙ У ЖЕНЩИН // Современные проблемы науки и образования. 2015. № 5. ;URL: https://science-education.ru/ru/article/view?id=21451 (дата обращения: 17.01.2026).



