В Челябинской областной клинической больнице и в ЮУГМУ в течение 30 лет осуществляется разработка клинического использования высокоточного анализа вариабельности сердечного ритма (ВСР) при кардиоваскулярной патологии, в частности при ишемической болезни сердца (ИБС). Исходно предполагалось, что суперинтегральный пейсмекер первого порядка в сократительной деятельности сердца — синоатриальный узел сердца (СУ) — имеет многовариантные дизрегуляторные изменения при клинических формах ИБС. Одной из задач при этом было создание аппаратно-программного комплекса, диагностически направленного на высокоточную регистрацию физиологических и патологических изменений регуляции СУ при хронической и острой ишемии миокарда. Диагностический комплекс КАП-РК-01-«Микор» был создан в 1992 г., зарегистрирован и разрешен к применению для обследования больных (Регистрационное удостоверение № ФС 022б2005/2447-06 Федеральной службы по надзору в сфере здравоохранения). Процесс усовершенствования его программной части постоянен и, вероятно, бесконечен в связи с изменениями компьютерной техники и операционных сред [11]. В состав комплекса для точной регистрации электрокардиосигнала (ЭКС) включен портативный прибор – преобразователь ЭКС — ПРКГ-01 [5]. Такая структура специализированного диагностического комплекса обеспечивает техническими и программными средствами точную регистрацию ЭКС (1000 Гц, т.е. в 1/1000 секунды), такой же анализ ВСР и хранение в оперативной памяти компьютера, что существенно отличается от чувствительности прочих электродиагностических систем. Сочетание разработок трех направлений: прибор, программное обеспечение и клиническое применение — дало вполне положительный результат, применимый в практическом нейрокардиологическом обследовании пациентов. Клиническая разработка является самой затратной по трудоемкости, поскольку требует тысяч сопоставлений ВСР со стандартно применимыми методами диагностики и клиникой заболеваний.
Из доступных методов доказательной медицины клинические разработки в виде диссертационных исследований с применением метода ритмокардиографии высокого разрешения (РКГ) были приоритетными за последние 15 лет. Защищено и утверждено ВАК 27 таких работ. Каждая из них, пройдя через 5 ступеней контроля специалистами высокого и высочайшего уровней, явилась законченным фрагментом разработки практического применения РКГ. Такой исследовательский подход оказался вполне результативным, обусловливающим развитие клинической нейрокардиологии. И если в настоящее время метод РКГ все же не приобрел широкого распространения, несмотря на очевидные результаты и перспективы, причины того не имеют никакого отношения к мало доказательной медицинской науке и связаны с реально существующими недостатками поддержки отечественных инноваций начиная с местного уровня и до государственного. Что же все-таки уже удалось и доказано, а что еще предстоит привести к практическому результату, представляется в настоящей статье. Перспективы связаны с существованием лаборатории нейрокардиологии в главной больнице Челябинской области с ее почти 70-тысячной базой данных больных, обследованных c ВСР-анализом. Лаборатория была учреждена губернатором области в 2001 г. по просьбе профессора Ю.С. Шамурова, экс-ректора медицинской академии и одного из научных руководителей. Оборудование лаборатории пришлось создавать авторам метода РКГ и затем передать ЧОКБ в виде благотворительного вклада. К сожалению, все, что осуществлено с разработкой клинической РКГ, происходит в весьма сложное для здравоохранения время, несмотря на международное признание полезности и перспектив метода. В настоящей статье представлены результаты РКГ при ИБС от ранней ее диагностики до интервенционного вмешательства.
Метод ритмокардиографии высокого разрешения и его оснащение.
Специализированный аппаратно-программный диагностический компьютерный комплекс КАП-РК-01-«Микор» состоит из портативного прибора преобразователя ПРКГ-01, в котором с помощью схемно-технических устройств неинвазивно в течение 25 мин регистрируется ЭКС с передней поверхности грудной клетки испытуемого пациента тремя электродами с соблюдением специально разработанных условий (таких как отмена лекарственных препаратов в соответствии с периодами их полувыведения, алкогольных напитков, полная тишина, отсутствие двигательной активности, до приема пищи и лечебных процедур и др.). Функции ПРКГ-01 – последовательные фильтрация разночастотных помех и усиление ЭКС перед передачей в компьютер для высокоточного анализа ВСР [11, 5]. Точность регистрации ЭКС в 0,001 доли секунды сохранялась в оперативной памяти компьютера и в последующих расчетах волновой структуры ВСР [11,10]. Возможно, что такая точность и не предел. Использовался аутокорреляционный статистический и спектральный анализ 260–300 межсистолических RR-интервалов. Также для расчета соотношения 3 факторов регуляции пейсмекерной активности СУ – симпатического, парасимпатического отделов вегетативной системы, а также гуморально-метаболического влияния на медленные потенциалы в СУ — использовалось частотное вычисление соответствующих 3 энергетических вкладов в общий тотальный спектр колебаний ВСР с применением быстрого преобразования Фурье и спектральных окон Хамминга и Парсена. Спектральное соотношение факторов регуляции в СУ после разложения на частотные гармоники представлено долями (степенями) воздействия на пейсмекеры гуморально-метаболического влияния (VLF%), симпатического (LF%) и парасимпатического (HF%). Как принято в клинической вегетологии, запись ВСР осуществлялась с использованием проб по клинико-экспериментальному методу А.М. Вейна с соавт. [1], характеризующих регуляцию СУ в состоянии покоя (Ph), в пробах Вальсальвы—Бюркера (Vm) преимущественно парасимпатической направленности, гуморально-метаболической Ашнера (pA), симпатической активной ортостатической (Aop) и субмаксимальной нагрузочной (PWC120), включающей все 3 фактора регуляции СУ. В каждой из 5 позиций регистрировалось 260–300 RR-интервалов, всего 1500 при однократном РКГ-исследовании. Для корректности спектрального результата после физической нагрузки иногда записывалась шестая ритмокардиограмма (Ркг). Анализировались постстимульный результат стационарной Ркг и отдельно — периоды стимуляции в пробах по времени достижения максимального изменения RR интервала (tAB), максимальной реакции на стимул в процентах относительно исхода (ΔRR%), а также время восстановления 95% исходного интервала после действия стимула (tr), в Аор до 78–83% от исхода. Все показатели статистического анализа, tAB и tr представлены в секундах (с). Данные спектрального анализа – в процентах долей 3 энергетических вкладов в тотальный спектр, принятый за 100% спектральной плотности. Результат статистического анализа представлен показателями: средние величины продолжительности RR-интервалов на анализируемой Ркг–(RR), их стандартной девиации от среднестатистической величины (SDNN), среднеквадратические отклонения всех волн гуморально-метаболического влияния (σl), симпатического (σm), парасимпатического (σs), средняя амплитуда дыхательной аритмии (ARA) в секундах. Ркг здорового человека представлена на рисунке 1.
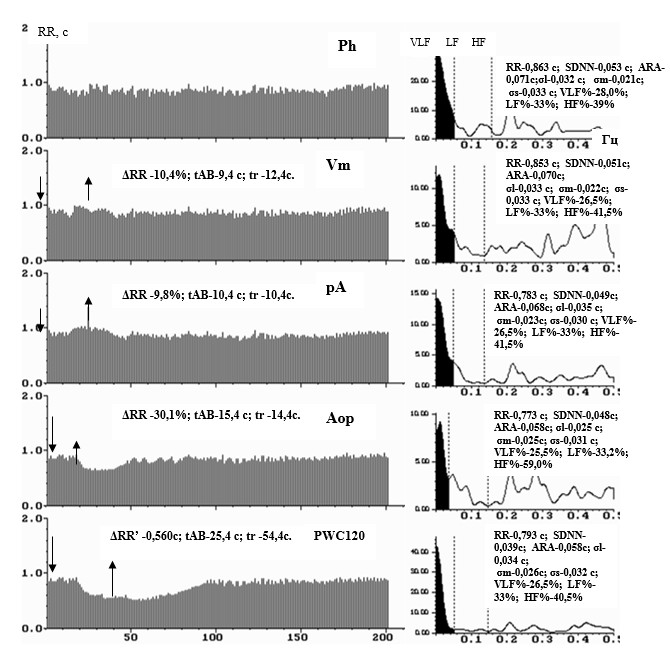
Рис. 1. Ритмокардиограммы, спектрограммы и средние значения показателей ВСР у здорового мужчины в покое (Ph), парасимпатическом маневре Вальсальвы—Бюркера (Vm), гуморальной пробе Ашнера (pA), в симпатической пробе активной ортостатической (Аор), нагрузочной пробе, дозированной по ЧСС 120 (PWC120). Средние показатели ВСР при аутокорреляционном статистическом анализе: RR — среднее значение всех RR-интервалов, SDNN – стандартное отклонение всех RR-интервалов, ARA – средняя амплитуда дыхательной аритмии, σl —среднеквадратичные отклонения гуморально-метаболических, σm – симпатических, σs –парасимпатических волн ВСР. Показатели спектрального соотношения энергетических вкладов долей гуморального (VLF%), симпатического (LF%) и парасимпатического (HF%) влияний в синусовом узле сердца относительно тотального спектра, принятого за 100%. Вертикальными стрелками отмечены начало и завершение стимуляции в пробах. Периоды стимуляции имеют показатели: ΔRR – максимальная реакция на стимул; tAB — время достижения максимальной реакции; tr – время восстановления после действия стимула в пробе. На спектрограммах – площади спектральной плотности соответствуют долям трех регулирующих воздействий в синусовом узле
Рассчитывались также показатели, нормированные на исход по формуле Wielder (1957), – nu для учета «Закона исходного уровня». Для выполнения РКГ-исследования при кардиохирургических вмешательствах была разработана модификация аппаратно-программного комплекса с мониторным режимом записи ВСР во время операции КАП-РК-02-«Микор». При математической обработке материалов использовалась программа «Stat» с проверкой гипотезы равенства вариационных рядов по критерию Стьюдента, а также критерию Z — аналогу t для непараметрических выборок большого объема. Для корреляционного анализа применен непараметрический метод Спирмена с пакетом SPSS 12.0. Регистрация и анализ интервалов осуществлялись с точностью до 0,001 с. Это составляет наиболее значимую особенность РКГ, отличающую ее от других предлагаемых вариантов аппаратно-программного обеспечения метода, в том числе от извлечений интервалов из записей Холтеровского мониторирования, предназначенных для ЭКГ и имеющих недостаточную степень дискретизации ЭКС (от 80 до 128 Гц). Многолетний опыт работы с анализом ВСР позволяет утверждать, что для регистрации и корректного анализа ВСР, оценивающего синаптический уровень регуляции в СУ, необходимы названная точность, корректное программное обеспечение и синхронная с Ркг запись ЭКГ в реальном текущем времени, что обеспечивает взаимоконтроль ЭКГ и РКГ. По решению врача возможны сохранение ЭКГ или ее фрагментов для детального анализа, увеличение и уменьшение масштаба записи.
Результаты исследования. В 2002 г. Миронов М.В., врач функциональной диагностики [7, 15], изучил с помощью РКГ периферическую вегетативную регуляцию СУ при стабильной стенокардии напряжения (Ст, n=171) и сердечной недостаточности (СН, n=123) у 294 больных ИБС. Выявлено, что ИБС облигатно сопровождается снижением периферической автономной регуляции хронотропной функции СУ и ишемическим поражением его пейсмекерных клеток с формированием их функциональной недостаточности. При ИБС в 100% случаев нарушения начинались со снижения амплитуды волн ВСР (σRR-SDNN), снижения σs и спектральной доли парасимпатического влияния -HF%, потери нормального протектирующего преобладания парасимпатической регуляции в СУ относительно нормы. В последующем снижалась амплитуда всех волн ВСР (σl, σm, σs), в частотном соотношении из-за названного снижения автономных долей регуляции СУ увеличивалась спектральная доля влияния гуморально-метаболического фактора регуляции — VLF%, снижалась реакция на действие разнонаправленных стимулов в пробах (всех ∆RR), увеличивалось время ее достижения (tAB) и восстановления после стимулов (tr) (рис. 2). При вазоспастическом варианте Ст перед ишемическим эпизодом усиливалась симпатическая периодика (σm= 0,017±0,005 c vs 0,008±0,002 c, n=24, p<0,05). При остром коронарном синдроме (ОКС) с субэпикардиальным поражением через все ткани желудочков сердца (n=24) и при субэндокардиальном синдроме (n=44) с нераспространенным поражением одинаково значиельно была снижена ВСР, регистрировались длительные эпизоды ишемии (рис. 3), но во 2-м варианте низкоамплитудная ВСР и нарушения ритма сохранялись.
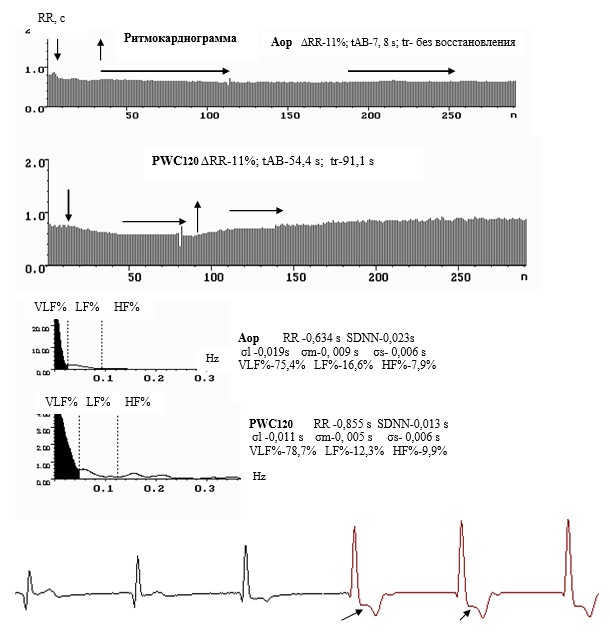
Рис. 2. Ритмокардиограммы, спектрограммы и средние значения показателей ВСР при ИБС и стабильной стенокардии в Aop и PWC120. Ишемические эпизоды стабилизации ВСР указаны горизонтальными стрелками. На ЭКГ стрелками указана синхронная депрессия ST. Статистические показатели SDNN, σl, σm и σs исчисляются единицами миллисекунд. В спектральном соотношении долей гуморально-метаболического, симпатического и парасимпатического влияний (VLF%, LF% и HF% ) на пейсмекерную активность синусового узла наибольшее воздействие принадлежит гуморальному фактору, медленному и недостаточному
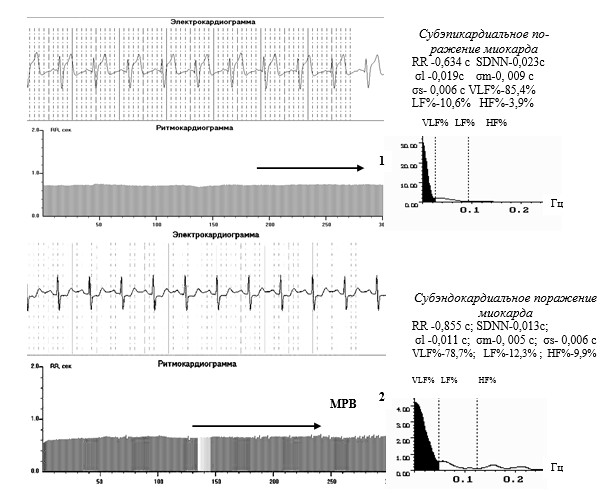
Рис. 3. Ркг, спектрограммы и средние значения показателей ВСР и ЭКГ с острым коронарным субэпикардиальным (1) и субэндокардиальным синдромами (2). В обоих случаях имеют место выраженное снижение волновой структуры ВСР в единицах миллисекунд (LF%, HF%) и длительные ишемические эпизоды (отмечены горизонтальными стрелками). В спектральном соотношении регулирующих факторов наибольшая спектральная плотность принадлежит очень низкочастотной периодике, соответствующей преобладанию неэффективного гуморального влияния в СУ(VLF%)
В прогредиентных наблюдениях найдены ВСР-доказательства не только симпатической и парасимпатической дизрегуляции, но и снижения показателей гуморально-метаболического влияния на потенциалы действия в СУ. Физиология автономных дизрегуляций и гуморально-метаболи-ческого воздействия различна, хотя и имеет одну точку приложения — пейсмекеры СУ. Поэтому объяснить однонаправленность их нарушений можно лишь единой причиной – состоянием самих пейсмекерных клеток СУ. Д.А.Учаевым, Е.В. Давыдовой и Э.А.Сафроновой [2, 12] был получен аутопсийный материал ткани СУ для электронной микроскопии у больных ИБС и у больных профессиональными заболеваниями в сочетании с ИБС. При хронической коронарной болезни сердца обнаружены структурные нарушения в самих пейсмекерных клетках СУ с разрушениями крист в митохондриях, кальцинатами, скоплениями фуксина, вакуолизацией, что в совокупности при ИБС свидетельствовало о дистрофических изменениях в пейсмекерах из-за хронического нарушения перфузии СУ (рис. 4, 5 и 6). Особенно это объяснимо при атеросклеротических бляшках в правой венечной артерии, от которой отходит артерия СУ.

Рис. 4. Рисунок Р-клеток синоатриального узла сердца в норме. Гистологический препарат клеток переходного типа проводящей системы сердца в области синоатриального узла сердца погибшего от внесердечной причины мужчины из группы контроля. Ультратонкий срез, контрастированный уранилацетатом свинца и цитратом свинца (увеличение 1260 и 1984 раз). Видны митохондрии с сохранными кристами внутри клетки (1)

Рис. 5. Гистологический препарат клетки переходного типа проводящей системы сердца в области синоатриального узла погибшего больного ИБС с автономной кардионейропатией. Ультратонкий срез, контрастированный уранилацетатом свинца и цитратом свинца (увеличение 1984 раза). Набухание множественных митохондрий и разрушение митохондриальных крист (1), кальцинаты в митохондриях (2). Внутриклеточные включения липидных капель (3) и липофусцина (4)
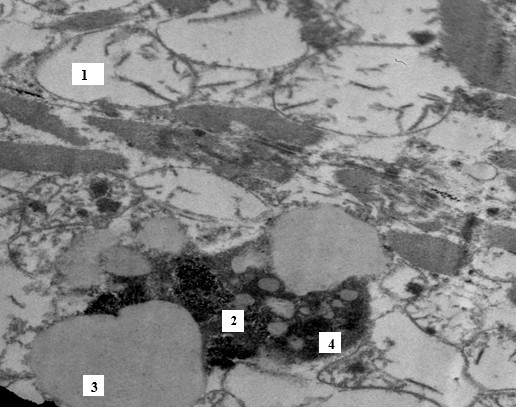
Рис. 6. Гистологический препарат клетки переходного типа проводящей системы сердца в области синусового узла погибшего больного с автономной кардионейропатией. Ультратонкий срез, контрастированный уранилацетатом свинца и цитратом свинца (увеличение 4000 раз). Набухание и разрушение митохондрий (1), депозиты кальция в митохондриях (2). Липидные капли на месте разрушенных митохондрий (3). Внутриклеточные включения липофусцина (4). ( На рис. 4, 5, 6 гистологические препараты Д.А.Учаева, Е.В.Давыдовой, Э.А. Сафроновой)
В исследовании М.В. Миронова наиболее полезен РКГ-симптом Ст в виде участков стабилизации ВСР с разницей между соседними RR-интервалами в 3,55±1,02 мс (рис. 2 и 3) во время ишемических эпизодов, по-видимому, из-за гибернации бледных клеток центральной зоны СУ в моменты наиболее значительного нарушения их кровоснабжения [3]. Стабилизация ВСР сильно коррелировала с клиническими, ЭКГ и ЭхоКГ симптомами Ст (r=0,725±0,017). Чувствительность же метода РКГ для диагностики Ст была 71,2% (т. е. в 2 раза выше, чем депрессия ST при ЭКГ), специфичность — 77%, прогностическая позитивная и негативная ценность — 62,1% и 84,5%. В свете найденного при высокоразрешающей РКГ можно предположить, что безболевая форма Ст все-таки имеет инструментальный РКГ-симптом. Выявлены также и дифференциально-диагностические показатели при СН: выраженное прогрессирующее снижение всех волн ВСР при предельно сниженном автономном воздействии, стабильное спектральное увеличение гуморально-метаболического влияния на пейсмекеры СУ, медленного, недостаточного, неадекватного и иногда парадоксального с замедленным достижением реакций и медленным восстановлением после стимулов в пробах (рис. 7), вплоть до формирования автономной кардионейропатии (АКН). Диагностическая ценность чувствительности РКГ при выявлении СН — 75%, специфичность — 43,5%, позитивный и негативный результат — 39,5 и 88,4%. АКН признана ВОЗ как маркер высокого риска летального исхода, приводится пример Ркг больного с АКН до коронарного шунтирования (рис. 8).
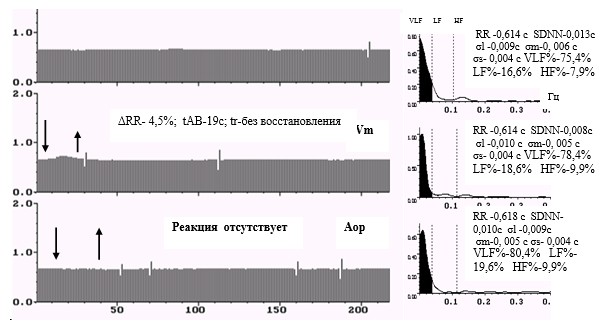
Рис. 7. Ркг, спектрограммы и средние значения показателей ВСР у больного с ишемической сердечной недостаточностью (СН) 3 ФК. Реакция в Vm снижена, в Аор отсутствует. Вертикальные стрелки показывают начало и конец действия стимулов в пробах. Статистические показатели ВСР выражены в единицах миллисекунд. В спектральном соотношении степени влияния факторов регуляции максимальная доля принадлежит гуморальному фактору регуляции, неэффективному и неадекватному. Автономная регуляция значительно снижена
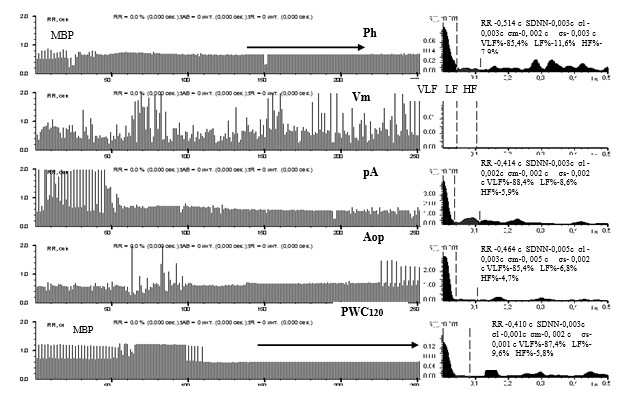
Рис. 8. Исходные ритмокардиограммы, спектрограммы и средние значения ВСР-показателей больного Д. до проведения коронарного шунтирования. В Ph (Ркг1) и PWC120 (Ркг4) значительно сниженная ВСР во время продолжительных эпизодов стенокардии. Между 1-м и 40-м интервалами — миграция водителя ритма (МВР). На фоне АКН между 130-м и 240-м интервалами длительный эпизод ишемии (указан горизонтальной стрелкой) с типичными клиническими проявлениями стенокардии. В Vm — фибрилляция предсердий. Среднеквадратичные отклонения амплитуды волн ВСР-SDNN, σl, σm, σs исчисляются единицами миллисекунд. В спектральном соотношении регулирующих факторов в СУ значительное преобладание гуморально-метаболического влияния(VLF%) над автономным симпато-парасимпатическим (LF%, HF%). В рА в начале записи между 1-м и 43-м интервалами синоатриальная блокада 2–3-й степени на фоне АКН и МВР. В Аор между 60-м и 100-м интервалами фибрилляция предсердий (ФП), затем ишемический эпизод со стабилизацией ВСР (разница между соседними RR-интервалами в пределах 3,55±1,02 мс) и в конце ортостаза суправентрикулярная бигеминия — СВБ (относительно одинаковые преэктопические интервалы), которая продолжилась во время ходьбы на тредмиле в PWC120, после чего вновь эпизод ишемии на фоне значительно сниженной ВСР, соответствующей АКН. Все аритмии возникали на фоне выраженного угнетения автономного влияния в СУ, что свидетельствует о протектирующем значении симпато-парасимпатической регуляции в СУ и повышении риска смерти при ее отсутствии. Больной умер на 4-й день после операции, что подтверждает значение АКН для прогноза летального исхода
В 1999 г. состоялась докторская защита В.А. Миронова по результатам клинического анализа волновой структуры синусового ритма сердца при гипертонической болезни [8], которая ассоциирована с ишемическим процессом как наиболее частый фактор риска. Из 1281 пациента с артериальной гипертензией после разнопрофильного обследования (в том числе многократная ЭКГ, Холтеровское мониторирование (ХМ), суточное мониторирование артериального давления, эхокардиография (ЭхоКГ)) были отобраны по специальным критериям включения и исключения больные с гипертонической болезнью (ГБ) 1-й и 2-й стадий (54 и 293 соответственно). Они были многократно обследованы методом РКГ в сравнении с контролем здоровых лиц (n=47), а также в сопоставлении между 1-й и 2-й стадиями. В работе были найдены особенности ВСР, характерные для ГБ и существенно отличающиеся от ВСР здоровых лиц с трехкомпонентной волновой структурой ритма. Высоко достоверные отличия были обнаружены и между стадиями ГБ. При ГБ 1-й степени у всех пациентов преобладающей периодикой ВСР были высокоамплитудные симпатические флуктуации (рис. 9). При этом почти вдвое ниже контроля оказался общий ВСР-показатель — SDNN (0,061± 0,018 vs 0,032± 0,013 с) с такой же, как в контроле, среднеквадратической дисперсией симпатических флуктуаций (σm = 0,023± 0,011 vs 0,025± 0,013 с). Максимально сниженной оказалась амплитуда парасимпатических волн (σm=0,011±0,008 vs 0,046± 0,017 с соответственно). Спектральное соотношение регулирующих факторов в СУ манифестировало с высокой достоверностью повышение гуморально-метаболического воздействия на пейсмекеры СУ (VLF%= 35,83±15,7 vs 23,42± 11,3% у здоровых) за счет значительного снижения парасимпатической регуляции (HF%=13,4±6,6 vs 57,0±17,4%) на фоне повышения симпатического влияния при ГБ1. Одновременно в период стимуляции в Аор при переходе в активный ортостаз увеличилось время восстановления (tr) как предвестник формирования гипертрофии левого желудочка (ЛЖ). ВСР при ГБ 2-й степени (рис. 10) существенно отличалась и от контроля, и от ГБ 1-й степени (рис. 1 и 9) значительным снижением ВСР (SDNN=0,021± 0,008 vs 0,061±0,018 и 0,032±0,013 c в контроле и при ГБ 1 соответственно p<0, 05-0,01). В периодах стимуляции достоверно снизились реакции на стимулы и увеличилось время достижения максимальной реакции и восстановления после действия стимулов. В совокупности такая динамика свидетельствовала об изменениях в тканях сердца при ГБ 2, патогенетически связанных с ремоделированием ЛЖ сердца. Поскольку высокое разрешение РКГ позволяет выявить тончайшие изменения в регуляции СУ, то удалось убедиться, что даже при разовой дозе лекарственных препаратов можно прогнозировать положительный или отрицательный результат лечения b-адреноблокаторами (b-АБ), антагонистами кальция или ингибиторами АПФ. Следовательно, с помощью РКГ возможно персонализировать медикаментозную терапию. Найдено, что при оценке σm ответ на неселективный b-АБ обзидан в разовой дозе был не симпатолитический. Парасимпатические показатели — ARA, σs — достоверно в 1,5 раза возросли, манифестируя холиномиметический результат (σm =0,017±0,007 до b-АБ и 0,015±0,009 c после b-АБ). Аналогичный результат показал и спектральный анализ. Средний же парасимпатический результат (σs=0,009±0,004 до и 0,016±0,009 с после b-АБ) наводил на мысль о холиномиметическом действии b-АБ, а не блокирующем b-адренорецепторы пресинаптической мембраны. Таким образом, совершенно узнаваемая визуально и в цифровых показателях оказалась стадийность ГБ при анализе ВСР. Метод же РКГ проявил свои возможности для персонализированной терапии при изучении вегетативных эффектов лекарственных средств.
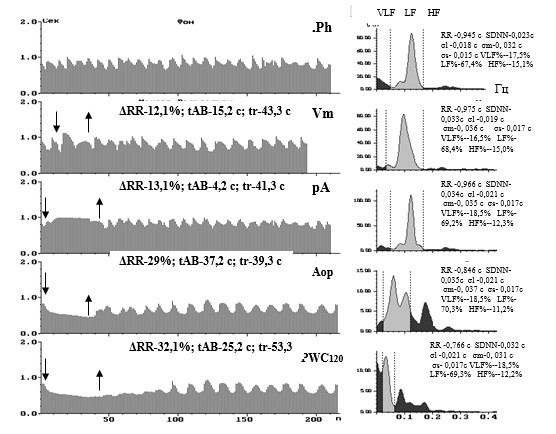
Рис. 9. Ритмокардиограммы, спектрограммы и средние значения показателей ВСР больного с гипертонической болезнью (ГБ) 1 степени. Преобладающая периодика на Ркг – симпатическая низкочастотная (σm), ей соответствует в спектральном отношении регулирующих факторов СУ наибольшая доля спектральной плотности в диапазоне 0,11-0,14 Гц. Статистические показатели среднеквадратичной дисперсии симпатических волн ВСР – σm наибольшие. Судя по увеличению времени достижения максимальной реакции в Аор (tAB-37,2 c против 15 с в норме), началось формирование гипертрофии левого желудочка сердца
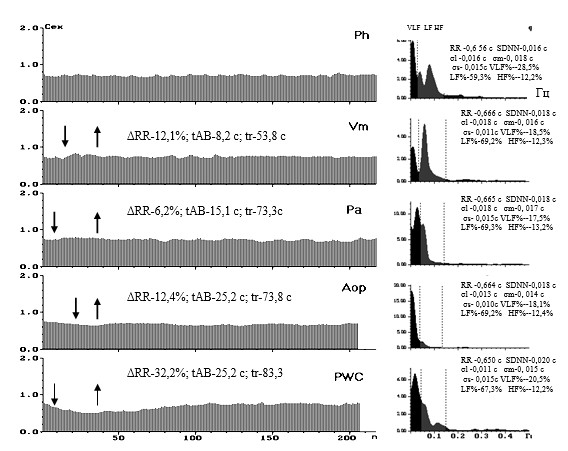
Рис. 10. Ритмокардиограммы, спектрограммы и средние значения показателей ВСР. Амплитуда волн ВСР существенно ниже нормы и показателей при ГБ 1-й степени. По-прежнему преобладает симпатическая периодика, в спектральном распределении долей влияния регулирующих факторов наибольшая спектральная площадь в низкочастотном диапазоне(LF%). Однако амплитуда флуктуаций исчисляется единицами миллисекунд. Снизились реакции ВСР на стимулы в пробах. Увеличилось время достижения максимальной реакции и восстановления после действия стимулов, что свидетельствует о ремоделировании тканей сердца в ответ на хроническую артериальную гипертензию
Изучая с помощью РКГ высокого разрешения антиаритмические эффекты феномена ишемического прекондиционирования у больных ИБС со стабильной стенокардией напряжения, Нохрина О.Ю. (2009) [10] выявила изменения волновой структуры ВСР в виде уменьшения суммарной продолжительности эпизодов ишемии с выраженной стабилизацией ВСР, временных и спектральных показателей автономной регуляции СУ с перераспределением степени влияния регулирующих факторов в СУ в сторону усиления парасимпатического влияния. Положительное влияние феномена «Разминки» зарегистрировано через 30 мин после провокации ишемического эпизода. По нашим данным, феномен сохраняется лишь при Ст 1 и 2 ФК.
Практические результаты получены Тюриным А.Ю. (2005) при многократном РКГ-обследовании 96 пациентов с острым инфарктом миокарда (ОИМ) в отделении реанимации и интенсивной терапии [13]. Найдены дифференцированные изменения ВСР при ОИМ передней и задней стенки левого желудочка (рис. 11), субэндокардиальном и субэпикардиальном остром коронарном синдроме (рис. 3). При ретроспективном анализе ВСР умерших (n=8) и оставшихся в живых (n=27) пациентов наименьшие значения автономной регуляции в единицах миллисекунд обнаружены у умерших больных. Это позволило установить, что значительно сниженная ВСР обратно и умеренно коррелирует с выраженностью риска летального исхода (r=0,412), поэтому является предиктором высокого риска смерти при ОИМ. Динамика улучшения и ухудшения состояния названных больных немедленно отражается в волновой структуре ВСР. В отдельных случаях регистрация аритмических эпизодов [4] является предвестником повышения названного риска.
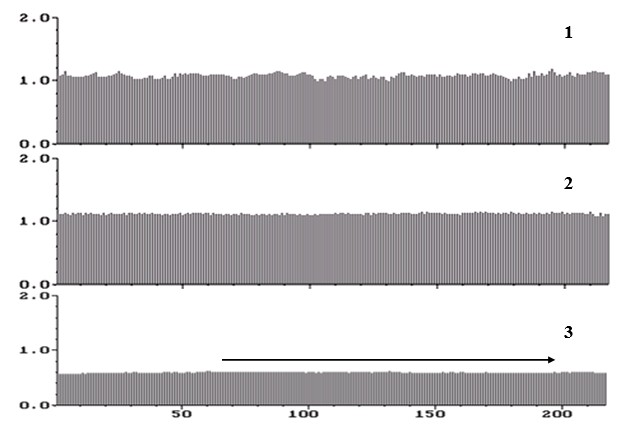
Рис. 11. Ритмокардиограммы при субэндокардиальном остром инфаркте миокарда (ОИМ) передней стенки левого желудочка (1), субэпикардиальном ОИМ передней стенки левого желудочка (2), субэпикардиальном ОИМ задней стенки левого желудочка сердца (3). На Ркг 1 сохранена волновая структура ВСР из-за эндокардиального поражения, но преобладают симпатические волны, по-видимому, из-за плотного расположения симпатических рецепторов в передней стенке левого желудочка сердца. На Ркг 2 более выраженное снижение амплитуды волн ВСР при субэпикардиальном поражении передней стенки левого желудочка. На Ркг 3 стабилизация ВСР при субэпикардиальном некрозе, ВСР соответствует автономной кардионейропатии
Апробация применения РКГ в кардиохирургии [9, 17] напрашивалось из-за высокого разрешения метода, менее чем за секунду откликающегося на малейшее воздействие, а также из-за отсутствия чувствительных маркеров, способных быстро идентифицировать актуальный кардиоваскулярный статус во время операции. При коронарном шунтировании (КШ) РКГ-исследование мониторно было осуществлено для анализа периферической вегетативной регуляции СУ при интервенционной реваскуляризации миокарда на открытом сердце у больных со стабильной Ст. На основе полученных результатов дана научно обоснованная оценка возможностям применения высокоразрешающего анализа ВСР для определения актуального периоперационного статуса при КШ. Куватовым В.А. [9] были с помощью РКГ обследованы 256 больных со стабильной Ст до КШ, во время проведения операции (n=123) и в раннем послеоперационном периоде (n=123). После первичного РКГ-исследования 133 пациента направлены на стентирование, КШ же на открытом сердце было проведено 123 больным. Результат оказался существеннее задуманного. Каждому этапу операции соответствовали физиологически объяснимые изменения ВСР. Некоторые примеры представлены на рисунках 12–14. Доказано, что анализ ВСР полезен в предоперационном периоде (рис. 8), поскольку именно он заранее позволяет предварительно выделить высокий риск жизнеопасных кардиоаритмий во время КШ, к примеру трепетание предсердий (рис. 14). Таким маркером была предельно сниженная ВСР с отсутствием на любые стимулы в пробах реакций SDNN, σm, σs и даже снижение σl до единиц миллисекунд. Следовательно, это была симптоматика, характерная для автономной кардионейропатии — АКН (рис. 8), признанная ВОЗ как симптом высокого риска летального исхода. Во время ишемических эпизодов на такой визуально стабилизированной Ркг разница между соседними RR-интервалами была в пределах 3,55±1,02 мс (n=20), что существенно ниже разрешающей возможности современных компьютерных экранов. Все случаи с исходной АКН до КШ сопровождались жизнеопасными аритмиями во время операции. В частотном соотношении регулирующих факторов СУ ведущим влиянием обладала гуморально-метаболическая среда (VLF%=95,73±7,64%), медленная и не обеспечивающая адекватного реагирования. Автономная же быстрая регуляция у больных почти отсутствовала (HF%=4,03±2,08% и LF%=3,76±2,005%). Реакции на стимулы в пробах также отсутствовали. Один из прооперированных больных с АКН скончался на 4-е сутки после КШ (рис. 8). Замечена зависимость возникновения кардиоаритмии (КА) от локализации манипуляций хирурга во время КШ. К примеру, предсердные аритмии возникали во время имплантации канюлей в сосуды (рис. 13 и 14). У пациентов с исходно сниженной, но все-таки сохранной ВСР с низкими реакциями в пробах на фоне клинически тяжелого состояния снижению ВСР соответствовала АКН. Сравнение ВСР до и после операции в течение первой недели показало ухудшение регуляции пейсмекерной функции СУ. Однако уже через одну неделю после КШ зарегистрировано улучшение волновой структуры ВСР со стойким повышением протективного парасимпатического влияния в спектральном соотношении факторов регуляции в СУ.
Во время международной конференции в 2012 г. впервые в мире продемонстрирована дистанционная в реальном текущем времени передача Ркг-записи из операционного зала в лабораторию нейрокардиологии ЧОКБ. Достижение осталось незамеченным.
При мониторной записи изучены поэтапно особенности анестезиологической регуляторной интраоперационной динамики в СУ во время КШ. У всех оперированных пациентов при введении в интубационный наркоз ВСР стабилизировалась (рис. 12). Во время канюляции сосудов, введения кардиоплегической смеси и, главное, при хирургических манипуляциях с тканями сердца были зарегистрированы кардиоаритмии (рис. 13 и 14). У всех вышеназванных пациентов с исходной до КШ АКН развилось трепетание предсердий (рис. 14). ЭхоКГ данные этих больных до КШ были сопоставлены с ВСР. Выявлены сильная и средняя положительная и отрицательная значимая корреляция ВСР-показателей (r=0,705–0,571) с увеличенными размерами правых полостей сердца, средняя и умеренная значимая связь их с толщиной задней стенки ЛЖ, межжелудочковой перегородки (r=0,577–0,410), конечно диастолическим и систолическим размерами ЛЖ, умеренная отрицательная значимая корреляция с фракцией систолы (r= –0,423), умеренная положительная и отрицательная значимая связь с гипертензией легочной артерии (r=0,370–0,398). В совокупности названные корреляции свидетельствовали об ассоциированности уже начавшихся структурных нарушений с ВСР-данными. Однако последние в их конкретной выраженности и однозначности опережали ЭхоКГ-нарушения. Следовательно, АКН по данным анализа ВСР является маркером тяжести кардиологического состояния, а также показателем необходимости специальных премедикаций, интраоперационного ведения больных во время КШ и персонализированной подготовки к фармакологической и интервенционной терапии. Результаты РКГ-исследования до, во время и после КШ у больных Ст подтвердили, что хроническая коронарная болезнь обязательно сопровождается дизрегуляциями пейсмекерной активности СУ, обусловленными перманентными нарушениями перфузии тканей сердца, в том числе СУ, а также повторяющимися ишемическими эпизодами, обеспечивающими морфофункциональную кумуляцию нарушения кровоснабжения и приводящими к необратимому моделированию. Это повышает риск опасных аритмий, влияющих на гемодинамику во время КШ на всех этапах вмешательства, снижает его успешность вплоть до летального исхода.
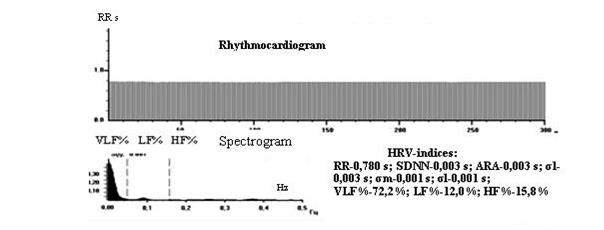
Рис. 12. Ритмокардиограмма, спектрограмма и средние значения ВСР-показателей во время коронарного шунтирования на этапе интубационного наркоза. Стабилизация ВСР, показатели SDNN, σl, σm, σs исчисляются единицами миллисекунд. В спектральном соотношении факторов регуляции пейсмекерной активности СУ значительное преобладание гуморально-метаболического влияния (VLF%) за счет снижения автономного воздействия (LF%, HF%)
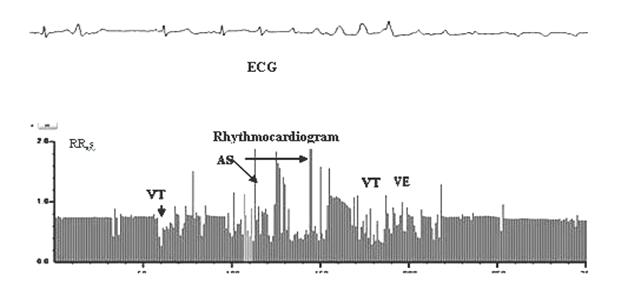
Рис. 13. Установка канюли в аорту во время коронарного шунтирования и введение кардиоплегической смеси для прекращения поступления крови из левого желудочка сердца перед подключением к аппарату искусственного кровообращения (АИК). Во время канюлирования и манипуляций хирурга нарушения ритма сердца – желудочковые экстрасистолы (VE), желудочковая тахикардия (VT), асистолия (AS)
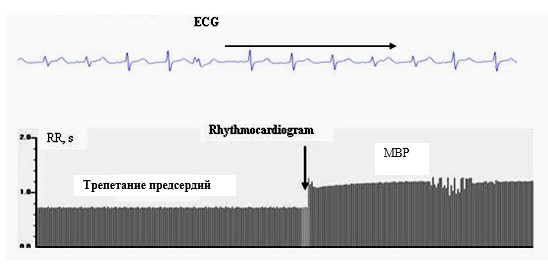
Рис. 14. Ритмокардиограмма и ЭКГ во время хирургических манипуляций на предсердиях. На Ркг – трепетание предсердий. Инсталляция канюль в вены, правое предсердие и аорту перед переводом кровообращения на АИК. На ЭКГ альтернация зубцов кардиокомплексов (указана горизонтальной стрелкой). Позднее на фоне повышения уровня Ркг — эпизод миграции водителя ритма (МВР)
Оценивались возможности РКГ-исследования для клинической диагностики кардиоаритмий (КА) [4, 6, 10, 15, 17]. Ретроспективно за 5 лет были отобраны 4620 пациентов, обследованных стандартными кардиологическими методами (ЭКГ, в том числе с ВЭМ, ДэхоКГ, мониторирование ЭКГ и АД, лабораторные анализы липидного профиля и др.). Также использовалась РКГ на КАП-РК-01-«Микор» с анализом ВСР. Представляются некоторые результаты использования РКГ в диагностике КА, а также некоторые примеры регистрации КА с помощью РКГ (рис. 15–20). Для оценки структуры КА и соотношения их клинических вариантов были проанализированы результаты РКГ у пациентов с различной кардиоваскулярной патологией, верифицированной данными клинических и инструментальных исследований. Распространенность КА при кардиоваскулярных болезнях составила 3313 случаев, почти 3/4. Желудочковые экстрасистолы встречались в 3 раза чаще, чем суправентрикулярные, — у 3483 и 1137 (75,4 и 24,6%) пациентов. В 2033 (44,4%) случаев они были сочетанными. КА, связанные с первичной сердечно-сосудистой патологией, были в 2343 (55%) наблюдениях. У 1617 (35%) больных она сочеталась с экстракардиальными болезнями, и по клинической актуальности вторые были ведущими — у 356 больных были обнаружены заболевания желудочно-кишечного тракта, у 330 – эндогенные интоксикации различного генеза, у 299 — дисгормонозы. Следовательно, данные подтверждали полиэтиологичность КА.
Наиболее клинически значимыми преимуществами для аритмологии можно считать возможность оценки автономного аритмогенного фона (что значимо для выбора фармакотерапии), а также определение влияния каждого эпизода КА на гемодинамику. РКГ-исследование как кратковременный, контролируемый, дозируемый в пробах мониторинг удобнее, чем ЭКГ и ХМ. Оказалось, что анализ Ркг позволяет определить связь КА с первичным патоморфологическим субстратом в сердце — наличием дополнительных проводящих путей, активных эктопических очагов, необратимой или частично обратимой дисфункции СУ. Эктопические очаги обычно были на фоне патологически измененной ВСР, часто — ее сглаженности и снижения реакций на стимулы, манифестирующих дистрофических изменений с заинтересованностью интрамуральной рецепторной ткани. Если активность КА была зависима от преобладания того или иного фактора регуляции СУ и в одном из тестов КА достоверно учащались, становились реже или исчезали, это позволяло судить о патогенетической связи КА с вегетативной регуляцией, а также об обратимости аритмогенного процесса. Автономный фон КА в большинстве случаев был связан с патогенезом основного заболевания. К примеру, при хронической ИБС клинико-экспериментальный характер анализа ВСР повышал возможности определения связи КА с преимущественным поражением сосудов, миокарда или с дисфункцией СУ. Если патогенез был связан с преимущественным поражением венечных сосудов (971 пациент), то фоном КА были снижение ВСР (низкие значения sRR, ARA,ss, sm), снижение или отсутствие реакции ВСР в Аор (DRR, соответствует коронарному резерву по Д. Жемайтите, 1989), участки выраженной стабилизации СР, синхронные с депрессией ST и клиническими признаками Ст. Обнаружена средняя и умеренная корреляционная связь стабилизации ВСР как ишемических эпизодов с клиническими ЭКГ- и ХМ-признаками Ст (r=0,473–0,610). Они оказались зависимыми по частоте и продолжительности от функционального класса (ФК) Ст, фиксированного или вариабельного порога ишемии. При остром коронарном синдроме (ОКС) эти участки стабилизации становились чаще и продолжительнее, порог ишемии — вариабельным. При субэпикардиальном варианте ОКС (54 пациента) стабилизация ВСР была предельно выраженной и соответствовала сформировавшейся АКН при p<0,01 (рис. 3). В 717 случаях ишемический эпизод предшествовал и провоцировал КА. У 154 больных КА была гемодинамически значима, и после эпизода аритмии на Ркг регистрировался эпизод ишемии (рис. 8, 19, 20).
Если же эктопия патогенетически была связана с преимущественным поражением миокарда и формированием сердечной недостаточности, это проявлялось увеличением времени достижения максимальной реакции (tAB) в Аор, ригидностью миокарда с РКГ-симптомами: увеличением tАВ и времени восстановления tr в PWC120, а также активацией эктопического очага при ослаблении активности СУ — КА учащались в Vm, рА. ВСР-симптомы коррелировали с дЭхоКГ-данными. Найдены значимая отрицательная корреляция потока Е в Аор и PWC120 c tAB — временем достижения максимальной реакции, положительная значимая корреляция между потоком А в Аор и PWC120 с тем же показателем, средняя отрицательная корреляция при сопоставлении Е/А в нагрузочной пробе с tАВ (r=–0,512–0,615), ДЗЛК и время изоволюмического расслабления положительно коррелировали в Аор и PWC120 с tAB. Результаты анализа ВСР свидетельствовали о начале формирования диастолической дисфункции миокарда, что при реально существующих сложностях ранней диагностики сердечной недостаточности может оказаться дополнительной клинически значимой симптоматикой. У 362 больных с дисфункцией синоатриального узла (ДФСУ), в том числе у 92 с синдромом слабости синоатриального узла (СССУ) [6, 16], зарегистрированы сверхкомпенсаторные паузы после экстрасистол и периодика Венкебаха с постепенным снижением декремента увеличенных постэктопических интервалов на фоне брадикардии, а также стабилизация ВСР — высокие значения RR и низкие — SDNN, ss, sm, HF%, LF%, хотя наблюдалось несколько случаев (у 17 пациентов) и с нормальной волновой структурой СР [6]. Это касается дифференциальной диагностики между ДФСУ и СССУ. ВСР многократно проанализирована у 268 и 92 пациентов с ИБС и с ДФСУ и СССУ 2-й степени 1-го и 2-го типа, у 2 лиц была периодика Мобитца. В анамнезе у всех были пресинкопы и синкопы. Классическим вариантом ДФСУ были симптомы: медленный выход импульсов из СУ, увеличивающий межсистолические интервалы, и средний RR, соответствующий брадикардии, повышенная реакция на парасимпатические стимулы в Vm и pA (увеличение RR и частоты эпизодов аритмий); зависимость аритмий от симпатических стимулов при выполнении постурального перехода в Аор или при выполнении нагрузки в PWC120 (эпизоды аритмий становились реже или исчезали); снижение Ркг и частоты эпизодов аритмий в атропиновой пробе. При СССУ постоянными РКГ-особенностями были: меньшая, чем при ДФСУ, зависимость частоты аритмических эпизодов от тонуса того или иного отдела вегетативной системы; зависимость СССУ от автономной регуляции была не столь прямолинейной, как при ДФСУ (учащение или урежение аритмий). При СССУ часто изменялись клинические формы кардиоаритмии. К примеру, экстрасистолия могла перейти в аллоритмию или смениться фибрилляцией предсердий. СССУ чаще, чем ДФСУ (у 74 и 139 пациентов соответственно при p<0,01), сопровождалась АКН со стабилизацией ритма и значительным снижением его реакций в пробах (рис. 20). При СССУ атропиновая проба была обычно отрицательная. Следовательно, в зависимости от дозы атропина аритмии могли стать реже (в 72 случаях), однако они никогда не исчезали полностью при СССУ. У всех больных в ответ на атропин снижались средние значения RR, SDNN, ss, число эпизодов аритмий. Однако при СССУ редукция была в достоверно большей мере (p<0,001); при СССУ чаще, чем при ДФСУ, были ЭКГ-симптомы миграции водителя ритма – изменения з. Р, PQ, альтернация R (в 92 и 132 случаях соответственно p<0,001). При дифференциальной диагностике между ДФСУ и СССУ найдено, что ВСР при дисфункции более сохранна, нежели при СССУ. Эти симптомы распознаваемы и по ЭКГ, однако РКГ-исследование удобнее. К тому же есть возможность диагностики периферической дизрегуляции СУ по данным ВСР [6].
Электрическая нестабильность миокарда на РКГ проявлялась желудочковыми экстрасистолами с удлиненной сверхкомпенсаторной паузой на фоне симпатической волны. Если после эпизода КА изменялись уровень и волновая структура ВСР на Ркг, это означало высокую возможность гемодинамических нарушений КА и высокий риск их жизнеопасности (рис. 17, 19). Вазовагальные синкопы (рис. 15) с обратно пропорциональным соотношением величин АД и межсистолических интервалов проявлялись повышением RR на фоне снижения АД и значений sm перед панической атакой Говерса. АКН является наиболее опасным вегетативным фоном для возникновения гемодинамически значимых и, стало быть, — жизнеопасных кардиоаритмий. При АКН регистрируются выраженное снижение всех РКГ показателей, отсутствие реакций на стимулы, что соответствует по N. Ewing (1978) 50%-ному риску смерти. АКН при этом была распознаваема на Ркг визуально. По данным электронной микроскопии СУ у умерших пациентов (n=14), имевших при жизни АКН, в Р-клетках СУ найдены структурные дистрофические изменения (рис. 4–6).
Анализ ВСР оказался полезным при оценке влияния экстракардиальных патологических процессов на частоту КА, а также для выбора и контроля медикаментозной терапии. Данные имеют достоверность, метод же РКГ-исследования — достаточные специфичность (66,4–71,5%) и чувствительность (71,2–77,1) в сопоставлении с референсными исследованиями, что предполагает заинтересованное внимание аритмологов к РКГ. В кардиологической практике РКГ-обследование оказалось значительно удобнее, чем ЭКГ и ХМ, для характеристики КА по количеству эктопических очагов, их желудочковой и предсердной локализации, времени появления в диастоле, частоте и взаимосвязи. Желудочковые и суправентрикулярные экстрасистолы различались на РКГ визуально и математически по наличию и отсутствию компенсаторной паузы, хотя при высокоразрешающей РКГ названная компенсированность не настолько точна, как принято считать. Регулярные би-, три- и квадригеминии легко распознаваемы на РКГ по чередованию нормальных интервалов и пар пре- и постэктопических пауз. Физиологическая тахикардия отличалась постепенностью снижения и восстановления величины RR-интервалов. Пароксизмальная же синусовая тахикардия возникала на фоне большего или меньшего снижения ВСР, вход и выход из пароксизма сопровождались аритмиями различных клинических форм (n=94). Тахикардия при повышенной гормонопродукции щитовидной железы сопровождалась высокой и продолжительной реакцией на рА. Так же, как и в случаях со сложными КА, РКГ-исследование позволяло конкретизировать характер автономного вмешательства в патогенез аритмий. Преимущественное участие в патогенезе КА парасимпатического отдела проявлялось учащением нарушений ВСР в Vm, симпатического — в Аор и/или в PWC120. Появление или учащение КА в рА при патологии гормонопродуцирующих органов обнаруживало их связь с нарушениями гормонального фона (r=0,610).
Использование РКГ-исследования определяло подбор медикаментозного воздействия и для купирования КА, и для коррекции патогенетического фона, что в конечном итоге предъявляло повышенные требования к индивидуальному выбору лечения и доз разового и курсового приема лекарственной терапии. В этой части наблюдений были выявлены ранее нигде не описанные свойства препаратов, в том числе и широко применяемых в кардиологии. К примеру, лечение b-адреноблокаторами оказалось наиболее эффективным при преобладании низкочастотной симпатической m-периодики ВСР, антагонистами кальция и ингибиторами АПФ — при стабилизации ВСР. Доказано [8, 10, 14, 16] , что РКГ содержит возможности для исследования периферических вегетативных эффектов препаратов, воздействующих на пре- и постсинаптическом уровнях соотношения вегетативных терминалей и клеток-эффекторов.
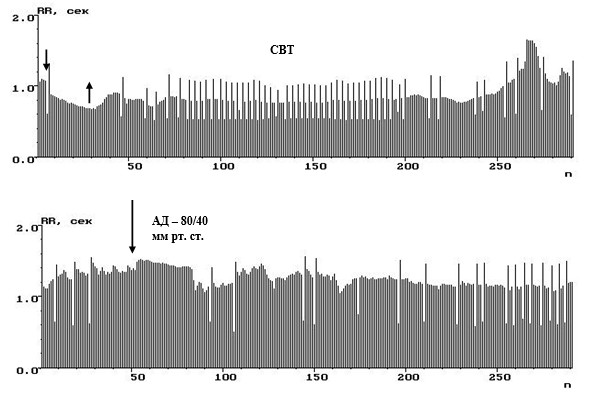
Рис. 15. Ритмокардиограммы при вазо-вагальном синдроме Говерса (паническая атака) в активной ортостатической пробе. На Ркг1 в активном ортостазе суправентрикулярная тригеминия (СВТ). К концу активного ортостаза уровень Ркг увеличился и на Ркг2 возрос до 1,5 с (ЧСС 40 в мин.). На фоне максимального повышения снизилось артериальное давление. В результате при сочетании выраженной брадикардии, низкого АД и нарушения церебральной перфузии у пациента началась потеря сознания
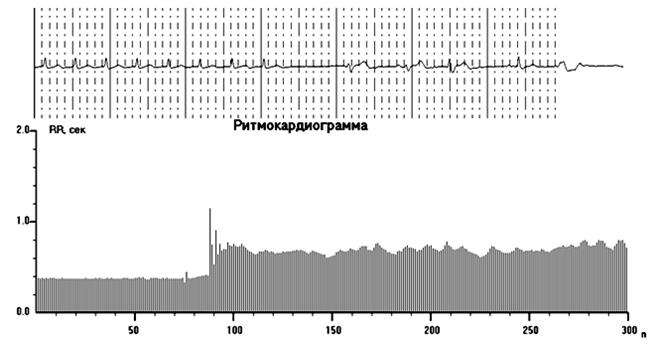
Рис. 16. Пример Ркг и ЭКГ при купировании пароксизма АВ узловой реципрокной тахикардии аденозинтрифосфатом с восстановлением синусового ритма с симпатической активацией – информация, необходимая для подбора медикаментозной терапии. Cудя по усилению симпатических волн ВСР, необходимо продолжить лечение β-адреноблокаторами
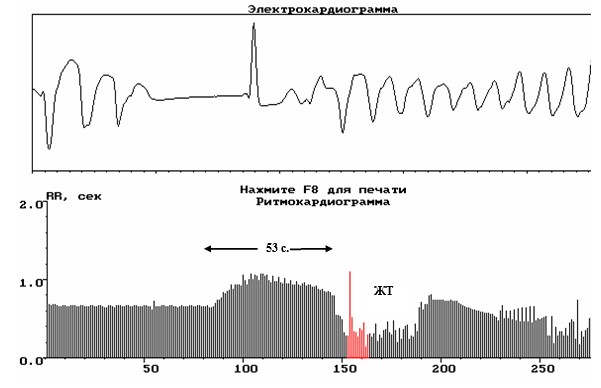
Рис. 17. Ритмокардиограмма и ЭКГ пациентки во время желудочковой тахикардии (ЖТ). В данном случае предиктором пароксизма было повышение уровня Ркг (урежение ритма) за 53 с до фибрилляции желудочков сердца. За это время в условиях реанимации успели подготовить меры, необходимые для прерывания жизнеопасной аритмии, и больная осталась жива
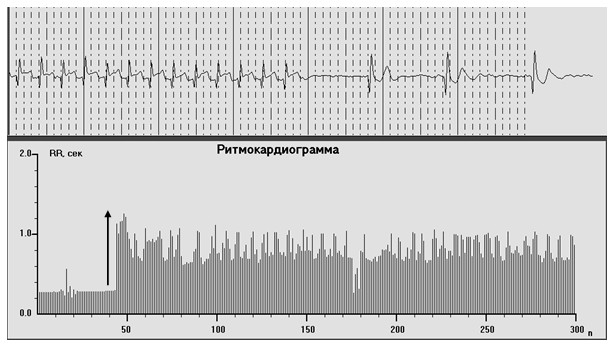
Рис. 18. Ритмокардиограмма и ЭКГ при суправентрикулярной АВ узловой тахикардии. Выход из пароксизма на 43-м RR-интервале с дальнейшим узловым медленным ритмом (синдром «тахи-бради» на уровне АВ узла)
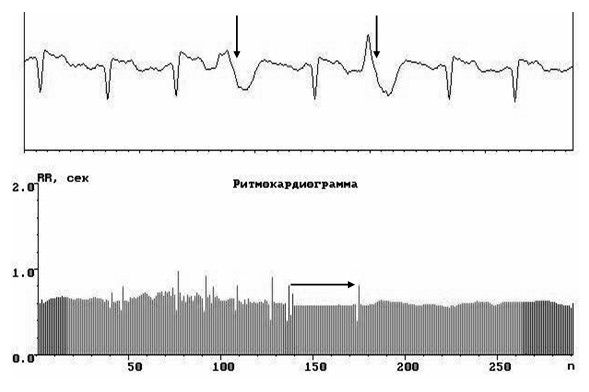
Рис. 19. Ритмокардиограмма и ЭКГ у больной с ИБС. Здесь зарегистрированы экстрасистолы, провоцировавшие гемодинамически значимый эпизод ишемии (показан горизонтальной стрелкой) в виде стабилизации ВСР и последующего усиления влияния гуморально-метаболического фактора регуляции в синоатриальном узле сердца – после ишемического эпизода заметно преобладание гуморальной периодики
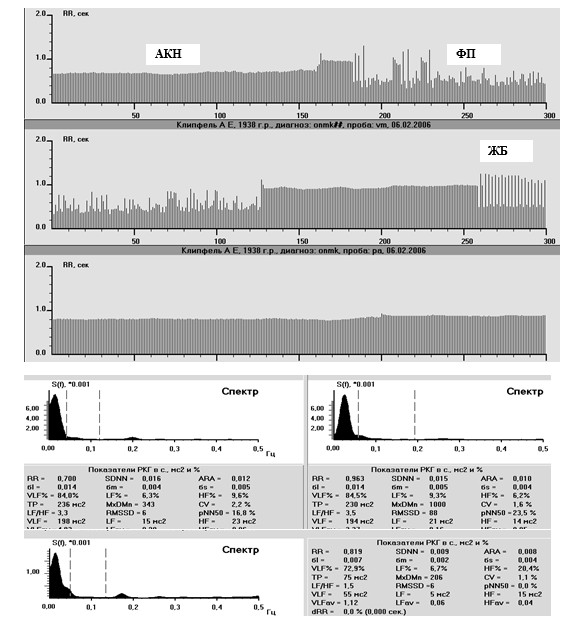
Рис. 20. Ритмокардиограммы, спектрограммы и средние ВСР-показатели пациента с синдромом слабости синусового узла – СССУ и автономной кардионейропатией (АКН). АКН на Ркг1 трансформировалась в фибрилляцию предсердий (ФП), в конце 2-ой Ркг зарегистрирована желудочковая бигеминия (ЖБ). Статистические показатели ВСР – SDNN, σl, σm, σs выражены в единицах миллисекунд. На спектрограммах наибольшая спектральная плотность в очень низкочастотном диапазоне –VLF%, что свидетельствует о преобладающем влиянии гуморально-метаболического фактора и выраженном угнетении быстрой автономной регуляции в СУ (LF%, HF%) соответственно симптомам АКН
Выводы:
1. Выявлены РКГ-симптомы, характерные для хронического ишемического процесса при формировании сердечной недостаточности в виде снижения ВСР по показателям симпато-парасимпатической автономной регуляции. При ишемической сердечной недостаточности снижается амплитуда всех волн ВСР (σRR-SDNN) за счет редукции амплитуды симпато-парасимпатических флуктуаций σs и σm, значительного и высокодостоверного снижения спектральной парасимпатической доли влияния — HF%, а также соответствующего увеличения доли спектрального влияния гуморально-метаболического фактора регуляции в СУ — σl% (VLF%). Снижаются реакции на действие разнонаправленных стимулов в пробах (всех ∆RR), увеличивается время достижения реакций (tAB) и восстановления после действия стимулов в пробах (tr). Симптомы имеют достаточную диагностическую чувствительность, в 2 раза превышающую клинические и ЭКГ-симптомы ИБС.
2. Найден Ркг-признак ишемических эпизодов в виде участков стабилизации ВСР во время стенокардии 1-3 ФК с разницей продолжительности RR-интервалов в пределах 3,55±1,02 мс. При вазоспастической стенокардии на Ркг перед эпизодом стабилизации в большинстве случаев усиливается симпатическая периодика.
3. Исследование волновой структуры сердечного ритма при гипертонической болезни результировало не только диагностическую информативность РКГ при определении стадии этого фактора риска, но и определенные удобства и высокую чувствительность анализа ВСР, важные в случаях клинически не манифестированных, а также возможности оценки влияния антигипертензивных лекарств при выборе персонализированной терапии.
4. При изучении ВСР у пациентов с острым инфарктом миокарда оказалось, что существуют дифференцированные изменения ВСР при некрозе передней или задней стенки левого желудочка, при субэндокардиальном и субэпикардиальном остром коронарном синдроме. При ретроспективном анализе ВСР умерших и оставшихся в живых пациентов наименьшие значения автономной регуляции в единицах миллисекунд в виде автономной кардионейропатии обнаружены у умерших, что достоверно свидетельствует об обратной умеренной корреляции (r=0,412) между снижением ВСР и степенью риска летального исхода.
5. Изучение ВСР с помощью РКГ высокого разрешения доказало возможность использования метода для периоперационной оценки актуального кардиоваскулярного статуса на каждом этапе проведения интервенционного вмешательства. Динамика выраженности волновой структуры ВСР по амплитуде волн и соотношению регулирующих факторов соответствовала патофизиологии каждого этапа операции от интубационного наркоза, остановки сердца и перехода на искусственное кровообращение до запуска сердца и восстановления его сократительной деятельности. Кардиоаритмии во время операции были связаны с локализацией хирургических манипуляций.
6. Исследование анализа ВСР при аритмиях сердца позволило выявить возможности РКГ, не реализуемые другими инструментальными методами: оценку аритмогенного автономного фона, гемодинамическую значимость каждого эпизода аритмии. На Ркг в удобной для наблюдения форме регистрируются все известные кардиоаритмии, а также зависимость их частоты от вегетативной регуляции СУ, что предполагает еще и возможности персонализированной терапии.
Рецензенты:
Шапошник И.И., д.м.н., профессор, заведующий кафедрой пропедевтики, ГБОУ ВПО «Южно-Уральский государственный медицинский университет» Министерства здравоохранения Российской Федерации, г. Челябинск;
Эфрос Л.А., д.м.н., профессор кафедры госпитальной терапии, ГБОУ ВПО «Южно-Уральский государственный медицинский университет» Министерства здравоохранения Российской Федерации, г. Челябинск.
Библиографическая ссылка
Миронова Т.Ф., Миронов В.А., Шамуров Ю.С. КЛИНИЧЕСКИЕ ВОЗМОЖНОСТИ РИТМОКАРДИОГРАФИИ ВЫСОКОГО РАЗРЕШЕНИЯ ПРИ АНАЛИЗЕ ВАРИАБЕЛЬНОСТИ СЕРДЕЧНОГО РИТМА У БОЛЬНЫХ ИШЕМИЧЕСКОЙ БОЛЕЗНЬЮ СЕРДЦА (ИННОВАЦИОННЫЙ ОПЫТ) // Современные проблемы науки и образования. 2015. № 2-1. ;URL: https://science-education.ru/ru/article/view?id=19258 (дата обращения: 01.07.2025).



