Проблема лечения вентральных грыж до сих пор привлекает внимание хирургов всего мира. Это можно объяснить большой распространенностью данной патологии. Так, грыжи передней стенки живота встречаются у 6-7% мужчин и у 2,5% женщин всего мира. Внедрение принципа пластики грыжевых ворот без натяжения тканей с использованием эндопротезов позволило упростить оперативную технику герниопластики, уменьшить операционную травму, а также улучшить отдаленные результаты (снизить частоту рецидивов с 10-30% до 0,1-1% [4]. Применение имплантатов привело к возникновению новой клинической проблемы – увеличению количества случаев инфекционных осложнений [7; 10]. При использовании протеза количество осложнений со стороны раны, таких как нагноение, серома, гематома, отторжение протеза, может достигать, по разным источникам, от 18,6 до 67% [3-5; 8]. Послеоперационные осложнения являются основной причиной продолжительного течения послеоперационного периода и значительного увеличения материальных затрат на лечение.
В доступной литературе встречаются разрозненные и единичные данные об использовании в герниопластике эндопротезов с серебряным покрытием, но нет данных о применении этих эндопротезов в инфицированной условиях, о морфологических изменениях элементов тканей, окружающих имплантированный эндопротез [4].
Таким образом, несистематизированное и разнонаправленное количество данных по проблеме использования эндопротезов с антибактериальным покрытием при обычной и инфицированной герниопластике и определило цель нашего экспериментального исследования.
Цель исследования. Изучить особенности реакции соединительной ткани передней брюшной стенки в раннем послеоперационном периоде при использовании опытных образцов сетчатых эндопротезов с антибактериальным покрытием.
Материалы и методы. Эксперименты in vivo выполнены на 30 белых крысах-самцах линии Wistar массой 180,0±20,00 г. Для проведения исследования нами были взяты экспериментальные образцы двух эндопротезов, состоящих из ПВДФ-нитей и пролипропилена, с нанесенным на них антибактериальным покрытием из серебра, предоставленных нам ООО «Линтекс» г. Санкт-Петербург.
Для исследования отбирали животных без внешних признаков заболевания, прошедших карантин в условиях вивария КГМУ. Животные были разделены на 2 экспериментальные группы по 15 крыс в каждой. Оперативные вмешательства выполняли в вечернее время суток в течение 2 недель. Во всех 3 сериях опытов под эфирным наркозом в стерильных условиях оперблока всем животным проводили разрез по средней линии живота в верхней трети длиной 4 см; рассекали кожу и подкожную клетчатку. Тупо выделяли участок апоневроза прямых мышц живота размером 4х4 см. К этому участку мононитью 2/0 фиксировали сетчатый эндопротез размером 2×2 см, моделируя надапоневротическую пластику. Эндопротез фиксировали узловыми швами по всей его площади. После этого в послеоперационную рану вводили 0,1 мл физиологического раствора, содержащего 1 млрд взвеси микробных тел суточной культуры Staphylococcus aureus 592 и Е. coli. Послеоперационную рану ушивали. Выведение животных из эксперимента проводили на 7, 14, и 21-е сутки путем передозировки средств для наркоза. После выведения животных из эксперимента забирали фрагмент брюшной стенки вместе с эндопротезом из центральной части имплантата размером 1x1 см. Далее изъятый материал фиксировали в 10%-ном растворе нейтрального формалина в течение 10 суток, затем образцы тканей обезвоживали и заливали в парафин по стандартной методике. С парафиновых блоков изготавливали срезы толщиной 5-7 мкм и окрашивали их гематоксилином и эозином, методом Ван-Гизона, PAS-реакция + альциановый синий с докраской ядер гематоксилином.
После юстировки оптической системы микроскопа Leica-CME с помощью окулярной фотонасадки DCM-510 были сфотографированы интересующие участки препаратов при ×40 и ×100-кратных увеличениях. Для определения преобладания воспалительных или репаративных тенденций производили подсчет качественного состава клеточных инфильтратов возле нитей эндопротезов и между ними. Выраженность воспалительной реакции оценивалась путем определения площади инфильтрата вокруг нитей эндопротеза.
Далее подсчет клеток производился в стандартном поле зрения в непосредственной близости к нити эндопротеза в расположенном рядом с нитью клеточном инфильтрате на увеличении х400. Расчет процентного состава производился на 100 клеток. Считали клетки резиденты (фиброциты, фибробласты и макрофаги) и нерезиденты (лимфоциты, нейтрофилы, эозинофилы и моноциты). С целью подтверждения статистической значимости расхождений средних величин в 2 сериях эксперимента нами в соответствии со стандартами ИСО 3534-3-99, а также ГОСТ Р 50779.10-2000 (ИСО 3534-1-93) после определения типа распределения данных был выбран метод оценки достоверности отличий Вилкоксона-Манна-Уитни. Все вычисления выполнялись с помощью аналитического пакета приложения Excel Office 2010.
Полученные результаты и их обсуждение
При изучении микропрепаратов с использованием эндопротезов двух образцов на 7-е сутки эксперимента было выявлено, что волокнистая соединительная ткань дермы резко отечна, кровеносные сосуды полнокровны. Нити окружены воспалительным инфильтратом, в котором преобладают сегменто- и палочкоядерные нейтрофилы, макрофаги и лимфоциты. Степень выраженности выявленных изменений больше в препаратах с использованием полипропиленового эндопротеза (рис. 1).
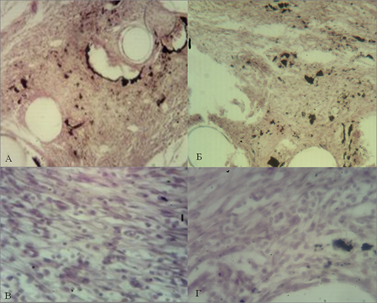
Рис. 1. Микрофотография области имплантации эндопротеза из ПВДФ-нитей (А), (В) и полипропилена (Б), (Г) на 7-е сутки эксперимента. Ув. х40 - А и Б, ув. х100 - В и Г. Окр. Г+Э.
На 14-е сутки эксперимента в препаратах с использованием ПВДФ-эндопротеза вокруг нитей имплантата сформирована хорошо выраженная двухслойная соединительнотканная капсула. Круглоклеточная инфильтрация частично сохранялась только в участках, расположенных между пучками нитей эндопротеза. Капсула хорошо васкуляризована. При использовании полипропиленового эндопротеза продолжала сохраняться отечность и лейкоцитарно-макрофагальная инфильтрация. Соединительнотканная капсула образована коллагеновыми волокнами, которые собраны в пучки, богата клеточными элементами, среди которых преобладают фибробласты и единичные гранулоциты, четкой границы между наружными и внутренними слоями капсулы нет (рис. 2).
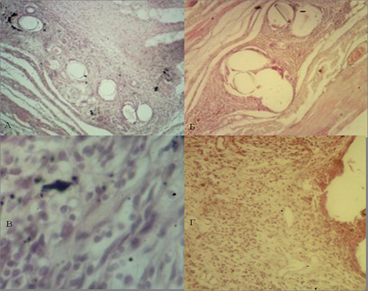
Рис. 2. Микрофотография области имплантации эндопротеза из ПВДФ-нитей (А), (В) и полипропилена (Б), (Г) на 14-е сутки эксперимента. Ув. х40 - А и Б, ув. х100 - В и Г. Окр. Г+Э.
На 21-е сутки в препаратах с использованием эндопротеза из ПВДФ-нитей среди клеток фибробластического ряда наблюдалось прорастание всех ячеек сетки эндопротеза волокнистой соединительной тканью с признаками организации волокон в пучки. На поверхности нитей сплошным слоем располагались фибробласты. При использовании полипропиленового эндопротеза продолжали сохраняться единичные очаги воспалительных изменений вокруг нитей эндопротеза. В окружающей соединительной ткани дермы в поле зрения встречалось большое количество гигантских клеток инородных тел. Вокруг нитей эндопротеза отмечается формирование хорошо выраженной соединительнотканной капсулы, от которой происходило врастание молодых соединительнотканных волокон в ячейки эндопротеза (рис. 3).
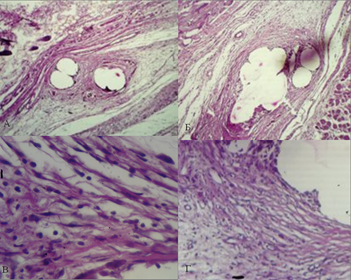
Рис. 3. Микрофотография области имплантации эндопротеза из ПВДФ-нитей (А), (В) и полипропилена (Б), (Г) на 21-е сутки эксперимента. Ув. х80 - А и Б, ув. х 400 - В и Г. Окр. Г+Э.
При определении площади инфильтрата нами были получены следующие результаты (таблица 1).
Таблица 1 - Динамика изменения площади воспалительно-клеточного инфильтрата, M±m, кв. мм
|
Образец Сутки |
7 |
14 |
21 |
|
Полипропиленовый |
1,23±0,021 |
0,94±0,042 |
0,84±0,02 |
|
ПВДФ-нити |
1,24±0,013 |
1,17±0,034,5 |
0,65±0,026 |
Примечание: различия клеточных индексов достоверны (p<0,05) 1 – по отношению к полипропиленовому эндопротезу на 14-е сутки, 2 – по отношению к полипропиленовому эндопротезу на 21-е сутки, 3 – по отношению к ПВДФ-эндопротезу на 14-е сутки,4 – по отношению к ПВДФ-эндопротезу на 21-е сутки, 5 - по отношению к полипропиленовому эндопротезу на 14-е сутки, 6 - по отношению к полипропиленовому эндопротезу на 21-е сутки.
Как видно из таблицы 1, динамика морфологических изменений вокруг нитей полипропиленового и ПВДФ-эндопротезов была сходной. Происходит снижение площади инфильтрата на 21-е сутки на 36,3 и 54,8% соответственно по отношению к начальным срокам эксперимента. Несмотря на то что у ПВДФ-эндопротеза на 7-е сутки имеется большая выраженность воспалительной реакции, в итоге на 21-е сутки площадь инфильтрации оказывается ниже по сравнению с полипропиленовым эндопротезом.
Аналогичную картину течения репаративного процесса подтверждают показатели подсчета клеточных элементов в воспалительном инфильтрате вокруг нитей эндопротеза (рис. 4).
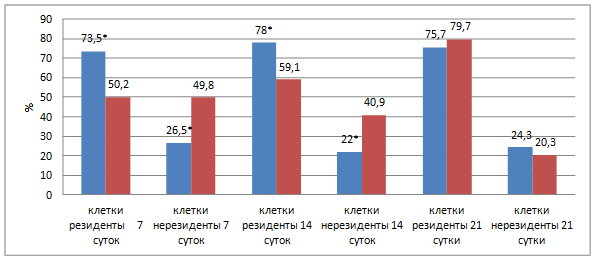
Рис. 4. Динамика изменения клеточного состава воспалительно-клеточного инфильтрата.
Примечание: *- различия значений клеточного состава достоверны (p<0,05) по отношению к группе с использованием полипропиленового эндопротеза.
На данной диаграмме представлена динамика изменения клеточного состава ткани вокруг нитей эндопротезов с антибактериальным покрытием из серебра на основе полипропилена и ПВДФ-нитей. На всех сроках эксперимента отмечалось увеличение количества клеток резидентов. Максимальное количество нерезидентных клеток выявлено на 7-е сутки с использованием полипропиленового имплантата (49,8%), в то время как с использованием ПВДФ-имплантата в 1,8 раза меньше - 26,5%. С использованием ПВДФ-эндопротеза максимальное количество резидентных клеток наблюдалось уже на 14-е сутки (78%), а с использованием полипропиленового эндопротеза максимальное значение было достигнуто только к 21-м суткам (79,7%). Численность нерезидентных клеток на 14-е сутки составляла 40,9 и 22% соответственно. На 21-е сутки при использовании полипропиленового эндопротеза количество клеток-нерезидентов снизилось почти в 2 раза и составило 20,3%, а при использовании ПВДФ-эндопротеза уменьшилось на 2,2% и составило 24,3%.
Выводы. Таким образом, при использовании сетчатого ПВДФ-эндопротеза с антибактериальным покрытием регенеративные процессы протекают более активно по сравнению с сетчатым полипропиленовым эндопротезом с антибактериальным покрытием.
Степень выраженности воспалительных изменений вокруг нитей эндопротезов обратно пропорциональна срокам эксперимента и наименее выражена в препаратах с использованием сетчатого ПВДФ-эндопротеза с антибактериальным покрытием.
Следовательно, наилучшей биосовместимостью и антибактериальными свойствами обладает имплантат с антибактериальным покрытием из серебра на основе ПВДФ-нитей.
Рецензенты:
Бежин А.И., д.м.н., профессор, заведующий кафедрой оперативной хирургии и топографической анатомии им. профессора А.Д. Мясникова, ГБОУ ВПО «КГМУ» Минздрава России, г. Курск;
Липатов В.А., д.м.н., профессор кафедры гистологии, эмбриологии, цитологии, доцент, ГБОУ ВПО «КГМУ» Минздрава России, г. Курск.
Библиографическая ссылка
Мишина Е.С., Затолокина М.А., Нетяга А.А., Климова Л.Г., Жуковский В.А. РЕАКТИВНЫЕ ИЗМЕНЕНИЯ СОЕДИНИТЕЛЬНОЙ ТКАНИ ПЕРЕДНЕЙ БРЮШНОЙ СТЕНКИ В РАННЕМ ПОСЛЕОПЕРАЦИОННОМ ПЕРИОДЕ ПРИ ИСПОЛЬЗОВАНИИ ОПЫТНЫХ ОБРАЗЦОВ СЕТЧАТЫХ ЭНДОПРОТЕЗОВ С АНТИБАКТЕРИАЛЬНЫМ ПОКРЫТИЕМ // Современные проблемы науки и образования. 2015. № 2-1. ;URL: https://science-education.ru/ru/article/view?id=18056 (дата обращения: 18.12.2025).



