Сердечно – сосудистые заболевания широко распространены и являются основной причиной смертности среди взрослого населения. Метаболический синдром, который представляет собой комплекс основных факторов риска сосудистых катастроф, достигает до 25-35% по частоте встречаемости в общей популяции. В основе метаболического синдрома (МС) лежит тканевая инсулинорезистентность (ИР), способствующая развитию гиперинсулинемии, активации симпатоадреналовой системы, повышению сосудистого тонуса и патологического сдвига в липидном спектре крови [4] На сегодняшний день имеются данные, позволяющие рассматривать нарушение структуры и функции эндотелия, в качестве важного компонента МС [7]. Выстилая сосудистое русло изнутри, эндотелиальные клетки представляют собой первичную мишень для воздействия гемодинамических, биохимических и иммунных факторов циркулирующей крови. Однако эндотелий выполняет не только барьерную функцию, но и является гормонально-активной тканью, вырабатывающей большое количество биологически активных веществ. Эндотелиальная дисфункция является системным патологическим нарушением, которое проявляется ослаблением эндотелий-зависимой вазодиляции и ремоделировании сосудов, что является ранним проявлением патологических процессов в сердечно-сосудистой системе [6]. Нарушение состояния эндотелия сосудов в клинических условиях можно диагностировать по биохимическим и функциональным маркерам. К биохимическим маркерам поврежденного эндотелия относятся изменение концентрации в крови большого количества биологически активных веществ, синтезируемых эндотелием и экспрессируемых на его поверхности, к ним относят: фактор фон Виллебранда, эндотелин-1, молекулы адгезии (Е-селектин, Р-селектин), тканевый активатор плазминогена, тромбомодулин, фибронектин [5].
Одним из признанных биомаркеров дисфункции эндотелия является васкулоэндотелиальный фактор роста (ВЭФ), который принимает участие в формировании атеросклероза, гипертонической болезни, сахарного диабета 2 типа. Экспрессия этого цитокина возрастает при гипоксии, обеспечивая регенерацию эпителия и образование новых сосудов [7].
К значимым и доказанным предиктором смертности от сердечно-сосудистых заболеваний относят микроальбуминурию (МАУ). Микроальбуминурия связана с нарушением капиллярной стенки клубочка с транскапиллярной потерей альбумина и это позволяет расценивать наличие МАУ как четкий маркер развития системной эндотелиальной дисфункции [3].
Однако большее значение для клинициста имеет значение не статические признаки дисфункции эндотелия, которые фиксируют биомаркеры, а возможность динамически оценить степень нарушения эндотелий-зависимую вазодилатацию сосудов. Микрососуды кожи являются удобным и доступным объектом для изучения, в том числе могут быть использованы для исследования функции эндотелия. Для регистрации кожного кровотока наиболее широко используются оптические методы, такие как фотоплетизмография и лазерная допплеровская флоуметрия (ЛДФ) а также термометрия высокого разрешения [6]. Спектральный анализ позволяет оценивать состояние сосудистого тонуса и реакцию его на внешние воздействия. В качестве простых, доступных функциональных проб для оценки состояния кожного кровотока традиционно используются холодовая и тепловая пробы.
На сегодняшний день отсутствует единый диагностический критерий дисфункции эндотелия, это позволило нам применить новый метод, основанный на измерении амплитуд кожной температуры с использованием вейвлет-анализа колебаний. Цель нашего исследования состояла в установлении взаимосвязи между доказанными биомаркерами дисфункции эндотелия и индексами вазоконстрикции и индексами востановления, полученными при проведении непрямой холодовой пробы у пациентов с МС.
Материалы и методы
В исследование были включены 24 пациента с МС в возрасте от 35 до 52 лет. Диагноз МС устанавливали в соответствии с критериями ВНОК (2009): абдоминальное ожирение - объем талии ≥94 см у мужчин, ≥80 см у женщин в сочетании с любыми 2 из следующих критериев - повышение триглицеридов (ТГ) ≥1,7 ммоль/л; снижение липопротеидов высокой плотности (ЛПВП) у женщин <1,3 ммоль/л, у мужчин- <1,03 ммоль/л; АД ≥135/85 мм рт. ст.; повышение уровня глюкозы плазмы ≥5,6 ммоль/л.
В исследование не включали пациентов с вторичными формами артериальной гипертензии (АГ), СД, ИБС, сердечной недостаточностью 3-4 функционального класса по классификации Нью-Йоркской ассоциации сердца, воспалительными заболеваниями миокарда, системными заболеваниями соединительной ткани, онкологическими заболеваниями, получающих статины и антигипертензивнае препараты. Индекс массы тела (ИМТ) рассчитывали по формуле Кетле: масса тела (кг)/рост (м²).
В качестве группы сравнения исследованы 14 практически здоровых лиц в возрасте 48,2±2,4 лет.
Всем было проведено общеклиническое и лабораторное обследование. Уровни липидов, глюкозы плазмы крови, креатинина, мочевой кислоты, трансаминаз, билирубина определяли стандартными биохимическими методоми. Уровень инсулина определяли методом ИФА «ELISA Monobind Inc» Германия, индекс инсулинрезистентности (ИР) определяли по формуле HOMA-IR. Концентрацию ВЭФ в сыворотке крови определяли методом иммуноферментного анализа (ИФА) с использованием соответствующих наборов реагентов ЗАО «Вектор-Бест» (Новосибирск) фотометра «Stat-Fax» («Awareness Technology Inc.», США), микроальбумин в моче определяли методом ИФА с использованием реагентов «ORGENTEC» (Германия). СКФ рассчитывали по формуле CKD-EPI мл/мин/1,73 кв.м
Для оценки реакции микрососудистого тонуса использовался метод вейвлет-анализа колебаний кожной температуры при охлаждении конечности [10]. Во время проведения контралатеральной холодовой пробы пациент находился в положении лежа на спине, температура в помещении при проведении измерений составляла 22,5±0,50С. Регистрировалась температура тыльной поверхности дистальной фаланги указательного пальца правой кисти прибором «Микротест» (Пермь, Россия, РУ Росздравнадзора № ФСР 2012/14175), обеспечивающим разрешение по температуре 0,0010С.. В процессе проведения холодовой пробы кисть левой руки погружалась в ванночку с водно-ледовой смесью (температура 00С) на 3 минуты. Измерение температуры проводилось непрерывно: в течение 10 минут до пробы, во время холодовой пробы (3 минуты) и в течение 10 минут после проведения пробы.
Частотно-временной анализ колебаний температуры проводился с использованием вейвлет-анализа [17]. Для реконструкции колебаний в эндотелиальном (0,02-0,0095 Гц) и нейрогенном (0,05-0,02 Гц) частотном диапазонах [2] применяли обратное вейвлет-преобразование. Предлагаемый метод обратного вейвлет-преобразования, это способ обработки экспериментальных сигналов (в нашем случае температурных колебаний), позволяющий выделить колебания в определенной области спектра. При этом в амплитудах колебаний содержится та же информация, что и в спектральной характеристике.
Для оценки вклада различных механизмов регуляции сосудистого тонуса была выбрана величина среднеквадратичных амплитуд колебаний кожной температуры <ΔT> в соответствующем частотном диапазоне. Кроме того, в каждом частотном диапазоне оценивались относительные изменения среднеквадратичных амплитуд колебаний: k = (STi-ST1)/ST1, где ST1 среднеквадратичные амплитуды колебаний до холодовой пробы, STi среднеквадратичные амплитуды колебаний для соответствующих временных интервалов (во время пробы, в течение 3 и 10 минут после пробы). Полученные показатели мы обозначили как индекс вазоконстрикции и индексы восстановления.
За индекс вазоконстрикции (ИВК) принято значение k= (ST2-ST1)/ ST1, где ST1 – показатель исходного состояния, ST2- показатель во время холодового воздействия.
За индекс постхолодового восстановления (ИПВ) принято значение k= (ST4-ST1)/ ST1, где ST1 – показатель исходного состояния, ST4 – значение через 10 мин после холодового теста.
За индекс раннего постхолодового восстановления (ИРВ) принято значение k= (ST3-ST1)/ ST1, где ST1 – показатель исходного состояния, ST3 - первые 3 мин после окончания холодового воздействия.
Данные представлены в виде M±SD, где M - среднеарифметическое значение по подргуппе; SD - погрешность измерения, рассчитанная по формуле Стьюдента. Достоверность отличий выборок определялась с использованием критерия Вилкоксона.
Результаты и обсуждение
Представительство различных проявлений МС было следующим. АГ была выявлена у всех пациентов, со средней длительностью 4,57±2,58 года. Отягощенная наследственность по сердечно-сосудистым заболеваниям (ССЗ) также была у всех пациентов. Дислипидемия с гипертриглицеридемией присутствовала у 90 %, гипо ХСЛПВП в 2%, а гипергликемия (без диагноза сахарного диабета) у 65 % пациентов.
У пациентов с МС по сравнению с группой практически здоровых лиц были выявлены повышенный уровень холестерина (ХС), триглицеридов (ТГ), липопротеидов низкой плотности (ЛПНП), глюкозы, мочевой кислоты (табл. 1). Также в группе МС ожидаемо присутствовала гиперинсулинемия и инсулинрезистентность. Кроме того, была установлена прямая достоверная корреляции между величиной окружности талии (ОТ) и уровнем мочевой кислоты (r=0,5; р=0,04), и уровнем ДАД (r=0,43; р=0,03). Инсулинрезистентность (HOMA-IR) сопровождалась повышением ХС (r=0,6; р=0,04), и мочевой кислоты (r=0,6; р=0,02).
Таблица 1
Показатели больных с метаболическим синдромом в сравнении с группой практически здоровых лиц (М ± SD)
|
Параметры (единицы) |
МС (n=24) |
Здоровые (n=14) |
р |
|
Возраст (годы) |
49,1±1,7 |
48,2±2,4 |
0,7 |
|
ОТ (см) |
110,4±11 |
80,7±11 |
0,0001 |
|
ИМТ (кг/м²) |
35,8 ±1,3 |
27±1,3 |
0,0001 |
|
САД (мм рт.ст.) |
147,2±8,1 |
128,3±7,2 |
0,0001 |
|
ДАД (мм рт.ст.) |
96,5±7,1 |
78,5±5,3 |
0,0001 |
|
глюкоза (ммоль/л) |
5,8±0,8 |
4,21±0,5 |
0,0001 |
|
ХС (ммоль/л) |
5,7±0,9 |
4±0,7 |
0,004 |
|
ЛПНП (ммоль/л) |
3,26±0,7 |
2,43±0,4 |
0,03 |
|
ЛПВП (ммоль/л) |
1,31±0,3 |
1,4±0,1 |
0,3 |
|
ТГ (ммоль/л) |
2,33±1,1 |
0,57±0,11 |
0,001 |
|
креатинин (мкмоль/л) |
75,8±12,5 |
66,0±10,1 |
0,2 |
|
мочевая кислота (ммоль/л) |
342,4±45,4 |
241,5±86,1 |
0,009 |
|
НвА1с (%) |
5,8±0,2 |
5,1±0,4 |
0,4 |
|
инсулин (мк ЕД/мл) |
19,8±8,6 |
6,7±1,2 |
0,001 |
|
HOMA-IR (ед.) |
5,2±2,3 |
1,25±0,7 |
0,01 |
|
СКФ ( мл/мин/1,73 кв.м ) |
88,5±5,8 |
112,7±7,6 |
0,001 |
р – достоверность отличий в сравниваемых группах
В группе МС было выявлено незначительное снижение СКФ, и отрицательная связь показателя с уровнем ДАД (r=-0,4 ; р=0,04). Уровень обоих маркеров ЭД - МАУ и ВЭФ - были значимо выше в группе МС (табл. 2). Была установлена положительная корреляция МАУ с уровнем ДАД (r=0,7 ; р=0,02) и отрицательная со значениями СКФ (r=-0.85 ; р=0,03).
Полученное изменения СКФ, в отсутствии заболеваний почек в анамнезе, и выявление четкой связи между показателями фильтрации, лабораторными проявлениями дисфункции эндотелия и уровня АД отражают начальные проявления нефропатии у больных МС. Полученная взаимосвязь МАУ с уровнем ВЭФ у данной категории больных свидетельствует о дисфункции эндотелия, а в сочетании со снижением СКФ можно рассматривать как раннее проявление почечного повреждения.
Таблица 2
Концентрация биомаркеров эндотелиальной дисфункции в группах
|
Показатель, единица измерения |
Значение медианы (25-75% перцентиль); [Min- и Max- величины показателя] |
||
|
МС (n = 24) |
контроль (n = 14) |
р |
|
|
ВЭФ, пг/мл |
91 (76 270); [0 441] |
75 (0 96); [0 129] |
0,04 |
|
Микроальбумин мкг/мл |
25,2±4,2 |
9,41±4,7 |
0,001 |
р – достоверность отличий в сравниваемых группах
Была установлена прямая высокой степени корреляция между уровнем ВЭФ и общим холестерином (r=0,74 ; р=0,02), креатинином (r=0,67 ; р=0,001), уровнем САД (r=0,6 ; р=0,02), МАУ (r=0,73 ; р=0,02) и отрицательная корреляция ВЭФ и СКФ (r=-0,7 ; р=0,02).
При проведении холодовой пробы у здоровых лиц амплитуда колебаний кожной температуры во время функциональной нагрузки в эндотелиальном, нейрогенном диапазонах частот достоверно снижалась более чем в 2 раза (табл. 3). После окончания холодового воздействия повышение температуры приводило к симметричному увеличению амплитуд колебаний и практически к их восстановлению до исходных значений в течение первых 3 минут
У пациентов с МС реакция на холодовую пробу значительно отличалась от здоровых лиц (табл. 3). В эндотелиальном диапазоне частот после достоверного снижения амплитуд колебаний кожной температуры их значения практически не нарастали, что свидетельствовало о длительной вазоконстрикции. В нейрогенном диапазоне амплитуды температур после холодового воздействия увеличивались, однако не достигали величины исходного уровня.
В таблице 4 представлены значения индексов реактивности микроциркуляции на холодовой прессорный тест.
Таблица 3
Средние амплитуды колебаний кожной температуры (*103, 0С ) при проведении холодового теста
|
Диапазон колебаний |
Группа |
исходно (1) |
во время пробы (2) |
через 3 мин (3) |
через 10 мин (4) |
|
Эндотелиальный |
Здоровые |
21,4±3,7
|
9,6±1,0 р1-2=0,000 |
20,1±3,7 р2-3=0,005 |
18,9±3,4 р2-4=0,019 |
|
Метаболический синдром |
24,1±3,3 |
13,2±2,1 р1-2=0,000 |
17,2±3,1 р1-3=0,033 |
14,2±2,2 р1-4=0,000 |
|
|
Нейрогенный |
Здоровые |
8,9±1,4 |
3,2±0,3 р1-2=0,001 |
7,0±1,3 р2-3=0,009 |
12,9±0,6 р2-4=0,006 |
|
Метаболический синдром |
8,3±1,3 |
6,5±2,1 р1-2=0,048 |
9,1±2,2 р2-3=0,004 |
6,4±1,1 |
Таблица 4
Значения индексов вазоконстрикции и постхолодового востановления в группах
|
Диапазон колебаний |
Группа |
ИВК (1) |
ИРВ (2) |
ИПВ (3) |
|
Эндотелиальный |
Здоровые |
-45,9±0,65 |
4,6±0,14 р1-2=0,0023 |
-7,4±0,13 р1-3=0,016 |
|
Метаболический синдром |
-39,3±0,07 |
-59,6±0,09
|
-39,4±0,06 |
|
|
Нейрогенный |
Здоровые |
-57,3±0,62 |
-14,6±0,12 р1-2=0,005 |
13,1±0,34 р1-3=0,004 |
|
Метаболический синдром |
-21,1±0,17 |
0,0039±0,17 р1-2=0,006 |
-0,08±0,13
|
Индекс вазоконстрикции (ИВК) со знаком «-» указывает на уменьшение амплитуды температурных осцилляций в сравнении с исходными значениями. Индексы раннего постхолодового восстановления (ИРВ) и постхолодового востановления (ИПВ) отражают увеличение амплитуды колебаний после окончания холодового воздействия, что соответствуют активности вазодиляторных механизмов.
Таким образом, можно говорить о том, что адекватная реакция эндотелия на холодовой стресс характеризуется значениями индексов вазоконстрикции в пределах от -40 до -60, и значениями индексов восстановления от -10 до +10.
Несмотря на то, что ИВК группе больных МС значимо меньше, чем у здоровых лиц, значения индексов постхолодого восстановления (ИРВ и ИПВ) остаются большим, поскольку увеличения амплитуд колебаний кожной температуры не происходит в силу нарушения вазодилятации. На рисунке схематично представлены значения описанных индексов у здоровых и больных МС.
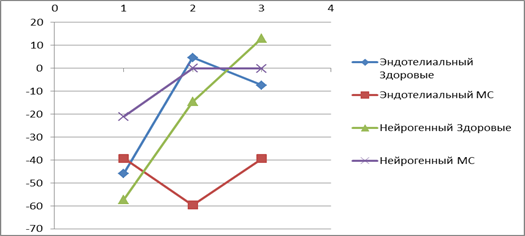
Рисунок. Индексы реактивности эндотелия у здоровых лиц и больных МС. Значения 1 – ИВК, 2- ИРВ, 3-ИПВ.
Холодовая проба приводит к мощной активации симпатической нервной системы, следствием чего является вазоконстрикция. У здоровых лиц вазоконстрикция на фоне холодовой пробы сопровождается уменьшением амплитуды колебаний кожной температуры и увеличением индекса вазоконстрикции. После окончания холодового воздействия начинается компенсаторная вазодиляции, которая сопровождается увеличением амплитуд колебаний кожной температуры до первоначальных значений в различных диапазонах частот, и следовательно снижается значение индекса постхолодовой восстановления. Таким образом, такую реакцию можно считать адекватной на прессорную пробу и расценивать как сохранение вазодилатационной функции эндотелиальных клеток.
У пациентов МС индекс постхолодовой вазодиляции в эндотелиальном диапазоне частот имеет высокие значения, а в нейрогенном значимо меньше, чем в группе сравнения, что отражает отсутствие восстановления амплитуд колебаний за счет нарушение вазодилаторных механизмов и может считаться признаком эндотелиальной дисфункции.
Наши данные подтверждают наличие взаимосвязи между показателями эндотелиальной дисфункции и метаболическими нарушениями при МС. Получена обратная корреляция между уровнем ХС ЛПВП и ИВК в эндотелиальном диапазоне частот (r=-0,73 ; р=0,001), т.е. чем ниже ХС ЛПВП, тем сильнее вазоконстрикция. Уровень инсулина коррелировал с ИВК в эндотелиальном (r=0,66 ; р=0,02), и нейрогенном диапазонах (r=0,64 ; р=0,01) частот.
На молекулярном уровне инсулин оказывает чрезвычайно сильное стимулирующее действие на экспрессию гена eNOS и на активность этого важного фермента для осуществления вазодилятации. При инсулинорезистентности действие инсулина через ФИ-3-киназу значительно угнетается, и в результате снижается влияние инсулина на активность eNOS и выработку NO. Было установлено, что в этих условиях инсулин утрачивает способность поддерживать стабильное состояние гладко-мышечных клеток (ГМК) и, наоборот, начинает стимулировать их миграцию и пролиферацию через неповрежденный МАП-киназный путь, т.е. действовать проатерогенно [9,5]. Таким образом, при МС подтверждается значимый вклад инсулинемии в развитии и поддержании эндотелиальной дисфункции, и в первую очередь, в усилении вазоконстрикторных влияний.
Связи между сывороточной концентрацией ВЭФ и изменениями амплитуд колебаний сосудистого тонуса не было получено. Однако, значимое увеличение уровня ВЭФ и МАУ у пациентов МС, а также полученные положительные корреляции уровней МАУ и ВЭФ с АД, могут косвенно свидетельствовать о связи увеличения значений биомаркеров вазоконстрикции с нарушением вазодилятирующей функции эндотелия, выявленным при термометрии.
Существует две точки зрения на причину эндотелиопатии при МС [5, 7]. С одной стороны утверждается, что дисфункция эндотелия вторична по отношению к имеющейся ИР, т.е. является следствием гипергликемии, артериальной гипертонии, дислипидемии. Влияние этих процессов на повреждение эндотелия достаточно изучено. При гипергликемии в эндотелиальных клетках активируется фермент протеинкиназа-С, который увеличивает проницаемость сосудистых клеток для белков и нарушает эндотелий-зависимую релаксацию сосудов. Кроме того, гипергликемия активирует процессы перекисного окисления, продукты которого угнетают сосудорасширяющую функцию эндотелия. При артериальной гипертонии повышенное механическое давление на стенки сосудов приводит к нарушению архитектоники эндотелиальных клеток, повышению их проницаемости для альбумина, усилению секреции сосудосуживающего эндотелина-1, ремоделированию стенок сосудов. Дислипидемия повышает экспрессию адгезивных молекул на поверхности эндотелиальных клеток, что дает начало формированию атеромы. Все перечисленные состояния, повышая проницаемость эндотелия, экспрессию адгезивных молекул, снижая эндотелий-зависимую релаксацию сосудов, способствуют прогрессированию атерогенеза и сосудистых катастроф.
С другой стороны можно считать, что дисфункция эндотелия является не следствием, а причиной развития ИР и, соответственно, связанных с ней состояний (гипергликемии, гипертонии, дислипидемии). Действительно, для того чтобы соединиться со своими рецепторами, инсулин должен пересечь эндотелий и попасть в межклеточное пространство. В случае первичного дефекта эндотелиальных клеток трансэндотелиальный транспорт инсулина нарушается и может развиться состояние ИР [5]. В таком случае ИР будет вторичной по отношению к эндотелиопатии. Нарушение секреторной (эндокринной) функции эндотелия, которое проявляется дисбалансом веществ, вырабатываемых им, ухудшает эндотелий-зависимое расслабление вследствие уменьшения синтеза NО при сохраненной или увеличенной продукции вазоконстрикторов, что ведет к изменению цитоархитектоники сосудов [1]
Пациенты с МС имели значимые отличия от здоровых лиц по всем метаболическим показателям. Полученные результаты дают основание полагать, что в данной категории пациентов повреждающими агентами в отношении эндотелия являются АГ, гипеурикемия, дислипидемия, гипергликемия, гиперинсулинемия. Кроме того, группа МС характеризовалась повышением ВЭФ, что определенно указывало на наличии дисфункции эндотелия. Нарушения вазодилации, выявленные при функциональной холодовой пробе у пациентов с МС, подтвердили взаимосвязь между аномальной сосудистой реактивностью и маркерами эндотелиальной дисфункции.
Таким образом, наши данные свидетельствуют о том, что при МС имеется дисбаланс между факторами, обеспечивающими в норме оптимальное течение всех эндотелийзависимых процессов, который может быть выявлен методом кожной термометрии с использованием вейвлет-анализа амплитуд колебаний.
Выводы:
1. Нормальный уровень ВЭФ и МАУ, биомаркеров эндотелиальной дисфункции, сопровождается адекватной реакцией эндотелия на холодовой стресс. У здоровых лиц амплитуда колебаний кожной температуры во время функциональной нагрузки в эндотелиальном, нейрогенном диапазонах частот достоверно снижается. После окончания холодового воздействия амплитуда колебаний увеличивается и в течение 3 минут восстанавливается до исходных значений.
2. Адекватная реакция тонуса сосудов на холодовой стресс характеризуется значениями индекса вазоконстрикции в пределах от -40 до -60, и значениями индексов восстановления от -10 до +10.
3. У пациентов МС дисфункция эндотелия проявляется повышением уровня ВЭФ и МАУ, значения которых коррелируют с уровнем АД, мочевой кислоты и липидов крови. Снижение СКФ сопряжено с увеличением уровней МАУ и ВЭФ, что можно рассматривать как подтверждение раннего почечного повреждения при МС.
4. У пациентов с МС при холодовой пробе после достоверного снижения амплитуд колебаний отсутствует их увеличение в эндотелиальном диапазоне частот и отсутствует окончательное восстановление в нейрогенном диапазоне, что объясняется нарушением процессов вазодилатации. Индекс вазоконстрикции в эндотелиальном и нейрогенном диапазонах частот связан с уровнем инсулинемии.
5. Результаты, полученные методом кожной термометрии с использованием вейвлет-анализа амплитуд колебаний температур, коррелируют с основными факторами, характеризующими дисбаланс эндотелий-зависимой регуляции тонуса сосудов и может использоваться для диагностики эндотелиальной дисфункции
Работа выполнена при поддержке ГРАНТа РНФ № 14-15-00809.
Рецензенты:Желобов В.Г., д.м.н., профессор кафедры госпитальной терапии ГБОУ ВПО Пермский государственный медицинский университет им. академика Е.А.Вагнера) Минздрава России, г. Пермь;
3aвражных Л.А., д.м.н., главный врач ЗАО «Курорт Усть-Качка», г. Пермь.
Библиографическая ссылка
Смирнова Е.Н., Лоран Е.А., Шулькина С.Г., Подтаев С.Ю. ИССЛЕДОВАНИЕ ФУНКЦИИ ЭНДОТЕЛИЯ С ПОМОЩЬЮ ХОЛОДОВОЙ ПРОБЫ У ПАЦИЕНТОВ С МЕТАБОЛИЧЕСКИМ СИНДРОМОМ // Современные проблемы науки и образования. – 2014. – № 6. ;URL: https://science-education.ru/ru/article/view?id=16248 (дата обращения: 02.05.2024).



