Введение
Бактериоцины - это антибактериальные вещества белковой природы, вырабатываемые бактериями и подавляющие жизнедеятельность других штаммов того же вида или родственных видов. Способностью к синтезу бактериоцинов обладают как грамположительные, так и грамотрицательные бактерии. Большинство бактериоцинов, продуцируемых грамотрицательными бактериями, имеют сравнительно узкий спектр действия, по сравнению с антибиотиками, и являются активными против штаммов того же или филогенетически родственных видов. Однако, бактериоцины грамположительных бактерий, особенно молочнокислых бактерий, обладают широким спектром антимикробного действия. Бактериоцины, продуцируемые культурой L. plantarum, получили название плантарицины. Это низкомолекулярные (с Mr<10 кДа) катионные термостабильные пептиды, сохраняющие свою активность в широком диапазоне значений рН от 3 до 9. Основным механизмом антимикробного действия плантарицинов является нарушение целостности цитоплазматической мембраны путём порообразования, что ведёт к нерегулируемому выходу из клетки ионов калия, аминокислот, и других низкомолекулярных веществ и, следовательно, к гибели клетки-мишени [2, 3].
Исследователи рассматривают бактериоцины в качестве потенциальных антимикробных лекарственных веществ и консервантов, подавляющих рост и развитие патогенных и условно патогенных бактерий и дрожжевых грибов. Известно, что антибиотики оказывают многочисленные побочные действия, негативно сказывающиеся на нашем организме, в то же время бактериоцины и продуцирующие их штаммы, посредством избирательного воздействия на микрофлору, нормализуют микробный ценоз при некоторых патологиях у человека и животных. Таким образом, проблема поиска и изучения свойств новых антимикробных бактериальных пептидов, перспективных для последующего создания медицинских препаратов, а также для использования в различных отраслях промышленности, является актуальной [1].
Данные по секвенированию ДНК промышленного пробиотического штамма L. plantarum 8PA-3 показали наличие локуса, предположительно, отвечающего за синтез двух бактериоцинов - плантарицинов EF и NC8, что послужило основой для выбора этой культуры для выделения и исследования бактериоциноподобных пептидов [4].
Цель работы
Провести хромато-масс-спектрометрический анализ фракций пептидов с молекулярной массой до 10 кДа, обладающих антимикробной активностью, выделенных из культуры L. plantarum 8PA-3, и провести сравнительный анализ с известными бактериоциноподобными пептидами. Для выполнения поставленной цели данного исследования были сформулированы следующие задачи: осуществить подбор штамма лактобактерий, проявляющих наивысшую антагонистическую активность в отношении большинства тест-культур, выделить и охарактеризовать фракции низкомолекулярных пептидов и белков, обладающих антимикробной активностью.
Научно-исследовательская работа выполнялась в рамках гранта НИР СПбГУ Ф-№0.37.123.2011 "Морфофизиологические и биохимические аспекты антимикробного воздействия бактериоцинов" в лаборатории внутриклеточной регуляции кафедры биохимии биолого-почвенного факультета СПбГУ и совместно с сотрудниками лаборатории электронной микроскопии и спектроскопии в ФГУП «Гос.НИИ ОЧБ» ФМБА России. Руководитель гранта - профессор, д.б.н. Рыбальченко О.В.
Материалы и методы
Для выделения и характеристики фракций низкомолекулярных пептидов, обладающих антимикробной активностью, был отобран штамм лактобактерий L. plantarum 8PA-3, проявляющий наивысшую антагонистическую активность в отношении большинства тест-культур. Культура была любезно предоставлена сотрудниками лаборатории электронной микроскопии и спектроскопии в ФГУП «Гос.НИИ ОЧБ» ФМБА России.
Пептиды экстрагировали из культуры препаративными методами, такими как кислотная экстракция раствором 5% уксусной кислоты и ультрафильтрация через фильтры из регенерированной целлюлозы c диаметром пор 10 кДа и 1 кДа.
Группу низкомолекулярных пептидов фракционировали с помощью хроматографических методов - катионообменная хроматография и обращенно-фазовая высокоэффективная жидкостная хроматография на колонке Discovery HS C18 на хроматографе ÄKTAexplorer 10S.
Спектр катионных пептидов и чистоту полученных препаратов оценивали электрофоретическими подходами в кислых по методу С. Панима (1969) и денатурирующих по методу Х. Шеггера (1987) условиях.
Для определения антимикробной активности выделенных фракций были использованы бактериологические методы: метод радиальной диффузии белков и пептидов в агарозном геле, предложенный Р. Лерером (1991), и метод overlay (наложение геля), описанный Е. Портером (1997).
Определение молекулярной массы полученных проб проводили хромато-масс-спектрометрический анализ на приборе LC/MS Agilent Tehnologies (LC-1260, MS-6538 UHD Accurate-Mass Q-TOF).
Результаты
Антимикробную активность проб, полученных после кислотной экстракции и ультрафильтрации, определяли против грамотрицательной бактерии E. сoli, грамположительных бактерий L. monocytogenes и St. epidermidis, низшего гриба C. albicans. Наиболее выраженную активность показали пробы, содержащие белки из концентрата супернатанта молекулярной массой от 1-10 кДа. Полученные пептиды обладали антимикробной активностью как в отношении грамположительных и грамотрицательных бактерий, так и против низших грибов, что показало их широкий спектр действия. В то же время, клеточный экстракт имел низкую антимикробную активность. Это, вероятно, можно объяснить теорией синтеза бактериоцинов, как неактивных форм - пребактериоцинов, и последующей их экскреции в среду в виде активных форм.
Фракционирование низкомолекулярных пептидов из концентрата супернатанта после ультрафильтрации с молекулярной массой 1-10 кДа осуществляли методом катионообменной хроматографии на колонке СМ-сефадекс G-25 (А: 1% уксусная кислота в воде, В: 3 М NaCl; градиент В до 1 М, скорость потока 1 мл/мин). Детекцию вели при длинах волн 240 нм, 260 нм и 280 нм (см. рис. 1).
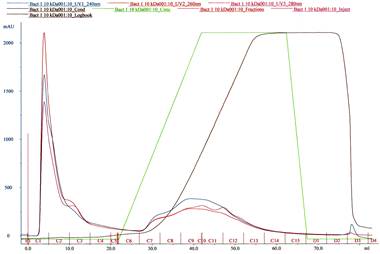
Рис. 1. Профиль элюции пробы из концентрата супернатанта с молекулярной массой 1-10 кДа на колонке СМ-сефадекс G-25. Детекцию вели при длинах волн 240 нм (синий график), 260 нм (красный график) и 280 нм (розовый график).
Для дальнейшего фракционирования группы низкомолекулярных катионных полипептидов (фракции С9, С11, С12) и обессоливания использовали метод ОФ ВЭЖХ. Наличие большого количества компонентов питательной среды для лактобактерий не позволило получить приемлимые результаты (см. рис. 2).
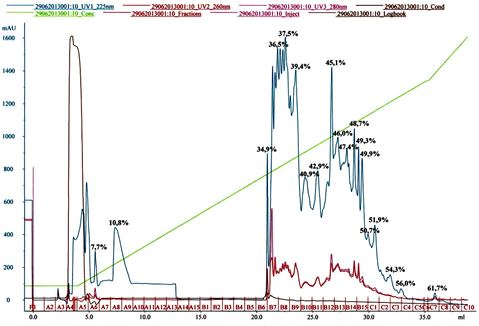
Рис. 2. Профиль элюции пробы С11 на колонке Discovery HS C18 4,6х250 мм, 5 мкм, 300 Å (Supelco, США) (А: 0.1% ТФУ в воде, В: ацетонитрил, градиент от 0% до 60% за 30 мин, скорость потока 2 мл/мин). Цифрами на графике отмечена концентрация ацетонитрила. Детекцию вели при длинах волн 225 нм (синий график), 260 нм (красный график) и 280 нм (розовый график).
Для определения антимикробной активности фракций использовали метод радиальной диффузии в геле. Антимикробная активность определялась против грамотрицательной бактерии E. сoli, грамположительных бактерий L. monocytogenes и St. epidermidis, низшего гриба C. albicans. Наибольшую активность показала проба В9, которую взяли для последующего анализа (см. рис. 2).
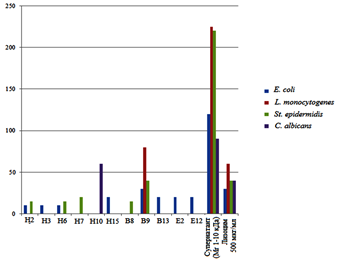
Рис. 3. Результаты антимикробного теста по методу радиальной диффузии в геле пробы после ОФ ВЭЖХ.
Хромато-масс-спектрометрический анализ фракции В9 был проведён в ресурсном центре СПбГУ «Развитие молекулярных и клеточных технологий». Анализ производили на приборе LC/MS Agilent Tehnologies (LC-1260, MS-6538 UHD Accurate-Mass Q-TOF), использовали колонку ZORBAX SB-C18, 5 мкм х 150 х 0.5 мм, скорость потока 20 мкл/мин. Разделение проводили в градиенте ацетонитрила от 0 до 50% за 25 минут (см. рис. 4). Детекцию вели при длине волны 280 нм. В процессе хромато-масс-спектрометрического анализа полученной фракции антимикробных пептидов с молекулярной массой до 10 кДа было показано наличие множества однозаряженных компонентов белковой низкомолекулярной матрицы (масса/заряд 300-750), входящей в состав питательной среды MRS, а также присутствие относительно высокомолекулярных пептидов с молекулярной массой: 2089,1 Да; 2112,9 Да; 2293,3 Да; 4845,8 Да.
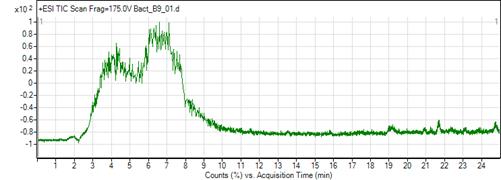
Рис. 4. TIC (total ion current) хроматограммы в режиме MS пробы В9.
Заключение
В результате проведённой научно-исследовательской работы и полученных данных можно сделать вывод, что штамм L. plantarum 8PA-3 является продуцентом антимикробных пептидов широкого спектра действия, обладающих электрофоретической подвижностью, сходной с таковой лизоцима, и относительно малыми молекулярными массами. Отсутствие в активных фракциях пептидов с молекулярными массами, сходными с массами предсказанных по базе данных бактериоцинов (плантарицинов E, F, NC8α и NC8β) [5], может быть объяснено их модификацией или частичной деградацией в процессе выделения. Описанный выше способ выделения бактериоциноподобных пептидов достаточно трудоемок и требуют больших затрат времени, что должно (и может) быть оптимизировано. Результатом оптимизации времени эксперимента может стать меньшая деградация предсказанных бактериоцинов и, как следствие, их прямое определение.
Рецензенты:
Гудков С.В., д.б.н., в.н.с., Федеральное государственное бюджетное учреждение науки Институт теоретической и экспериментальной биофизики РАН (ИТЭБ РАН), г.Пущино.
Белова Н.А., д.б.н., в.н.с., Федеральное государственное бюджетное учреждение науки Институт теоретической и экспериментальной биофизики РАН (ИТЭБ РАН), г.Пущино.
Библиографическая ссылка
Соболева А.В., Колобов А.А., Гришина Т.В. ХРОМАТО-МАСС-СПЕКТРОМЕТРИЧЕСКИЙ АНАЛИЗ АНТИМИКРОБНЫХ ПЕПТИДОВ ИЗ КУЛЬТУРЫ LACTOBACILLUS PLANTARUM 8РА-3 // Современные проблемы науки и образования. 2014. № 3. ;URL: https://science-education.ru/ru/article/view?id=13561 (дата обращения: 06.07.2025).



