В условиях постоянно усиливающейся антропогенной нагрузки актуально проведение мероприятий, направленных на профилактику экологически обусловленных заболеваний органов дыхания, к которым относятся аллергический ринит и бронхиальная астма. Проведенный нами анализ заболеваемости детей болезнями органов дыхания позволил выявить преобладание аллергической патологии в ряде городов Оренбургской области, в которых зарегистрирован наибольший уровень загрязнения воздушной среды.
Ранее, рядом авторов было установлено, что среди детей с астматическим бронхитом и бронхиальной астмой высок уровень резидентных стафилококковых бактерионосителей [5].
Таким образом, актуальной является санация резидентных стафилококковых бактерионосителей как превентивная мера в возникновении экологически обусловленных заболеваний верхних дыхательных путей. Для санации целесообразно использование лекарственного препарата, который, с одной стороны, стимулировал бы местный иммунитет и естественную колонизационную резистентность слизистых оболочек макроорганизма, а с другой - снижал персистентные свойства патогена, в частности, его антикарнозиновую активность (АКрА), являющуюся маркером персистенции [6], поскольку подавление персистирующих свойств возбудителя затрудняет его паразитирование внутри клеток и тем самым повышает эффективность лекарственных воздействий [2]. В качестве такого препарата нами был выбран иммуномодулятор циклоферон, который, как было показано ранее, снижает АКрА микроорганизмов [4].
Кроме того, известно, что микроорганизмы образуют в организме хозяина высокоорганизованные сообщества, которые позволяют им выживать в любых неблагоприятных условиях, - биопленки [5], поэтому представляло интерес определить влияние циклоферона на способность стафилококков к биопленкобразованию.
Цель работы
Определение длительности эффективной санации резидентных стафилококковых бактерионосителей с помощью циклоферона по его способности модулировать антикарнозиновую активность и биопленкообразование золотистых стафилококков.
Материалы и методы
Выделение клонов S. aureus осуществляли путем рассева суточной бульонной культуры на плотную питательную среду с последующим определением АКрА (О. В. Бухарин и соавт., 1999) и способности формировать биопленки (G.O'Toole, 2000). Соинкубирование стафилококков с терапевтическими концентрациями циклоферона (ООО «НТФФ «Полисан», г. Санкт-Петербург) проводили по Д. А. Кириллову (2004) в течение 7 дней, параллельно определяли способность микроорганизмов к инактивации карнозина и биопленкообразованию, положительным результатом считали значения более 1,1. Статистическую обработку результатов проводили с использованием критерия Стъюдента [1].
Результаты и обсуждение
Популяционная структура исходной культуры S. aureus по АКрА была представлена клонами с разной выраженностью признака: 67 % обладали высокой АКрА (2,0-3,0 мг/мл), по 16,5 % - средней активностью (1,0-2,0 мг/мл) и нулевой. Среднепопуляционный уровень АКрА составлял 2,03±0,26 мг/мл (рис. 1).
Рис. 1
Изменение популяционной структуры S. aureus по АКрА под влиянием циклоферона
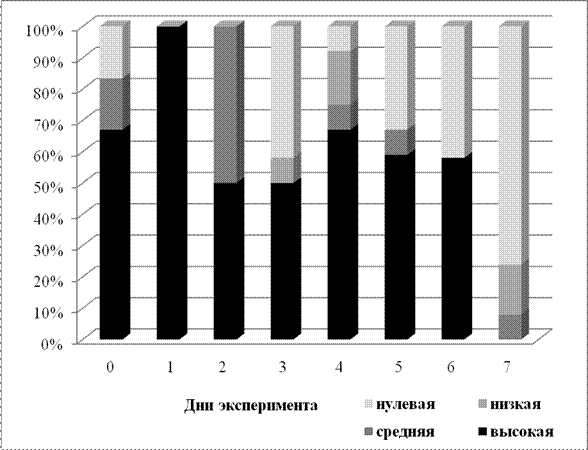
Под действием циклоферона после первого соинкубирования доля клонов S.aureus с высокой АКрА составила 100 %, после второго - 50 % с высокой и 50 % со средней АКрА. Среднепопуляционный уровень признака был равен 2,62±0,16 мг/мл и 2,05±0,94 мг/мл соответственно. На третий день выделялось 50 % клонов с высокой АКрА, появились клоны с низкой (1,1-1,8 мг/мл) и нулевой активностью (8 % и 42 % соответственно), а средний уровень продукции ингибиторов карнозина снизился до 1,44±0,26 мг/мл. Далее возросло число клонов с высокой (67 %) и низкой (17 %) АКрА, а также до 8 % уменьшилось количество клонов с нулевой активностью и появилось 8 % со средней, что сопровождалось повышением среднепопуляционного значения антикарнозивой активности до 2,2±0,26 мг/мл. После пятого соинкубирования, наряду с клонами, обладающими высокой АКрА (59 %), появилась доля клонов со средней способностью к инактивации карнозина (8 %), а уровень клонов, не обладающих признаком, увеличился до 33 %; далее было зарегистрировано такое же количество клонов с высокой АКрА (58 %) и 42 % клонов без признака. Средний уровень АКрА в популяции составил 1,75±0,26 мг/мл и 1,7±0,26 мг/мл соответственно. На седьмой день эксперимента отмечено нарастание доли клонов без АКрА (76 %), 8 % составляли клоны со средним и 16 % с низким уровнем активности, а среднее значение антикарнозиновой активности в популяции снизилось до 0,195±0,12 мг/мл.
Таким образом, установлено, что в течение семи дней эксперимента наблюдалась перестройка популяционной структуры в сторону клонов, не обладающих антикарнозиновой активностью. Кроме того, наименьшая среднепопуляционная способность золотистых стафилококков к инактивации карнозина была отмечена также на седьмой день соинкубирования с циклофероном.
Одновременно нами проведено изучение влияния циклоферона на способность золотистых стафилококков образовывать биопленки (рис. 2). Исходную популяцию штамма стафилококка составляли 80 % клонов со средней способностью биопленкообразования (от 1,9 до 2,5) и 20 % - с высокой (2,6 и более), среднее значение способности популяции образовывать биопленки было равно 2,44±0,04.
Рис. 2
Изменение популяционной структуры S. aureus по способности формировать биопленки под влиянием циклоферона

Соинкубация стафилококков с циклофероном приводила как к снижению доли клонов со средним показателем до 40 % и появлению 60 % клонов с низкой способностью (1,1-1,8) формировать биопленки, так и к снижению среднепопуляционного показателя биопленкообразования (1,69±0,07). При дальнейшей соинкубации доля клонов со средними значениями увеличилась до 53 % и появились клоны с высокими значениями (47 %), средняя способность популяции формировать биопленки составила 2,26±0,12. После третьего дня выделялись клоны с низким (73 %) и нулевым (7 %) биопленкообразованием, до 20 % уменьшилось число клонов со средними значениями, и до 1,5±0,09 снизился средний уровень биопленкообразования. После четвертого дня 93 % клонов характеризовались низкими значениями признака, 7 % - средними (средняя способность биопленкообразования популяции - 1,4±0,05), затем вновь появились клоны с нулевой способностью (7 %), наряду с клонами со средними (7 %) и низкими (86 %) значениями (средняя способность - 1,48±0,06).
На шестой и седьмой дни эксперимента соотношение клонов было примерно одинаковым - около 80 % клонов обладали низкой способностью биопленкообразования и около 20 % клонов - нулевой, а средний уровень биопленкообразования в популяции составил 1,31±0,07 и 1,26±0,05 соответственно.
Полученные результаты показали, что в течение семи дней эксперимента наблюдалась перестройка популяционной структуры в сторону клонов с низкой и нулевой способностью к биопленкообразованию. Кроме того, на шестой и седьмой дни соинкубации стафилококков с циклофероном были отмечены наименьшие среднепопуляционные значения биопленкообразования.
Таким образом, при изучении влияния циклоферона на биологические свойства клонов золотистого стафилококка установлена перестройка популяционной структуры носительского штамма по биопленкообразованию и способности к инактивации карнозина. В ходе эксперимента изменялось соотношение клонов с низкими, средними и высокими значениями и появлялись клоны с нулевыми. Наибольшее число клонов, не обладающих способностью к инактивации карнозина, отмечено на седьмой день соинкубирования, а наименьший уровень биопленкообразования (80 % клонов с низкой способностью и 20 % - с нулевой) зарегистрирован на шестой и седьмой дни эксперимента. Аналогичная тенденция наблюдалась при сравнении средних показателей в популяции. Таким образом, полученные результаты позволили установить оптимальную продолжительность санации стафилококковых бактерионосителей циклофероном, которая составляет семь дней.
На следующем этапе работы нами по трехкратному бактериологическому обследованию была сформирована группа из 40 резидентных стафилококковых бактерионосителей в возрасте 9-12 лет. Они были просанированы циклофероном в течение 7 дней. После первой санации были получены следующие результаты: S.aureus выделялся в 80 % случаев, КОС - в 20 % случаев. После второй отмечено появление у бактерионосителей золотистых стафилококков, наряду с S.aureus, коагулазоотрицательных штаммов в 9,5 % случаев, золотистый стафилококк продолжал высеваться в 76,2 % случаев, только КОС высевали у 14,3 % детей. Третья санация способствовала снижению выделения золотистых стафилококков, стафилококковые бактерионосители составили 66,6 %, коагулазоотрицательные стафилококки высевали в 14,3 % случаев, совместное выделение золотистых и коагулазоотрицательных стафилококков отмечено в 23,8 % случаев. Четвертая, пятая и шестая санации способствовали уменьшению числа бактерионосителей золотистых стафилококков до 47,1 %, 43,5 %, 40,1 % соответственно и одновременно увеличению числа коагулазоотрицательных стафилококков до 23,5 %, 26,1 %, 27,3 %. Увеличилось также число бактерионосителей, у которых, наряду с золотистыми, стали выделяться и коагулазоотрицательные стафилококки (29,4 %, 30,4 %, 31,8 %). Далее мы изучили динамику антикарнозиновой активности золотистых стафилококков в процессе санации циклофероном. Было установлено, что после первой санации циклоферон оказывал разнонаправленное действие на S.aureus: повышал признак у 50 % выделенных штаммов, снижал - у 33,3 % и не оказывал влияния на 16,6 % выделенных от бактерионосителей микроорганизмов. После второй санации способность к инактивации карнозина также повышалась у 50 % выделенных штаммов, снижалась у 43,8 %, не изменялась у 6,3 % выделенных стафилококков; после третьей - у 42,8 %, 50 % и 7,1 % соответственно. После четвертой санации уменьшилось число штаммов, повышающих АКрА, до 14,3 % и до 71,4 % увеличилось число золотистых стафилококков, не способных инактивировать карнозин, АКрА не изменялась у 14,3 % выделенных культур. После пятой и шестой санаций снижение признака зарегистрировано у 80,0 % и 77,7 % штаммов; повышение и индифферентное действие у - 10 % и 11,1 % штаммов золотистых стафилококков соответственно. После седьмой и восьмой санаций выявлены штаммы, в основном ингибирующие АКрА (в 90,9 % случаев) и в 9,1 % повышающие данный признак. Далее мы провели изучение видового состава и антикарнозиновой активности у выделенных штаммов микроорганизмов через месяц после санации. Были получены следующие данные: в 38,1 % случаев выделялся золотистый стафилококк, в 38,1 % - эпидермальный и в 23,1 % - одновременно золотистый и эпидермальный стафилококк или микрококк. Вместе с тем отмечено снижение антикарнозиновой активности у 80 % выделенных штаммов S.aureus по сравнению с исходным уровнем признака (до санации) и у 20 % культур способность к инактивации карнозина не изменилась. Среднее значение признака составило 0,4 мг/мл.
Таким образом, проведенные in vitro и in vivo исследования показали возможность санации резидентных бактерионосителей циклофероном. Установленные режимы санации способствуют не только элиминации золотистых стафилококков со слизистой оболочки переднего отдела носа, но и ингибируют его способность к инактивации карнозина. Циклоферон в качестве препарата для санации стафилококковых бактерионосителей может применяться для профилактики экологически обусловленных заболеваний, в частности, аллергических ринитов и бронхиальной астмы.
Рецензенты:
Гриценко Виктор Александрович, д.м.н., профессор, зав. лабораторией клеточного симбиоза Федерального государственного бюджетного учреждения науки Института клеточного и внутриклеточного симбиоза Уральского отделения Российской Академии наук (ИКВС УрО РАН), г. Оренбург.
Чайникова Ирина Николаевна, д.м.н., профессор кафедры микробиологии, вирусологии и иммунологии Государственного образовательного учреждения высшего профессионального образования «Оренбургская государственная медицинская академия Федерального агентства по здравоохранению и социальному развитию» (ГОУ ВПО ОрГМА), г. Оренбург.



