Актуальность. Современная хирургическая вертебрология немыслима без применения динамических и ригидных фиксирующих устройств, позволяющих восстановить утраченную стабильность позвоночных сегментов вследствие травмы, воспаления или при прогрессировании дегенеративно-дистрофических процессов в его различных элементах. Имплантируемые фиксаторы позволяют протезировать утраченные функции двигательных сегментов, но, вместе с тем, достаточно часто возникают проблемы, обусловленные нарушениями в биосовместимости, остеоинтеграции и диссонансом модулей упругости имплантатов с костной, хрящевой тканями позвоночных сегментов. В клинической практике при имплантации в межостистые, межтеловые промежутки динамических или ригидных фиксирующих конструкций в 4,6–85,0 % [6] случаев наблюдается развитие нестабильности фиксатора с возобновлением болевого вертебрального и радикулярного синдромов и необходимостью выполнения реопераций.
Именно поэтому одной из актуальных проблем в вертебральной имплантологии является разработка технологий, исключающих избыточную компрессию костной и хрящевой ткани в зонах контактов имплантируемых фиксаторов с сохранением микроциркуляции в зонах контакта. В настоящее время клиницистами во время оперативных вмешательств не определяются допустимые нагрузки на костную ткань фиксаторами, в связи с чем достаточно часто развивается нестабильность имплантируемой конструкции с последующей необходимостью её перемонтажа. Логично предположить, что при имплантации фиксирующих устройств в межостистые промежутки при лечении пациентов с дегенеративно-дистрофическими заболеваниями с развитием нестабильности компрессия элементами имплантируемой конструкции всех питающих ветвей остистого отростка может привести к развитию ишемии, гипоксии с изменением минерального обмена, к снижению модуля упругости, структурных и функциональных свойств костной ткани с развитием резорбции в зонах фиксации конструкции и нестабильности конструкции в целом.
Таким образом, для исключения нарушений микроциркуляции в костной ткани, снижения степени интраоперационного повреждения ее, возникает необходимость в мониторинге сатурации, как интегрального показателя в костных структурах, контактируемых с фиксаторами, ретракторами и в защите костной ткани, повышении её устойчивости к повреждающим факторам.
Цель исследования: создание технологии имплантации межостистых фиксаторов у пациентов с болевым вертебральным и корешковым синдромами вследствие нестабильности поясничных сегментов с применением объективных методик диагностики нарушения васкуляризации в костной ткани под контролем локальной и системной сатурации.
Материал и методы исследования
Оксиметрические исследования ткани остистых отростков в контактных зонах с имплантатами (межостистыми динамическими и ригидными фиксаторами) проведены у 25 пациентов (средний возраст 37±2,7 лет, 11 мужчин, 14 женщин) при операциях стабилизации поясничных сегментов межостистыми фиксаторами динамического и ригидного типов (патент РФ на полезную модель №128481, патент на промышленный образец №87386). В группу сравнения включены 37 пациентов, средний возраст – 35,5+3,2 лет, с имплантированными межостистыми фиксаторами без интраоперационного оксиметрического и динамометрического контроля. Все пациенты оперированы по поводу выраженного болевого корешкового и вертебрального синдромов, вследствие прогрессирующего дегенеративно-дистрофического процесса в люмбальных сегментах позвоночного столба с развитием диско-радикулярных конфликтов и нестабильности сегментов. Непосредственными показаниями к оперативному вмешательству являлись радикулярный и вертебральный болевые синдромы, резистентные к медикаментозной и физиотерапии в течение 4–6 недель.
Для оценки локального насыщения кислородом остистых отростков применялся комплекс «ЛАКК-М» [4] (рис. 1), который обеспечивал одновременные измерения перфузии ткани кровью, сатурации гемоглобина кислородом (SO2) и объём фракции гемоглобина (Vr) в зондируемой области. Одномоментно, для исключения ошибки влияния изменений системной сатурации на локальную, в отростках сравнивали показатели локальной сатурации с изменениями системной сатурации по показателям тканевого церебрального оксиметра FOR-SIHT (М2000,USA) [1,2,5] (график 1). Компрессионные нагрузки при фиксации протезирующего динамического устройства контролировались динамометрическим ключом с цифровой индикацией момента силы при закреплении межостистого фиксатора (рис. 2).

Рис. 1. Схема регистрации сатурации в остистом отростке при имплантации динамического фиксатора. 1 – ЛДФ (лазерный доплеровский флуометр); 2 – световод; 3 – межостистый фиксатор; 4 – динамометрический ключ
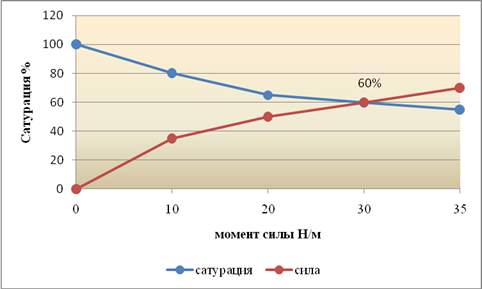
График 1. Динамика сатурации ткани отростка от момента силы ключа
Оценка SO2 и Vr производилась по методологии абсорбционной спектроскопии на основе разных оптических свойств оксигенированных и дезоксигенированных фракций гемоглобина. Глубина оптического зондирования не менее 1, 0 мм, что отражало уровень насыщения кислородом плотной и части губчатой ткани остистых отростков. Записи проводили, устанавливая датчик световода на боковые поверхности остистых отростков и его верхушку с оценкой насыщения кислородом в 3–5 зонах. Для анализа выделялись фрагменты записей длительностью 300 сек. Перед анализом ЛДФ-грамм проводили их выравнивание параллельно изолинии для устранения погрешностей при анализе колебательного процесса.


Рис. 2. Фиксации протезирующего динамического устройства контролировались динамометрическим ключом с цифровой индикацией момента силы при закреплении межостистого фиксатора
Именно потому, что параметр SO2 является интегральным показателем, соотнесенным с общим объёмом биоткани (средним арифметическим для артериальной и венозной крови), и поскольку в микроциркуляторном русле содержится артериальной крови с высоким содержанием О2 в несколько раз меньше, чем в венозной, поэтому данный факт позволял оценить потребление кислорода тканями.
Достоверное снижение SO2 (р≤0,05) в костной ткани при имплантации межостистого фиксатора подтверждало гипотезу о том, что при избыточной компрессии остистого отростка имплантатом происходило изменение газообмена, снижение потребления тканью кислорода, что служило развитием ишемии костной ткани с последующими изменениями минерального обмена, процессов остеоинтеграции с развитием резорбции и нестабильности конструкции.
Результаты и их обсуждение
Одной из основных задач, решаемых при данном исследовании, являлось установление параметров компрессионной нагрузки с применением цифрового динамометрического устройства на боковые поверхности остистых отростков, их верхушки, при которых оксиметрические показатели соответствовали базовым (до имплантации) и не приводили к критическим снижениям кислорода на измеряемых зонах контакта фиксатора и остистого отростка при контролируемом усилии.
По данным Г.А. Илизарова, А.М. Мархашова [3], кровоснабжение остистых отростков осуществляется ветвями сегментарных артерий от 2–3 порядка, идущих по боковым поверхностям остистых отростков, разветвляющихся на 8–10 ветвей, реже на 4–6, диметрами от 0,5 мм до 2,0 мм. Анастомозы в области верхушек остистых отростков присутствуют, но крайне редко. При измерении насыщения кислородом структур остистых отростков до имплантации фиксаторов оксиметрические значения соответствовали 78,1±3,7 %.
Шаг градации компрессии фиксирующих элементов фиксатора на боковые поверхности отростков составил 5 Н/м. Динамика изменения насыщения кислородом костной ткани отражена на графике № 1. Критическим снижением кислорода в измеряемых зонах надкостницы межостистых отростков мы условно считали значения менее 60 % (при показателях системной оксигенации 88,1±3,7 %). При избыточной компрессионной нагрузке, более 30 Н/м, фиксирующими элементами имплантата на костную ткань остистых отростков оксиметрические показатели неуклонно снижались, что указывало на необходимость ограничения компрессии на костную ткань до 25-27Н. При оксиметрических показателях 65–70 % с ткани отростков в течение 13–15 минут наблюдали стабильные значения показателей кислорода, что и служило основанием для окончательного закрепления межостистого фиксатора при максимальном моменте силы от 25 до 27 Н/м
Клинические и параклинические результаты импланатации межостистых фиксаторов с применением оксиметрического контроля.
Оценку функции и положения межостистых фиксаторов, имплантируемых с контролем сатурации в костной ткани остистых отростков, осуществляли в 12 и 24 месяца с применением клинических (ВАШ) и параклинических критериев (КТ, прицельные и функциональные рентгенограммы). Проводился клинический опрос пациентов с оценкой данных визуально-аналоговой шкалы (ВАШ) и сравнением с дооперационными данными ВАШ. Интегральные результаты оценки снижения болевого синдрома у пациентов основной группы оценены на «отлично», в связи с тем, что дельта ВАШ в 100 % случаев превышала 5,7 ступеней (р 0,05), в то время как в группе сравнения дельта ВАШ не превышала 4 баллов.
При выполнении функциональных рентгенограмм в 23 (92 %) случаях пациентов основной группы функция имплантируемых фиксаторов сохранена, положение их в межостистых промежутках правильное. В 2 (8 %) случаях функция фиксаторов не определялась, их положение было «ригидным», но признаков смещения фиксаторов не наблюдалось. К сожалению, у 4(10,8 %) пациентов группы сравнения выявлены зоны резорбции костной ткани в зонах контакта с фиксатором и, естественно, нестабильное положение фиксатора. В 3 (8,1 %) случаях, в связи с выраженным болевым синдромом, пациенты оперированы повторно с имплантацией транспедикулярного фиксатора.
Данные компьютерной томографии, выполненной в 12 и 24 месяца у 20 пациентов, доказывали стабильное положение фиксаторов в межостистых промежутках без развития зон резорбции. В группе сравнения зоны резорбции подтверждены у 4 (10,8 %) пациентов.
Выводы:
1. При имплантации межостистых фиксаторов необходимо интраоперационно применять цифровые динамометрические устройства и контролировать оксиметрические показатели в зонах контакта имплантата с остистыми отростками.
2. Величина компрессии (момент силы) элементов фиксатора на костную ткань остистых отростков не должна превышать 25–27 Н/М. В противном случае вероятность развития нестабильности фиксатора и необходимости выполнения повторной операции составляет 4 %.



