До настоящего времени патогенез острого панкреатита остается одним из недостаточно изученных. Усилия патофизиологов и клиницистов направлены на углубленное исследование не только ключевых патогенетических механизмов этой тяжелой болезни, но и на установление их последовательности появления, что продиктовано особенностями воспаления и невозможностью трансформации имеющихся знаний по типовым патологическим процессам на эту патологию, в патогенезе которой превалируют аутолитические явления [3, 7, 9].
Немалозначимым направлением исследователей является и изучение поражения различных органов и систем, поскольку включение их в патофизиологический процесс не только вносит вклад в расстройства гомеостаза на организменном уровне и может нести в себе фатальные последствия, но и влияет на течение основного патологического процесса в органе поражения, определяя характер болезни и ее течение. В этом отношении заслуживают особого внимания изменения в сердечно-сосудистой системе, поскольку гемодинамические расстройства являются одними из ключевых в пато- и танатогенезе заболевания, а сама система достаточно уязвима к действию различных патологических агентов [4, 6].
Последнее десятилетие пристальное внимание уделяется морфо-функциональным нарушениям в кишечнике при неотложных заболеваниях органов брюшной полости, в том числе и при остром панкреатите [3]. Нарушение энтерогематического барьера как одного из патологических проявлений энтеральной недостаточности (ЭН) приводит к возникновению дополнительного источника эндотоксикоза, что замыкает порочный круг и обусловливает возникновение необратимых поражений различных органов и систем [5, 8].
Настоящая работа направлена на изучение при остром панкреатите в динамике некоторых патофизиологических процессов в миокарде и кишечнике и на основе этого разработку наиболее оптимальных схем патогенетической терапии по предупреждению развития (прогрессирования) кардиальных и энтеральных расстройств.
Цель работы. На модели острого панкреатита в динамике установить характер и выраженность патологических нарушений со стороны сердца и кишечника и влияние на них лазерного излучения и антиоксиданта-антигипоксанта ремаксола.
Материалы и методы исследования
В основу работы положены экспериментальные исследования на 24 взрослых беспородных половозрелых собаках обоего пола, массой от 5,7 до 14 кг, разделенных для решения поставленных задач на следующие группы.
Первая группа – контрольная (12 животных). При остром экспериментальном панкреатите исследовали функциональное состояние миокарда и кишечника, качественный и количественный состав липидов, выраженность эндогенной интоксикации по гидрофильному и гидрофобному компонентам.
Вторая группа – опытная (12 животных). В данной группе исследовались эффекты, возникающие при использовании комбинации ремаксола и низкоэнергетического гелий-неонового лазерного излучения.
Панкреатит моделировали по способу В.М. Буянова с соавт. (1989). Для воспроизведения острого очагового панкреонекроза пунктировали желчный пузырь, забирали желчь с последующим лигированием места пункции. Затем желчь вводили в паренхиму вертикальной части поджелудочной железы по 0,5 мл в 6 точек. Все экспериментальные исследования проводились в соответствии с этическими требованиями по работе с экспериментальными животными («Правила проведения работ с использованием экспериментальных животных» (Приказ МЗ СССР №755 от 12.08.1987 г.) и Федеральный закон о защите животных от жестокого обращения от 01.01.1997 г.), «Правилами лабораторной практики в Российской Федерации» (2004 г.), с положениями соответствующих нормативных документов Минздрава Российской Федерации, соблюдением требований этических и правовых норм под внутривенным наркозом с использованием тиопентал-натрия из расчета 0,04 г/кг массы животного. В контрольные сроки (1-е, 3-и, 5-е сутки) животным осуществляли забор крови, выполняли биопсию тканей миокарда и кишечника.
В послеоперационном периоде экспериментальным животным проводили дезинтоксикационную (внутривенное введение 5 % раствора глюкозы и 0,89 % раствора хлорида натрия из расчета 50 мл/кг массы животного) терапию.
В опытной группе животным в комплексную терапию включали лекарственное средство, обладающее антиоксидантным эффектом (ежедневно осуществлялись внутривенные вливания ремаксола из расчета 15 мг/кг массы тела животного) и низкоинтенсивное лазерное излучение (внутрисосудистое облучение крови гелий-неоновым лазером при мощности излучения на выходе световода 5 мВт и времени воздействия 15 мин – дозой 0,1 Дж/см2).
Методы исследования
Уровень эндотоксемии оценивали по содержанию молекул средней массы (МСМ) в сыворотке крови. Содержание молекул средней массы в сыворотке крови измеряли на спектрофотометре СФ-46 при длине волны 250 и 280 нм (Пикуза О.И., Шакирова Л.З., 1994).
Для характеристики физико-химических свойств альбумина определяли эффективную (ЭКА) и общую (ОКА) концентрацию альбумина в сыворотке крови. Резерв связывания альбумина (РСА) определяли по формуле РСА = ЭКА/ОКА. Индекс токсичности (ИТ) определяли по формуле: ИТ = ОКА/ЭКА – 1 (Грызунов Ю.А., Добрецов Г.Е., 1994).
Липиды из биоптатов миокарда и кишечника экстрагировали хлороформметаноловой смесью (Хиггинс Дж.А., 1990).
Хроматографическое разделение липидов (тонкослойная хроматография). Липиды фракционировали методом тонкослойной хроматографии на силикагелевых пластинах. Полярные фосфолипиды разделяли на пластинах фирмы Merk на стеклянной основе, нейтральные липиды фракционировали на силикагелевых пластинах для обращенно-фазной тонкослойной хроматографии (Хиггинс Дж. А., 1990; Vaskovsky V.E. etal., 1975).
Количественное определение липидов. Молекулярный анализ проводили на денситометре Model GS-670 (BIO-RAD, США) с соответствующим программным обеспечением (PhosphorAnalyst/PS Sowtware).
Определяли показатели гемостаза: время рекальцификации обычной плазмы по Bergerhof и Roka (1954), каолиновое время (КВ) свертывания плазмы по P.G.J. Hattersley (1966), протромбиновое время (ПВ) плазмы по A.J. Quick (1966), тромбиновое время (ТВ) по R.M. Biggs и R.G. Macfarlane (1962), эуглобулиновый метод определения фибринолитической активности крови по H. Kowarzyk, L. Buluck (1954).
Интраоперационно окислительно-восстановительный потенциал (ОВП) тканей кишечника и миокарда определяли на универсальном ионометре ЭВ-74 с платиновым электродом, а электродом сравнения служил хлорсеребряный электрод. Коэффициент диффузии кислорода (КДК) в тканях определяли на основе учета темпа падения диффузного тока восстановления по уравнению И.М. Эпштейна (Труфанов Л.А., 1991). Изменение гистогематической проницаемости регистрировалось по капиллярной фильтрации и потере белка (метод Лендиса) (Чернух А.М. и др., 1984).
Электрокардиография. Электрокардиограмму (ЭКГ) регистрировали в стандартных отведениях на электрокардиографе ЭК ЭТ-01-«Р-Д».
Макроскопия проводилась прижизненно при лапаротомии и релапаротомии.
Полученные цифровые данные обрабатывали методом вариационной статистики, с использованием критерия t Стьюдента. Вычисления производили на CPU 1600 MHz “IntelPentium-IV” с помощью пакета программ MicrosoftOfficeXP. Использован текстовый процессор MicrosoftWord 2000. Динамика показателей отражена на графиках, построенных с использованием программы электронных таблиц MicrosoftExcel 2000.
Результаты исследования и их обсуждение
Проведенные исследования показали адекватность выбранной модели, о чем свидетельствовали морфологические и лабораторные признаки заболевания. В поджелудочной железе возникали явления некроза тканей: в первые сутки в местах инъекций желчи; в последующие – очаговые явления панкреонекроза. В слизистой оболочке кишечника наблюдались выраженные морфологические изменения, представленные воспалительно-дегенеративными явлениями вплоть до язвенных дефектов.
Экспериментально установлено, что при очаговом панкреонекрозе развивается синдром ЭИ, что подтверждалось ростом уровня МСМ, снижением ОКА, ЭКА, РСА и увеличение ИТ плазмы крови в 2,5 раза по сравнению с нормой у животных контрольной группы.
Повреждение клеточных мембран является пусковым моментом ЭИ. С учетом того, что в организации биомембран ведущее значение имеют липиды, очевидна роль нарушения их метаболизма в инициировании и прогрессировании эндотоксикоза [1, 2]. Качественный и количественный состав липидов в тканях миокарда и кишечника при остром очаговом панкреонекрозе был подвержен существенным изменениям: наблюдалось снижение уровня суммарных фосфолипидов (СФЛ), моноацилглицерола (МАГ), холестерола (ХС) и увеличение уровня свободных жирных кислот (СЖК) и триацилглицеридов (ТАГ). В составе фосфолипидов зарегистрировано достоверное уменьшение фосфатидилхолина (ФХ), фосфатидилсерина (ФС), фосфатидилинозита (ФИ) и повышение фосфатидилэтаноламина (ФЭА) и лизофосфолипидов (ЛФЛ).
Важнейшим фактором прогрессирования острого панкреатита выступает нарушение микроциркуляции, транскапиллярного обмена и биоэнергетики тканей. Микроциркуляторные нарушения тесно связаны с патологией транскапиллярного обмена. При различных по этиологии эндотоксикозах наблюдаются изменения в виде повышения проницаемости сосудистой стенки с выходом жидкости и белка в интерстициальное пространство. С целью изучения микроциркуляции и трофики тканей организма при панкреатогенном эндотоксикозе исследовали транскапиллярный обмен и биоэнергетику cердца и кишечника в динамике острого экспериментального панкреатита (таблица).
При остром панкреатите регистрировались изменения микроциркуляции и трофики миокарда, что подтверждалось снижением ОВП на 24,3–31,6 % (р<0,05), нарушением диффузии кислорода, повышением проницаемости исследуемой ткани для белка и воды, а также кровенаполнения миокарда на 16,0–36,4 % (р<0,05). Следует отметить, что наиболее выраженные расстройства трофики ткани отмечались на третьи сутки развития острого панкреатита, когда диапазон изменений всех показателей максимален. На пятые сутки применения инфузионной терапии наблюдалась некоторая стабилизация показателей, что соответствует снижению выраженности эндотоксикоза и свидетельствует в пользу стихания воспалительного процесса. Подобная динамика отмечалась также при исследовании микроциркуляции и трофики кишечника.
Токсическое поражение миокарда при остром панкреатите сопровождалось также нарушением его электрофизиологической активности, наблюдаемым с первых суток заболевания, что проявлялось в виде уменьшения вольтажа зубцов, изменения процессов реполяризации (снижение сегмента ST на 1–2 мм), появления в некоторых случаях патологического зубца Q и комплекса QS как признака реактивного повреждения миокарда чаще всего передней и боковой стенок левого желудочка (I, aVL, II), укорочения интервалов, увеличения частоты сердечных сокращений, различных нарушений ритма сердца. При этом инфузионная терапия не ограничивала изменения электрофункциональных показателей сердца даже на конечном этапе наблюдения.
Одним из значимых патогенетических компонентов развития энтеральной недостаточности при панкреонекрозе являются дисмикроциркуляторные процессы, которые во многом зависят от гемостатических нарушений. Нами изучено состояние тканевой (кишечной стенки) коагуляционно-литической системы. В ходе эксперимента в динамике выявлены нарушения в тканевой системе гемостаза. Так, экстракт ткани кишечника при очаговом панкреонекрозе укорачивал время рекальцификации, каолиновое, протромбиновое и тромбиновое время на 34,5-42,9, 42,5-53,1, 17,5-37,8 и 30,3-48,2 % (р<0,05) соответственно. При очаговом панкреонекрозе нарушалась и фибринолитическая система тканей кишечной стенки. При этом время эуглобулинового фибринолиза удлинялось на 29,7–56,4 % (р<0,05).
На следующем этапе нами изучены эффекты влияния на функциональное состояние миокарда и кишечника при очаговом панкреонекрозе комбинированного применения лазерной и антиоксидантной терапии (на примере ремаксола).
Использование комбинированной терапии способствовало выраженному снижению содержания токсических продуктов в плазме крови – гидрофильных и гидрофобных маркеров ЭИ, что свидетельствовало об ограничении интоксикационного синдрома. Первые положительные результаты действия препарата проявлялись с первых суток терапии, но более значительно были выражены на третьи-пятые сутки эксперимента (рис. 1).
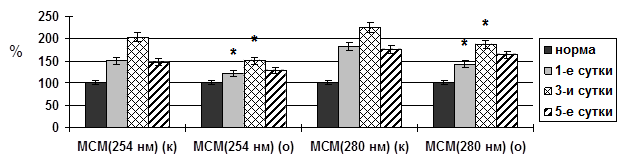
Рис. 1. Некоторые показатели эндогенной интоксикации при остром очаговом панкреонекрозе на фоне комбинированной терапии (* – достоверность отличия показателей по отношению к контролю при p<0,05; к – данные контрольной группы исследований; о – данные опытной группы исследований)
Динамика изменения липидного состава ткани миокарда при остром панкреатите на фоне комбинированной терапии характеризовалась следующими особенностями: содержание СЖК по сравнению с контролем снижалось на 21,1–31,5 % (р<0,05), ДАГ – на 16,3–33,9 % (р<0,05), МАГ – на 23,6–34,9 % (р<0,05), ХС – на 24,1–37,3 % (р<0,05); уровень СФЛ возрастал на 19,9–23,4 % (р<0,05). В составе фосфолипидов ткани миокарда наиболее значимая динамика отмечена в отношении ЛФЛ, содержание которых снижалось на 19,4–57,9 % (р<0,05) (рис. 2). Сходные изменения показателей липидного обмена отмечены нами также при исследовании тканей кишечника.
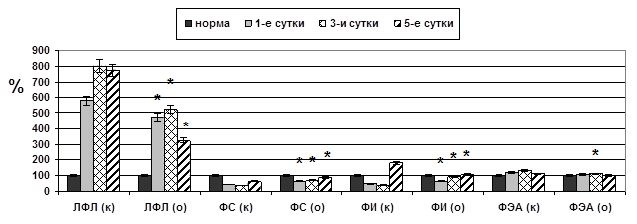
Рис. 2. Качественный состав липидов ткани миокарда при остром очаговом панкреонекрозе на фоне комбинированной терапии (* – достоверность отличия по отношению к контролю при p<0,05; к – контрольная группа; о – опытная группа)
Исследование микроциркуляции и трофики тканей на примере транскапиллярного обмена и биоэнергетики сердца и кишечника при остром панкреатите на фоне комбинированной терапии показало результаты, свидетельствующие о коррекции нарушений транскапиллярного обмена, диффузии кислорода и трофики сердца и кишечника с первых суток применения терапии (таблица).
Показатели транскапиллярного обмена и биоэнергетики сердца при остром очаговом панкреонекрозе на фоне комбинированной терапии (M±m)
|
Показатель |
Группа |
Исходные данные |
Этапы наблюдения (от момента моделирования) |
||
|
1-е сутки |
3-и сутки |
5-е сутки |
|||
|
Капиллярный фильтрат, мл |
I |
2,26±0,12 |
4,19±0,22* |
5,38±0,25* |
3,42±0,17* |
|
II |
3,75±0,20* |
4,42±0,22* |
2,89±0,13* |
||
|
Потеря белка, % |
I |
1,43±0,06 |
3,76±0,20* |
4,64±0,26* |
2,58±0,18* |
|
II |
3,19±0,15* |
3,86±0,21* |
2,11±0,11* |
||
|
Кровенаполнение, мкл/г |
I |
444,3±18,3 |
500,5±27,2 |
605,8±33,2* |
514,8±26,1* |
|
II |
485,2±22,5 |
524,1±28,9* |
470,1±22,1 |
||
|
КДК, см2/с х 10-3 |
I |
3,10±0,15 |
1,98±0,06* |
1,85±0,08* |
2,36±0,21* |
|
II |
2,54±0,10* |
2,71±0,09* |
2,89±0,12 |
||
|
ОВП, мВ |
I |
-31,90±1,65 |
-39,67±2,17* |
-41,98±2,37* |
-34,96±2,22 |
|
II |
-36,00±2,10 |
-36,51±2,23 |
-31,93±1,51 |
||
Примечание: I – контрольная группа, II – опытная группа; * – достоверность отличия по отношению к исходу при p<0,05, жирный шрифт – достоверность отличия по отношению к контролю при p<0,05.
Комбинированная терапия острого панкреатита способствовала уменьшению токсического поражения миокарда, что проявлялось в улучшении показателей биоэлектрической активности сердца, зарегистрированных по данным ЭКГ исследования.
Комбинация лазеро- и ремаксолотерапии при очаговом панкреонекрозе способствовала улучшению показателей гемостаза уже с первых суток применения. Экстракт ткани кишечника на фоне комбинированного лечения панкреонекроза укорачивал время рекальцификации, КВ, ТВ относительно исходных данных на 15,7–30,5, 33,1–40,8 и 14,7–27,3 % (p<0,05) соответственно. Относительно группы контроля значения данных показателей достоверно были выше на всех этапах исследования на 21,8–45,9, 20,6–41,9 и 26,3–54,5 % соответственно. ПВ на фоне терапии лазером и ремаксолом укорачивалось относительно нормы на третьи сутки на 13,9 % (p<0,05), а относительно контроля было выше на третьи и пятые сутки эксперимента на 33,8 и 60,7 % (p<0,05) соответственно.
Время эуглобулинового фибринолиза при комбинированной терапии тотального панкреонекроза превышало норму лишь на третьи сутки исследования на 34,6 % (p<0,05), а относительно контроля данный показатель был достоверно ниже на всех этапах наблюдения на 19,7–35,9 % (p<0,05).
Выводы
1. В условиях нарушенного гомеостаза оксидативно-токсического характера панкреатического происхождения выявлена закономерность, что в миокарде и в кишечнике возникают существенные нарушения липидного метаболизма, коагуляционно-литические расстройства, а также расстройства микроциркуляции и биоэнергетики.
2. Установлен значимый эффект в коррекции (предупреждении прогрессирования) функционально-метаболических нарушений миокарда и кишечника при комбинированном применении ремаксола и лазерной терапии, что обусловлено их способностью влиять на триггерные патогенетические механизмы уже в начале заболевания.



