В настоящее время гомеопатический метод лечения по-прежнему востребован и широко применяется в различных странах мирового сообщества. Об этом свидетельствует тот факт, что в Европейскую, Американскую, Индийскую фармакопеи, фармакопею Великобритании и ряд других включены монографии на гомеопатические лекарственные средства. Кроме того, во многих странах (Германия, Франция, Великобритания, США, Индия) регулярно издаются гомеопатические фармакопеи, в которых содержатся монографии не только на гомеопатические препараты, но и на лекарственные формы, методы анализа гомеопатических лекарственных средств [4].
Одним из наиболее широко используемых в гомеопатической практике лекарственных растений является эхинацея пурпурная Echinacea purpurea (L.) Moench. семейства астровых (Asteraceae). Все растительные иммуномодуляторы, получаемые из эхинацеи, обладают такими фармакологическими эффектами, как иммуностимулирующий, противовоспалительный и противовирусный, и применяются при различных патологических состояниях, связанных с недостаточностью иммунной системы. Препараты эхинацеи применяют внутрь при инфекционных и септических заболеваниях, наружно – при абсцессах, инфицированных ранах, ожогах I и III степени и тяжелых пролежнях. Имеются данные об эффективности препаратов эхинацеи при урогенитальных инфекциях и при длительном применении антибиотиков [3, 5]. Однако ассортимент имеющихся в настоящее время на фармацевтическом рынке препаратов эхинацеи, оказывающих местное и резорбтивное действие, ограничен. Выгодно отличается простотой введения, быстротой всасывания активного вещества, исключением эффекта первого прохождения через печень, способностью оказывать местное и резорбтивное действие такая лекарственная форма, как суппозитории [1]. Поэтому перспективным направлением фармацевтической технологии продолжает оставаться разработка новых гомеопатических препаратов эхинацеи в виде суппозиториев.
В качестве объекта исследования использовали свежую траву эхинацеи пурпурной, собранную в фазу цветения с опытных участков ботанического сада Пятигорского медико-фармацевтического института. Свежесобранное сырье эхинацеи пурпурной представляет собой цилиндрические, прямые, шершавые, ребристые, диаметром до 1,5 см облиственные стебли длиной до 80 см, цветочные корзинки, цветки, бутоны. Цвет стеблей зеленый, иногда с малиновыми или пурпурными пятнами; цвет листьев – зеленый; цветков – малиновый. Запах сырья слабый, вкус – слегка горьковатый. Прикорневые листья с длинными черешками, широкоовальные, зубчатые по краям, суженые к черешку, образуют розетку. Стеблевые листья – сидячие, яйцевидные, остроконечные, неравномерно-крупнозубчатые, реже цельнокрайные с 3-5 продольными жилками. Цветочные корзинки с выпуклым, полым, густоусаженным прицветниками, цветоложем. Обертка блюдцевидная, трехрядная. Краевые цветки язычковые, пестичные, бесплодные, с двух-, трехзубчатым снаружи опушенным отгибом, до 6 см длины. Срединные цветки трубчатые, обоеполые, венчик пятизубчатый.
Диагностическими анатомическими признаками являются: проводящая система пучкового типа, пучок открытый коллатеральный, устьичный аппарат аномоцитного типа, волоски четырех типов (четырехклеточные толстостенные; двухклеточные грубобородавчатые щетинистые; простые одноклеточные; редко встречаются железистые волоски), с розеткой клеток при основании, млечники в мезофилле листа, сопровождающие жилку (рис. 1, 2) [6].
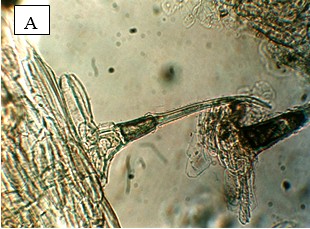
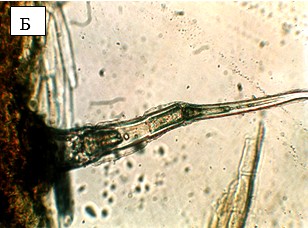
Рисунок 1 – Трихомы листа эхинацеи пурпурной
А - Трихомы верховых листьев (ув.10×1,6)
Б - Трихомы прикорневых листьев (ув.10×1,6)
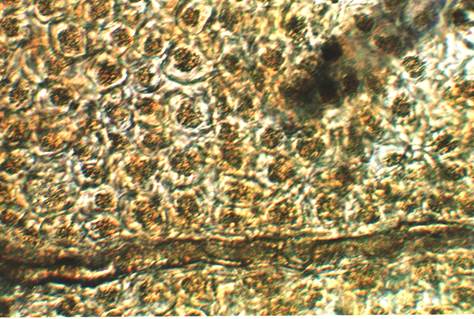
Рис. 2. Млечники в мезофилле листа, сопровождающие жилку (ув. 10×1,6)
Получение настойки эхинацеи гомеопатической матричной осуществляли по третьему методу общей фармакопейной статьи «Настойки гомеопатические матричные» из свежего растительного сырья: свежесобранную траву эхинацеи измельчали и заливали спиртом в соответствии с расчетами 3 параграфа. Настаивали настойку 7 дней в прохладном темном месте. Полученная нами настойка гомеопатическая матричная представляла собой прозрачную жидкость светло-коричневого цвета, горьковатого вкуса с запахом спирта.
В результате проведенных исследований разработана технология и состав настойки гомеопатической матричной Эхинацеи:
|
Травы эхинацеи пурпурной свежей (влажность 60–65 %) |
1,000 кг |
|
Спирта этилового (этанола) 86% (по массе) или 90% (ФС 42-3071-00) |
1,200 кг |
Стандартизацию эхинацеи пурпурной травы в соответствии с ВФС 42-2372-94 проводят по содержанию суммы гидроксикоричных кислот в пересчете на кислоту цикориевую методом УФ-спектрофотометрии. Мы сравнивали УФ-спектры поглощения опытных образцов экстракта эхинацеи жидкого в 0,1М растворе кислоты хлористоводородной и извлечений из травы, которые имеют максимумы при (328±2) нм, минимумы при (265±2) нм и перегибы в области от 200 нм до 400 нм (рис. 3). Это соответствует поглощению суммы гидроксикоричных кислот. Кроме того, установлено, что сопутствующие действующие вещества, в основном хлорофилл, не мешают количественному определению суммы гидроксикоричных кислот.
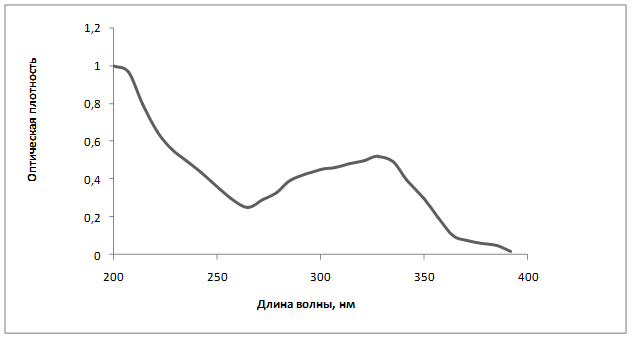
Рис. 3. УФ-спектр экстракта эхинацеи жидкого
В проект фармакопейной статьи предприятия на эхинацеи настойку гомеопатическую матричную нами включены показатели качества, принятые фармакопейной статьей «Настойки гомеопатические матричные», а также показатели, традиционно принятые в зарубежных гомеопатических фармакопеях для матричных настоек из лекарственного растительного сырья [2] (табл. 1).
Таблица 1
Спецификация на настойку гомеопатическую матричную эхинацеи
|
Показатели |
Методы |
Нормы |
|
Описание |
Органолептический |
Прозрачная жидкость от коричневого до зеленовато-коричневого цвета, горьковатого вкуса, с запахом спирта |
|
Подлинность |
Спектрофотометрический |
Спектр поглощения должен иметь максимум при 328±2 нм и перегиб в области 300 – 320 нм (гидроксикоричные кислоты) |
|
Химическая реакция |
С хлоридом железа (III) появляется темно-зеленое окрашивание (фенольные соединения) |
|
|
Сухой остаток |
ГФ XI, вып. 2, с. 161 |
Не менее 3,5% |
|
Плотность |
ГФ XI, вып. 1, с. 24 |
От 0,900 до 0,925 г/см |
|
Содержание спирта |
ГФ XI, вып. 1, с. 26 |
Не менее 64 % |
|
Тяжелые металлы |
ГФ XI, вып. 2, с. 161 |
Не более 0,001% |
|
Микробиологическая чистота |
ГФ XI, вып. 2, с. 193 и изм. от 28.12.1995 г. |
Категория 3 д |
|
Упаковка |
|
В соответствии с ФСП |
|
Маркировка |
|
В соответствии с ФСП |
|
Условия хранения |
|
В прохладном, защищенном от света месте при температуре не выше +12°+15 °С |
|
Срок годности |
|
2 года |
Суппозитории гомеопатические формировали способом выкатывания с помощью основы масло какао или методом выливания расплавленной массы в литьевые суппозиторные формы. При выливании суппозиториев использовали разрешенную фармакопейной статьей на суппозитории гомеопатические основу – твердый жир кондитерский типа А (ГОСТ 28414–89). На основании проведенных исследований предложен следующий состав суппозиториев эхинацеи гомеопатических:
|
Настойка гомеопатическая матричная |
0,2 |
|
Твердый жир типа А (ГОСТ 28414–89) |
достаточное количество для получения суппозиториев массой 2,31 |
Оценку качества суппозиториев эхинацеи гомеопатических проводили в соответствие с требованиями, предъявляемыми к данной лекарственной форме общей фармакопейной статьей «Суппозитории гомеопатические» (табл. 2).
Одним из важнейших критериев оценки качества любой лекарственной формы является стабильность в процессе хранения. Изучение стабильности проводили на 5 сериях суппозиториев в процессе хранения в холодильнике (4±1°С). Суппозитории хранили в ленте ячейковой из поливинилхлорида (ПВХ) и в ленте из алюминиевой фольги. Качество суппозиториев проверяли в день приготовления, а также через 3, 6, 12, 18, 24 месяцев. В процессе хранения суппозиториев установлено, что все показатели оставались без изменения в течение 2,5 лет при хранении суппозиториев при 8°С, что послужило основанием для регламентации срока и условий хранения – 2 года.
Таблица 2
Спецификация на суппозитории эхинацеи гомеопатические
|
Показатели |
Методы |
Нормы |
|
Описание |
Органолептический |
Однородные кремового цвета с желтоватым оттенком без механических включений и блесток |
|
Средняя масса, г |
|
от 2,17 до 2,2 |
|
рН водной вытяжки |
|
6,1-6,7 |
|
Т плавления, °С |
|
не выше 37ºС |
|
Время полной деформации, мин |
|
не более 15 |
|
Подлинность
|
- максимум в области 300-350 нм извлечения в 0,1 моль/л кислоте хлористоводородной
- значение Rf при облучении УФ-светом при длине волны 365 нм |
328±2 нм
3 голубых пятна с Rf 0,40±0,06; 0,53±0,05; 0,64±0,05 |
|
Упаковка |
|
В соответствии с ФСП |
|
Маркировка |
|
В соответствии с ФСП |
|
Условия хранения |
|
В прохладном, защищенном от света месте при температуре не выше +12°+15 °С |
|
Срок годности |
|
2 года |
Технологический процесс получения суппозиториев эхинацеи ректальных гомеопатических представлен на схеме 1 (рис. 3).
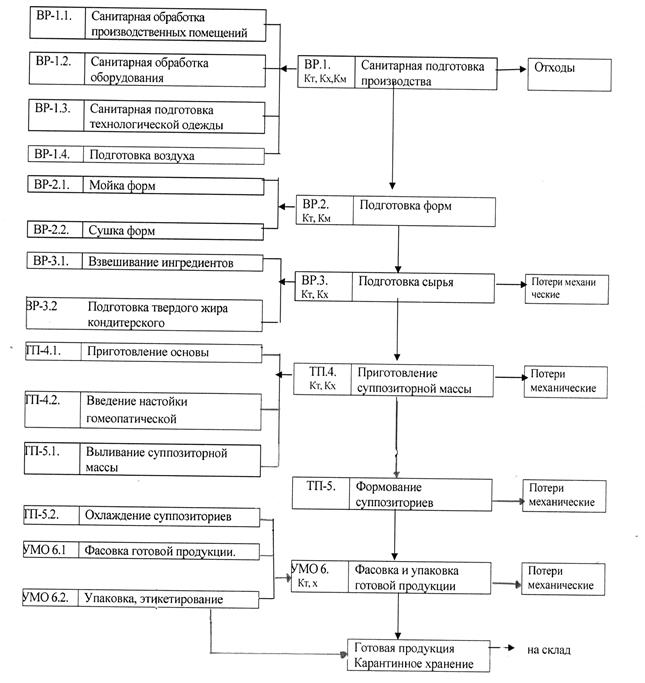
Рис. 3. Схема получения эхинацеи суппозиториев ректальных гомеопатических
Результаты проведенных нами исследований положены в основу нормативной документации в виде проектов фармакопейных статей «Эхинацеи суппозитории ректальные гомеопатические», «Эхинацеи настойка матричная гомеопатическая», которые прошли положительную технологическую апробацию в условиях производства Краснодарского краевого гомеопатического центра.
Методики анализа, включенные в проекты предлагаемых фармакопейных статей, апробированы в условиях Республиканского центра контроля качества и сертификации лекарственных средств Министерства Здравоохранения Республики Северная Осетия-Алания.
Перспектива дальнейшего развития темы исследования возможна в разработке опытно-промышленного регламента, технологической оценке показателей серийного производства, а также в доклиническом изучении разработанной лекарственной формы.
Рецензенты:
Компанцев Д.В., д.фарм.н., заведующий кафедрой технологии лекарств, Пятигорский медико-фармацевтический институт — филиал государственного бюджетного образовательного учреждения высшего профессионального образования «Волгоградский государственный медицинский университет» Министерства здравоохранения России, г. Волгоград;
Шевченко А.М., д.фарм.н., доцент кафедры технологии лекарств, Пятигорский медико-фармацевтический институт — филиал государственного бюджетного образовательного учреждения высшего профессионального образования «Волгоградский государственный медицинский университет» Министерства здравоохранения России , г. Волгоград.



