Считается, что механизм перехода хромосом от одного типа деления к другому вообще, и в частности от митоза к мейозу, остается не известным [5]. Однако на основании проведенного цитологического анализа характера поведения унивалента в анафазе I мейоза у полной серии моносомных линий сорта пшеницы Мильтурум 553 было показано, что коориентация центромер детерминируется зоной исходного полюса [2]. При этом ее структурные изменения меняют ориентацию центромер (с митотического на мейотическое) одного гаплоидного набора хромосом, в то время как их гомологи сохраняют свою прежнюю митотическую ориентацию. Подобного рода манипуляции приводят в соответствие взаимное расположение плеч хромосом и тем самым обеспечивают необходимые условия для прохождения их конъюгации. После завершения синапсиса гомологи с биполярной ориентацией переходят на униполярную. Дальнейшая сегрегация хромосом осуществляется путем разведения кинетохорных нитей веретена в противоположные стороны и их встраивания в центральное веретено. Исходя из полюсной детерминации ориентации хромосом и предложенной концепции «разводящих нитей» может быть понят и механизм автоориентации хромосом в мейозе II.
Материал и методы исследования
Исследования проводили на сорте яровой мягкой пшеницы Мильтурум 553 и его полной серии моносомных линий. Потомство моносомных растений и исходного сорта высевали в теплице в сосуды и выращивали при 16-часовом освещении с 23/18 оС температурным циклом.
Фиксацию микроспороцитов осуществляли в межфазный период «выход в трубку – колошение». В качестве фиксаторов использовали смеси Ньюкомера [4] и Навашина [9]. Для этого с каждого растения брали по одному-два колоса. Цитологический анализ мейоза проводили на временных давленых ацетокарминовых препаратах с помощь светового микроскопа МБИ-3 при увеличении 20х10. По каждой линии анализировали от 10 до 15 растений. Для цитологического анализа использовались только первый и второй цветок колосков, расположенных в нижней части колоса.
Результаты исследования и их обсуждение
При мейотическом делении клеток в профазе I происходит удвоение хромосом. В результате каждая из них к началу редукционного деления состоит из двух хроматид, имеющих свои центромеры. В метафазе I и анафазе I сестринские центромеры хромосом, входящих в состав бивалентов, имеют униполярную ориентацию, которая сохраняется до начала второго мейотического деления. Следовательно, для перехода хромосом от редукционного типа деления к эквационному необходима соответствующая перестройка ориентации центромер, то есть автоориентация [6].
По данным литературных источников [1; 3], в профазе митоза на двух противоположных сторонах центромеры образуются два кинетохора, ориентированные в противоположных направлениях. Считается, что именно данное обстоятельство определяет в дальнейшем эквационное деление хромосом. Однако в работе [8] показано, что отделенные кинетохоры хроматид в мейозе II сохраняют свое расположение «бок о бок» (side-by-side) до их приложения к веретену. Это в свою очередь указывает на то, что в данном случае не положение кинетохор определяет характер их дальнейшего расхождения, а, наоборот, смена ориентации сил приложения с униполярного на биполярное определяет расположение кинетохор относительно друг друга.
В результате завершения первого мейотического деления образуются диады, которые содержат уменьшенное количество хромосом, но при этом n = 2х. На данной стадии формируется ядро, а из мембран и его оболочка. В это время хромосомы частично деконденсируются. Данный период интерпретируется еще как интеркинез. Его целесообразность, кроме как возможность дополнительного синтеза веществ, остается до конца не понятной. Однако при полюсной детерминации ориентации центромер в мейозе наличие в переходный период между двумя его стадиями интеркинеза становится не только понятным, но и просто необходимым.
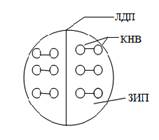
После завершения первого мейотического деления в интеркинезе хромосомы не теряют своей связи с полюсной зоной, о чем свидетельствует сохранение пространственной организации расположения хромосом. Однако точки фиксации в ней остаются ориентированными по типу предыдущего редукционного деления (рис. 1 а, б).
 а
а 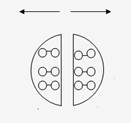 б
б
 в
в 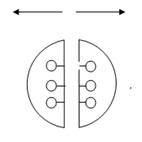 г
г
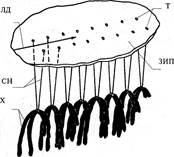
Рис. 1. Ориентация кинетохор при редукционном (а, б) и эквационном (в, г) делении хромосом; ЗИП – зона исходного полюса; ЛДП (ЛД) – линия деления зоны исходного полюса; КНВ – кинетохорные нити веретена; Т – точки фиксации кинетохорных нитей веретена; Х – хромосомы.
Для того чтобы перевести точки фиксации центромер с униполярной ориентации на биполярную, необходимо выстроить их в зоне исходного полюса относительно линии его потенциального деления в последовательности, обеспечивающей при разведении кинетохорных нитей веретена эквационное деление хромосом (рис. 1 в, г). Для проведения подобного рода манипуляций наличие ядерной оболочки оказывается в данном случае оправданным.
Трудность изучения переходного периода от мейоза I к мейозу II заключается в том, что определяющие его периоды интеркинез и профаза II проходят достаточно быстро и уловить нужный момент оказывается не так просто. При изучении двух вышеперечисленных стадий были проанализировано более 16 тысяч диад. Однако полученные результаты дали вполне логическое построение событий, происходящих при переходе от редукционного к эквационному типу деления хромосом.
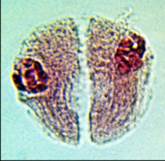
Исследования, проведенные на материале, фиксированном смесью Навашина, показали, что в диадах микроспор пшеницы в норме часто наблюдаются дугообразные светлые зоны, идущие от клеточной перегородки диады. При этом ядра оказываются прижаты к внешней оболочке ядра (рис. 2а). Характерные линии, образующие эти зоны, дают основание считать, что образование подобного рода конфигураций связано с началом формирования центрального веретена деления.
 а
а 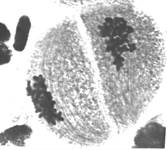 б
б
 в
в 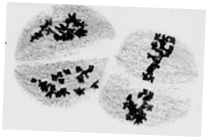 г
г
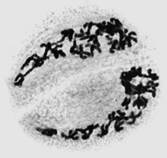
Рис. 2.
К сожалению, используемая методика проводимых исследований не дает возможности достоверно определить наличие ядерной оболочки на данном этапе происходящих мейотических процессов. Тем не менее это не исключает возможности начала формирования центрального веретена деления на стадии интеркинеза. В то же время результаты дальнейших наблюдений показывают, что при демонтаже ядерных мембран и конденсации хромосом клетки диады имеют вполне оформленное центральное веретено деления (рис. 2б). При этом хромосомы также оказываются прижатыми к внешней оболочке клетки. Однако часто группы хромосом, ранее входящие в состав ядра, располагаются в зоне одного из полюсов центрального веретена. После разведения зоной исходного полюса кинетохорных нитей они встраиваются в центральное веретено и вступают с ним во взаимодействие (рис. 2в). Данный фактор приводит в движение хромосомы, которые перемещаются вдоль нитей центрального веретена. При достижении уравновешивания сил натяжения хромосомы выстраиваются в экваториальной плоскости клетки (рис. 2г).
Таким образом, предлагаемая модель механизма автоориентации хромосом при их переходе от редукционного типа деления к эквационному достаточно хорошо согласуется с результатами проведенных цитологических наблюдений за диадами микроспор. Одним из важных моментов, происходящих при этом процессе, является полюсная детерминация ориентации центромер в мейозе и тот факт, что центральное и кинетохорное веретено формируются в разном месте и до определенного периода непосредственно не связаны между собой. В одной из своих работ R. Bruce Nicklas [7] отмечает, что центральное веретено и кинетохорное формируются в разное время и в разном месте.
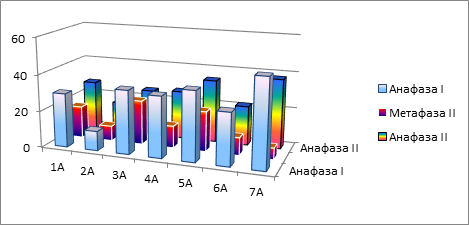
При переходе хромосом от редукционного типа деления к эквационному в норме они имеют две хроматиды, каждая из которых обладает своей центромерой а, следовательно, и кинетохором. Наличие двух кинетохор является определяющим моментом в прохождении правильной их полюсной ориентации при переходе хромосом от редукционного деления к эквационному. Однако несколько иначе складываются обстоятельства, когда в данном процессе участвует только один кинетохор. Подобно коориентации унивалента в профазе I, точка фиксации единичного кинетохора может быть не затронута структурными изменениями зоны исходного полюса, и тогда хроматида должна сохранять свою прежнюю униполярную ориентацию. Однако при полюсных изменениях эта точка может быть смещена в зону предстоящего раздела исходного полюса, и после разведения образовавшихся секторов в противоположные стороны хроматида будет задействована двумя полюсами центрального веретена деления. При этом исход дальнейшей сегрегации хроматиды в анафазе II будет зависеть от характера произошедшего расщепления кинетохорного пучка микротрубочек. Соответственно, в зависимости от распределения сил приложения либо она выстроится вместе с другими хромосомами в экваториальной плоскости, либо окажется вне ее зоны, либо произойдет поперечное деление ее центромеры. Проведенный статистический анализ характера поведения хроматиды по всему гаплоидному набору хромосом в мейозе II показал, что в процессе автоориентации происходит их дифференциация по геномной принадлежности (рис. 3).
 а
а
 б
б
 в
в
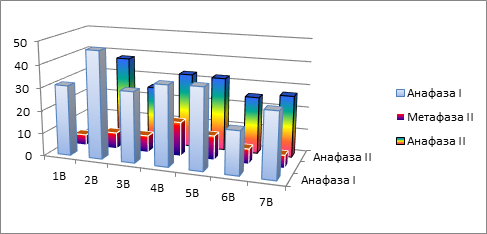
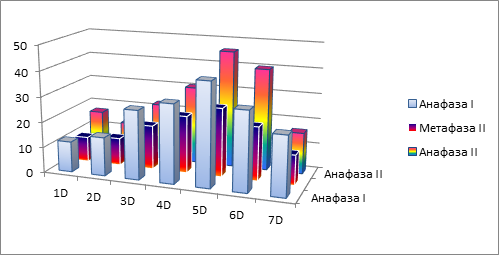
Рис. 3. Гистограммы распределения частоты клеток с отстающими хроматидами на разных стадиях мейотического деления по хромосомам геномов А, В и D
Как следует из вышесказанного, источником присутствия отдельных хроматид во втором мейотическом делении является продольное расщепление унивалента в анафазе I. В среднем по серии моносомных линий доля клеток в анафазе I с эквационным делением унивалента составила 29,75%, а их количество с отброшенными хроматидами в метафазе II – 13,56%. Разница между двумя этими показателями оказалась равной 16,19%. Следовательно, можно предположить, что в 16,19% случаев от всех изученных клеток хроматиды в метафазе II располагались вместе с другими хромосомами в экваториальной зоне.
Как уже отмечалось ранее, полученное содержание клеток в метафазе II с отброшенными хроматидами отражает лишь общую закономерность анализируемого генотипа. Конкретное же их содержание существенно варьировало по моносомным линиям. При этом коэффициент парной корреляции между частотой биполярного типа поведения унивалента в анафазе I и наличием клеток с отброшенными хроматидами в метафазе II в среднем по серии моносомных линий составил 0,23. Однако этот показатель существенно менялся в пределах хромосом одного генома (рис. 3). Так, по геному А - r = 0,16, геному В - r = 0,27, геному D - r = 0,95.
Для метафазы II оказалось характерным проявление некоторой закономерности распределения частоты клеток с отброшенными хроматидами. Так, по геному А просматривается два уровня кривых распределения (рис. 3а). К первому можно отнести хромосомы 1А, 3А и 5А, ко второму – 2А, 4А, 6А и 7А. По геномам В и D в состав аналогичного ряда входят все 7 хромосом каждого из них (рис. 3 б, в). При этом характер распределения частот по хромосомам в обоих случаях оказался близок к кривой нормального распределения.
Ситуация с хроматидами во втором мейотическом делении существенно меняется в анафазе II. Количество клеток с отстающими хроматидами по сравнению с метафазой II резко возрастает. При этом их уровень почти достигает частоты продольного расщепления в анафазе I (27,36% против 29,75%). Однако характер варьирования данного признака также дифференцируется по геномам. Как видно из рисунков 3а и 3б, в пределах хромосом геномов А и В оно имело несколько хаотичное проявление. Однако при этом доля клеток с отстающими хроматидами в анафазе II достаточно тесно коррелировала с частотой эквационного деления унивалента в анафазе I. Их частные коэффициенты составили по геному А 0,92, геному В – 0,91. Соответственно между анафазой и метафазой второго деления - -0,04 и 0,38.
Весьма своеобразно проявились частота образования хроматид по хромосомам генома D в мейозе I и их поведение в мейозе II (рис. 3в). Прежде всего, при попарном сравнении наблюдалась тесная корреляционная зависимость между тремя анализируемыми фазами мейоза. Их коэффициенты находились в пределах 0,92 – 0,95. При этом для хромосом генома D по каждой из рассматриваемых фаз мейоза оказалась специфичной тенденция проявления характера варьирования частот по типу нормального распределения (рис. 3в).
При сопоставлении гистограмм, представленных на рисунке 3, видно, что своего рода упорядоченность поведения хроматид идет в возрастающем порядке от генома А к геному D. Подобного рода дифференциация может быть связана с особенностями эволюции мягкой пшеницы как вида, где к геному А были привнесены хромосомы генома В, а потом и генома D.
Таким образом, результаты исследований, проведенные на диадах микроспор, показали, что центральное веретено и кинетохорное формируются независимо друг от друга. В момент формирования центрального веретена деления ядра оказываются прижатыми к внешней оболочке ядра. При этом они могут быть перемещены к одному из противоположных полюсов центрального веретена, откуда начинается взаимодействие кинетохорных нитей с центральными и продольное перемещение хромосом до уравновешивания альтернативных сил натяжения и выравнивания их в экваториальной плоскости. Анализ характера поведения хроматид во втором мейотическом делении показал, что по частоте клеток с отброшенной или отстающей хроматидой существует определенная упорядоченность. При этом хромосомы дифференцируются по их геномной принадлежности. Подобного рода упорядоченность возможна только при наличии определенной централизации управления данным процессом. Таким образом, на основании проведенных исследований есть все основания считать, что автоориентация хромосом в мейозе II детерминируется зоной исходного полюса, которая обеспечивала их расхождение при эквационном делении.
Рецензенты:
Плотникова Л.Я., д.б.н., профессор кафедры селекции, генетики и физиологии растений ОмГАУ, г. Омск.
Евдокимов М.Г., д.с.-х.н., заведующий лабораторией селекции твердой пшеницы ФГБНУ «СИБНИИСХ», г. Омск.



