Закономерности распределения микроэлементов в нефтях и пластовых водах раскрывают природу генезиса химических элементов в природных системах, то есть их источник, характер миграции, накопления и осаждения [130,131]. По литературным данным, хлоридно-натриевые воды и рассолы являются аккумуляторами микро- и макрокомпонентов, таких как йода, брома, бора, стронция, германия, цезия и другие элементы, позволяющие использовать их на практике [21].
Воды нефтяных месторождений и причины обогащения йодом интересовали многих ученых и посвящены многочисленные исследования. В пластовых водах концентрирование йода связано с накоплением йода в морских илах и воде [11,140].
Такой химический элемент как йод можно охарактеризовать как подвижного эмигранта и рассеянного элемента в земной коре. В природе йод встречается в морской воде, в виде минералов и в минерализованных водах. Йодосодержащие минералы не имеют промышленного значения из-за своей редкости и малочисленности. Низкое содержание йода в морской воде объясняется тем, что из-за деятельности микроорганизмов не происходит накопление йода. Так как воды нефтяных месторождений попутно добываются попутно, то рационально было бы использовать в качестве бесплатного сырья [80].
При содержании йода не меньше 10 -18 мг/л, попутные воды считаются перспективными для добычи йода.
В нашем исследовании анализировались пробы пластовых минерализованных вод таких нефтяных месторождений как Калининское, Курганное, Комсомольское, Состинское, Курганное.
Для анализа содержания йода и брома применялись методы потенциометрии с ион-селективными электродами.
Бром и йод, относятся к рассеянным элементам. Наибольшая концентрация брома наблюдается в водах таких гидрогеологических зон, где существуют условия, благоприятные для сохранения нефти, поэтому содержание брома можно использовать при прогнозе нефтегазоносности как один из показателей гидрогеологической закрытости структур.
Наиболее четко это проявляется в значениях хлорбромного коэффициента. Большая минерализация вод и накопление хлоридов кальция и брома в них характерно для структур, к которым приурочены залежи нефти, и по мере увеличения степени метаморфизма вод происходит обогащение вод хлоридами и бромом. Однако при определенных концентрациях это соотношение нарушается, и накопление брома опережает рост абсолютного содержания хлоридов, что связывается с достижением предела растворимости у хлоридов раньше, чем у брома (NaBr), и часть хлоридов удаляется из рассола.
В морской воде содержание брома составляет около 6 мг/дм3, и при процессах концентрирования вод в первой фазе содержание брома увеличивается пропорционально содержанию хлора, вследствие чего их отношение равно 290-300. Так как для вод моря эта величина является геохимической константой, ее значение предложено именовать показателем степени метаморфизованности вод. [149]. Отклонение значений хлорбромного коэффициента в сторону увеличения обусловливается процессами аномального накопления хлора, в частности, выщелачиванием залежей каменной соли.
Вторым по значению микрокомпонентом пластовых вод является йод.
Причины обогащения йодом вод нефтяных месторождений интересовали многих ученых и этому вопросы посвящены многие исследования. Установлено, что концентрирование йода в пластовых водах непосредственно связано с процессами накопления его в морских илах и содержащейся в илах воде. Устанавливается тенденция к уменьшению концентрации йода с глубиной, то есть с увеличением минерализации вод.
Таблица 1
Распределение содержания йода и брома и хлорбромного коэффициента
|
Месторождение |
Содержание (мг/л) |
Хлорбромный коэффициент (Cl/Br) |
|
|
йода |
брома |
||
|
Калининское |
9,52 |
215 |
346,26 |
|
Комсомольское |
10,00 |
230,00 |
258,94 |
|
Курганное |
10,50 |
221,70 |
528,42 |
|
Состинское |
9,00 |
126,00 |
517,88 |
|
Шахметское |
7,50 |
250,00 |
343,16 |
Содержание йода в пробах пластовых вод исследуемых нефтяных месторождений варьировало от 7,5 мг/л до 10,5 мг/л. Наименьшее содержание йода соответствовало пробе вода Шахметского месторождения, а наибольшее количество – пробе Курганного месторождения (табл.1).
Хлорбромный коэффициент представляет собой функцию глубины залегания вод, минерализации и степени закрытости недр. То есть можно отметить, что данный коэффициент не зависит от литолого-фациального характера пород. Если же данный коэффициент с глубиной уменьшается, то тогда увеличивается закрытость недр, а также уменьшается соляные залежи. По распределению данного коэффициента по пластовым водам исследуемых месторождений наблюдается следующее: наименьшее значение коэффициента соответствует пробе Комсомольского месторождения, а наибольшее значение – пробе Курганного месторождения. По распределению данного коэффициента можно сказать, что наименьшее содержание хлоридов будет отмечено в пробе пластовой воды Комсомольского месторождения.
Не остается незамеченным тот факт, что исследуемые пластовые воды являясь источником йода и брома, могут быть применены в качестве промышленного сырья данных микроэлементов.
Наиболее подходящим и более рентабельным является метод ионообменной сорбции. Перспективность этого метода разделения и концентрирования элементов в целях химического анализа. Сорбция в динамических условиях не требует разделения фаз и позволяет ускорить разделение и концентрирование и автоматизировать весь цикл анализа, включая отбор проб, концентрирование и определение элементов. Дополнительное преимущество сорбции – это селективность. Суть ионообменной сорбции заключается в обменной адсорбции. В результате адсорбции лежит диффузия иона к активным центрам ионообменника и в раствор.
Для наших исследований возможность сорбции йода и брома из пластовых минерализованных вод оценивалась степенью извлечения микроэлементов. В ходе исследований применялись ионообменные смолы – аниониты АН-31 и АН-2ФН.
Таблица 2
Физико-химические показатели анионитов
|
Показатели |
Марки анионитов |
|||
|
АН-31 |
АН-2ФН |
|||
|
Внешний вид |
Зерна желтого цвета |
Зерна кирпичного цвета |
||
|
Размер зерен, мм |
0,4 – 2,0 |
0,4-2,0 |
||
|
Коэффициент однородности |
0,3 |
0,3 |
||
|
Содержание влаги, % |
5 |
5 |
||
|
Влагоемкость, В±0,02 г H2O/г |
OH-форма |
Cl-форма |
OH-форма |
Cl- форма |
|
1,21 |
1,45 |
0,70 |
0,95 |
|
|
Полная статическая обменная емкость |
2,6 |
3,0 |
||
|
Обменная емкость (±0,03) ммоль-экв/г |
По сильным группам |
ПОЕ |
По сильным группам |
ПОЕ |
|
0,28 |
10,00 |
0,18 |
4,63 |
|
Анализировали сорбцию иода и брома в динамических условиях. Опыты проводили на хроматографических колонках с диаметром d=16 мм. Для исследований брали навеску 10 г анионитов. Высота слоя сорбента в колонке составляла 16 см.
Исследования проводили при разных температурах, а именно 5°С, 25°С, 35°С. При помощи уравнения Ленгмюра были рассчитаны термодинамические характеристики, в частности ∆H, ∆G, ∆S и К.
Таблица 3
Термодинамические показатели (∆Н, ∆G, ∆S) и константы равновесия при различных температурах
|
Температура, К |
∆Н, кДж/моль |
-∆G, кДж/моль |
∆S, Дж/моль∙К |
Константа,К |
|
278 |
9,77 |
13,002 |
8,19 |
0,1118 |
|
298 |
14,108 |
8,01 |
0,1437 |
|
|
308 |
14,946 |
8,02 |
0,1905 |
Из табл. 3 и табл. 4 следует, что полученные значения энергии Гиббса (∆G) с повышением температуры изменяются незначительно.
Таблица 4
Термодинамические показатели сорбции бромид-ионов
|
Температура, К |
∆Н, кДж/моль |
-∆G, кДж/моль |
∆S, Дж/моль∙К |
Константа,К |
|
278 |
4,32 |
10,000 |
2,04 |
0,0132 |
|
298 |
10,270 |
2,00 |
0,0158 |
|
|
308 |
10,010 |
1,85 |
0,0199 |
Значения энергии Гиббса подтверждают возможность самопроизвольного протекания процесса сорбции йода и брома на анионитах АН-31 и АН-2ФН.
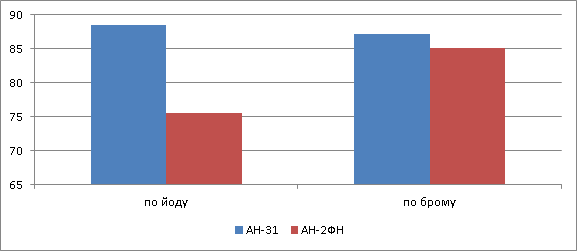
Рис.1. Степень извлечения (%) йода и брома анионитами АН-31 и АН-2ФН.
По рис.1 видно, что для извлечения йода из пластовых вод имеет смысл применить анионит марки АН – 31, т. к его степень извлечения на 7 % больше, чем степень извлечения анионита АН – 2ФН. Для извлечения брома необходимо применять анионит 2 –ФН (рис.1).
С увеличением времени сорбции пластовых вод увеличивается степень извлечения йода и только при 80 мин происходит полное насыщение сорбента. Наиболее выгодным для извлечения йода является анионит АН-31 и при температуре 308 К (рис. 2).
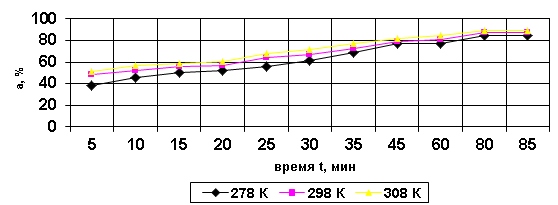
Рис. 2. Кинетическая кривая сорбции йодид-ионов АН – 31.
Максимальная концентрация йодид-ионов на анионите марки АН–2ФН отмечается по истечению 1 часа и степень извлечения составляет 80%.
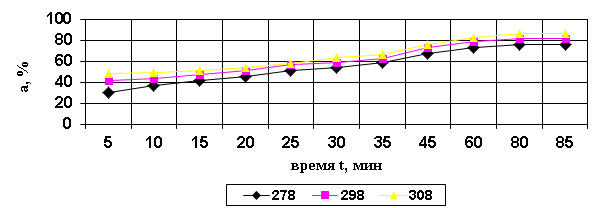
Рис.3. Кривые сорбции иодид-ионов АН-2ФН.
Оценивая степень извлечения анионитов двух марок, можно объективно сказать, что наиболее подходящим сорбентом для йодид - ионов служит ионообменная смола АН – 31 (рис.2, рис.3).
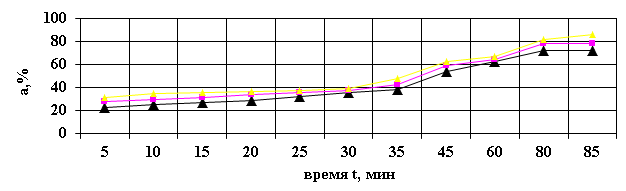
Рис.4. Кривые сорбции бромид-ионов АН-31.
По степени извлечения бромид - ионов обоих анионитов существенной разницы не отмечается. Так, например, степень извлечения АН – 31 составляет 87 %, а степень извлечения АН – 2 ФН – 75 %.
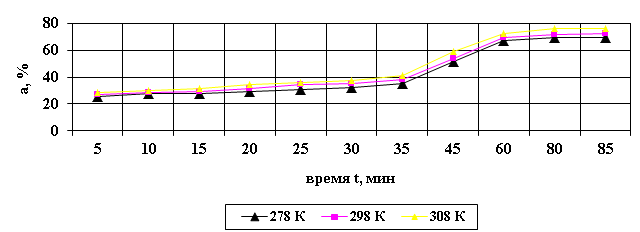
Рис. 5. Кинетическая кривая сорбции бромид – ионов анионитом АН – 2ФН.
Максимальное извлечение бромид – ионов для АН – 31 и для анионита АН – 2 ФН – характерно по истечении 60 мин (рис. 4, рис. 5).
Подведя итоги, можно сказать:
- пластовые воды значительные количества йода и брома, являясь высокоперспективным сырьем микроэлементов;
-по результатам анализов, кинетики сорбции извлечения йода видно, что наибольшее насыщение сорбента происходит при температуре 308 К;
- по кинетике сорбции максимальное насыщение сорбента на АН-31 наблюдаем после 80 мин., на анионите АН-2ФН – 60 мин.
-по результатам анализа видно, что для извлечения йода из пластовых вод имеет смысл применить анионит марки АН – 31, т. к его степень извлечения на 7 % больше, чем степень извлечения анионита АН – 2ФН. Для извлечения брома необходимо применять анионит 2 –ФН.
Рецензенты:
Мойсейкина Л.Г., д.б.н., профессор Калмыцкого Государственного университета, г. Элиста;
Сангаджиева Л.Х., д.б.н., профессор Калмыцкого Государственного университета, г. Элиста.



