Введение
Геморрагическая лихорадка с почечным синдромом (ГЛПС) относится к числу тяжелых природно-очаговых вирусных инфекций, при которых наблюдаются выраженные клинические проявления, включая лихорадку, нарушение функции почек и склонность к геморрагическим осложнениям. Повышенный интерес к изучению данной патологии обусловлен ее значительным вкладом в структуру инфекционной заболеваемости и высокой смертностью при осложненном течении [1].
Патогенетические механизмы развития ГЛПС в значительной степени связаны с деструктивными процессами на уровне клеточных мембран, вызванными активацией перекисного окисления липидов (ПОЛ) и дефицитом ферментов антиоксидантной защиты [2, 3]. Усиленное образование свободных радикалов при вирусной агрессии приводит к повреждению липидных компонентов биомембран, нарушению их целостности и, как следствие, к ухудшению функционирования клеток и тканей.
Процесс ПОЛ представляет собой цепную реакцию окисления полиненасыщенных жирных кислот, сопровождающуюся образованием промежуточных соединений – диеновых конъюгатов и кетонов. Повышенная концентрация этих продуктов указывает на наличие окислительного стресса, усугубляющего течение инфекционного процесса [4, 5].
Исследования последних лет демонстрируют, что в остром периоде вирусной инфекции уровень диеновых соединений возрастает в несколько раз по сравнению с физиологической нормой, что подтверждает вовлеченность процессов ПОЛ в патогенез [6, 7]. Наряду с этим наблюдается снижение активности супероксиддисмутазы (СОД) – фермента, выполняющего ключевую роль в нейтрализации активных форм кислорода. При поражениях почек снижение активности СОД может достигать четырехкратного значения, что отражает выраженность патологического процесса [8].
Согласно литературным источникам, комплексный анализ показателей ПОЛ и антиоксидантной активности является важным направлением мониторинга состояния пациентов.
Применение спектрофотометрических методов и определение ферментативной активности позволяют выявить степень окислительного стресса и обосновать необходимость коррекции терапии [9, 10].
Установлено, что нормализация активности СОД у пациентов с ГЛПС коррелирует с положительной клинической динамикой, что делает данные параметры важными в оценке эффективности лечения [11, 12].
С учетом вышеизложенного целесообразно исследование уровня оксидативного стресса и состояния антиоксидантной системы у больных ГЛПС средней степени тяжести на фоне проводимой терапии. Это позволит глубже понять механизмы патогенеза заболевания и разработать подходы к его коррекции [13].
Цель исследования – оценить состояние перекисного окисления липидов на основании определения содержания диеновых конъюгатов и диеновых кетонов, а также активности супероксиддисмутазы у пациентов с ГЛПС средней степени тяжести, получающих стандартную базисную терапию.
Материал и методы исследования
В исследование включены 37 пациентов (25 мужчин, 12 женщин) в возрасте от 19 до 54 лет (средний возраст 34,8±6,2 года) с подтвержденным диагнозом ГЛПС средней степени тяжести. Контрольную группу составили 10 условно здоровых добровольцев, сопоставимых по полу и возрасту.
Критерии включения:
- лабораторно подтвержденный диагноз ГЛПС;
- средняя степень тяжести;
- возраст 18–60 лет;
- отсутствие хронических заболеваний в стадии декомпенсации.
Критерии невключения:
- тяжелая или легкая форма ГЛПС;
- выраженная печеночная, сердечная или почечная недостаточность иной природы;
- прием антиоксидантных препаратов до включения в исследование;
- беременность.
Критерии исключения:
- появление осложнений, требующих интенсивной терапии;
- отказ пациента от участия;
- выявление ранее не указанной коморбидности, влияющей на показатели ПОЛ.
У обследуемых регистрировались уровни диеновых конъюгатов и диеновых кетонов в плазме крови, а также активность СОД. Забор биоматериала осуществлялся дважды: при поступлении и на 10-е сутки терапии.
Для количественного определения диеновых соединений использовался спектрофотометрический метод, основанный на измерении оптической плотности [14]. Оценка ферментативной активности СОД проводилась по способности замедлять автоокисление кверцетина, что позволяет судить о функциональном состоянии антиоксидантной системы [15].
Обработка данных выполнена в программе Statistica 10.0. Тип распределения проверен критерием Шапиро – Уилка. Поскольку данные распределялись нормально, применялся параметрический t‑критерий Стьюдента. Статистически значимыми считали различия при p<0,05.
Результаты исследования и их обсуждение
Диеновые соединения образуются в результате окисления полиненасыщенных жирных кислот, которые являются ключевыми компонентами мембранных липидов клеток. Колебания концентрации этих веществ отражают степень выраженности окислительного стресса и степень структурных нарушений мембран. Диеновые кетоны также указывают на прогрессирующее повреждение мембранных структур и могут выступать предикторами клеточной дисфункции.
Уровень первичных диеновых конъюгатов и диеновых кетонов может влиять на уровень антиоксидантной защиты организма, в том числе активности ферментов супероксиддисмутазы. В связи с этим проведены исследования по оценке этих показателей у больных ГЛПС.
В начальной фазе заболевания было отмечено повышение уровня диеновых конъюгатов. Средний уровень этого показателя у пациентов достигал 1,076±0,36 едА/мл, что в 4,2 раза превышало значения в контрольной группе (0,255±0,09 едА/мл, p=0,003). Это указывает на активное развитие ПОЛ в остром периоде ГЛПС.
Аналогичная тенденция наблюдалась и для диеновых кетонов – их уровень составил 0,106±0,045 едА/мл, что в 2,4 раза выше, чем у здоровых лиц (0,043±0,03 едА/мл, p=0,011). (табл.1, рис. 1).
Таблица1
Содержание диеновых соединений в плазме крови контрольной группы и основной группы (больные ГЛПС средней степени тяжести)
|
Показатели |
Контрольная группа (n=10) |
Основная группа (n=37) |
р |
|
Диеновые конъюгаты едА/мл |
0,255±0,09 |
1,076±0,36 |
0,003 |
|
Диеновые кетоны едА/мл |
0,043±0,03 |
0,106±0,045 |
0,011 |
Примечание: р – достоверность различий между показателями основной группы и контрольной группы
Составлена авторами на основе полученных данных в ходе исследования
|
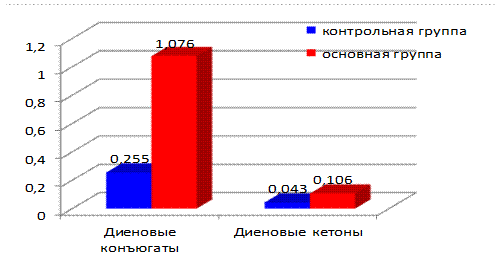
Рис.1. Содержание диеновых конъюгатов и диеновых кетонов (едА/мл) в плазме крови контрольной группы и основной группы.
Примечание: составлен авторами по результатам данного исследования
В начальный период заболевания происходит интенсивное образование первичных продуктов перекисного окисления липидов. Изменения в концентрации первичных диеновых конъюгатов и диеновых кетонов свидетельствуют о наличии окислительного стресса в организме. Повышенный уровень окислительного стресса в организме пациентов с геморрагической лихорадкой с почечным синдромом является следствием увеличения производства свободных радикалов и повышенного окислительного метаболизма в клетках.
Об интенсивности первичных (начальных) процессов ПОЛ говорит тот факт, что концентрация диеновых кетонов, которые являются продуктами дальнейшего превращения диеновых конъюгатов, превышено в 2 раза, а диеновых конъюгатов в 4 раза.
На фоне проведенной терапии (10 суток) отмечалось снижение концентрации как диеновых конъюгатов, так и кетонов примерно в 1,3 раза по сравнению с исходными показателями. Это может свидетельствовать о частичной нормализации процессов перекисного окисления липидов на фоне лечебного воздействия (табл.2, рис. 2).
Таблица2
Содержание диеновых соединений в плазме крови больных ГЛПС средней степени тяжести до и после лечения
|
Показатели |
До лечения |
После лечения |
р |
|
Диеновые конъюгаты едА/мл |
1,076±0,36 |
0,812±0,31 |
0,027 |
|
Диеновые кетоны едА/мл |
0,106±0,045 |
0,078±0,06 |
0,041 |
Примечание: р – достоверность различий между показателями до и после лечения.
Составлена авторами на основе полученных данных в ходе исследования
|
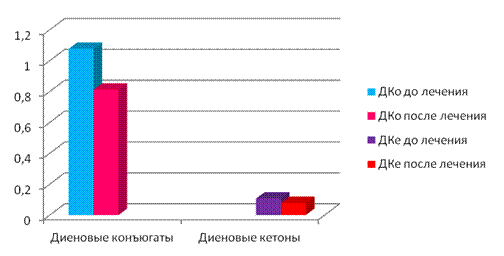
Рис.2. Изменение концентрации ДКо и ДКе в плазме крови больных ГЛПС средней степени тяжести до и после лечения.
Примечание: составлен авторами по результатам данного исследования
Представленные результаты подтверждают, что вирусная инфекция при ГЛПС сопровождается выраженным окислительным стрессом. Значительное повышение уровней диеновых продуктов в плазме отражает активацию деструктивных процессов в клеточных структурах. Положительная динамика на фоне терапии позволяет говорить об эффективности применяемого лечения в отношении подавления ПОЛ.
Таким образом, измерение концентрации первичных диеновых конъюгатов и диеновых кетонов в крови может быть полезным методом оценки окислительного стресса и повреждения мембран у пациентов с ГЛПС
Дополнительно авторами было проанализировано влияние возраста и пола на уровень первичных диеновых конъюгатов и диеновых кетонов у больных ГЛПС средней степени тяжести на фоне базисной терапии. Полученные данные не выявили статистически значимых различий между подгруппами, что позволяет рассматривать данные параметры как независимые от этих факторов.
На уровень первичных диеновых конъюгатов и диеновых кетонов может влиять уровень антиоксидантной защиты организма, в том числе активности ферментов супероксиддисмутазы (СОД) и каталазы, а также уровень малонового диальдегида (МДА) – продукта ПОЛ.
Динамику работы антиоксидантной системы больных ГЛПС средней степени тяжести авторы изучали на примере изменения активности СОД плазмы крови. В начальный период болезни активность данного фермента в плазме крови резко снижена с достоверным отличием от контрольной группы, что коррелируется с данными по диеновых конъюгатов (табл.3, рис.3).
Таблица3
Активность СОД в плазме крови больных ГЛПС средней степени тяжести до и после лечения
|
Показатели |
Контрольная группа |
До лечения |
После лечения |
|
СОД, у.е. |
0,576±0,07 |
0,164±0,07
|
0,188±0,10
|
Примечание: составлена авторами на основе полученных данных в ходе исследования
|
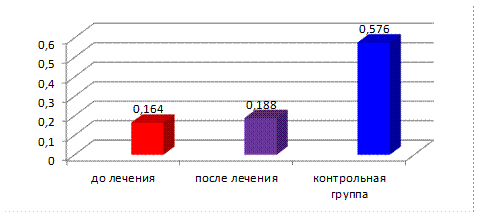
Рис.3. Изменения активности СОД в плазме крови больных ГЛПС средней степени тяжести до и после лечения.
Примечание: составлен авторами по результатам данного исследования
Исследование показало, что уровень СОД в плазме крови пациентов в начальный период заболевания существенно снижен по сравнению с нормальными значениями. Это свидетельствует о нарушении антиоксидантной защиты организма пациентов с ГЛПС. Активность СОД у больных ГЛПС со средней степенью тяжести составила 0,164±0,07 у.е, что является ниже значений контрольной группы в 3,6 раза (0,576±0,07 у.е. (p=0,002)).
После проведения 10-дневной базисной терапии активности СОД увеличилась (0,188±0,10 у.е., различия с исходным значением статистически незначимы (p=0,12)). Однако уровень СОД все еще оставался ниже значений контрольной группы в 3,1 раза. Снижение активности СОД отражает истощение антиоксидантных резервов организма, что также подтверждается исследованиями зарубежных авторов.
Полученные данные демонстрируют выраженный окислительный стресс при ГЛПС средней тяжести. Значительное увеличение первичных продуктов ПОЛ указывает на активное повреждение мембранных структур. Наряду с этим у пациентов отмечается снижение активности СОД, что согласуется с данными современных исследований, указывающих на подавление ферментативного звена антиоксидантной защиты при хантавирусной инфекции.
На фоне базисной терапии наблюдалось частичное восстановление показателей ПОЛ, что отражает снижение выраженности окислительного стресса. Однако активность СОД остается низкой, что требует дальнейшего изучения вопроса о возможной коррекции антиоксидантной терапии.
Заключение
У пациентов с геморрагической лихорадкой с почечным синдромом средней степени тяжести в олигурический период отмечается выраженная активация первичных звеньев перекисного окисления липидов, сопровождающаяся накоплением начальных продуктов липопероксидации – диеновых конъюгатов. Повышение концентрации диеновых конъюгатов и диеновых кетонов отражает развитие окислительного стресса и свидетельствует о повреждении клеточных мембран вследствие интенсификации свободнорадикальных процессов.
У больных геморрагической лихорадкой с почечным синдромом на высоте инфекционного процесса на фоне накопления продуктов перекисного окисления липидов наблюдалось снижение активности ферментативного звена антиоксидантной защиты, в частности супероксиддисмутазы. В процессе базисной терапии отмечалось повышение активности супероксиддисмутазы и тенденция к снижению количества продуктов липопероксидации, что отражает процесс восстановления баланса между про- и антиоксидантной активностями плазмы крови. Этот факт указывает на эффективность стандартного лечения и в определенной степени на благоприятный исход заболевания.
Таким образом, при геморрагической лихорадке с почечным синдромом средней тяжести отмечается нарушение равновесия между процессами перекисного окисления липидов и активностью антиоксидантной защиты. Применение базисной терапии способствует нормализации показателей липопероксидации и ферментативного звена антиоксидантной системы. Для уточнения механизмов формирования окислительного стресса и оптимизации терапевтических подходов необходимы дальнейшие клинико-биохимические исследования.
Конфликт интересов
Финансирование
Библиографическая ссылка
Коваленко Е.Н., Зотова Л.В., Громова Е.В., Абрашина И.В., Павелкина В.Ф. ИССЛЕДОВАНИЕ ИЗМЕНЕНИЙ ПРОДУКТОВ ПЕРЕКИСНОГО ОКИСЛЕНИЯ ЛИПИДОВ И СОСТОЯНИЯ АНТИОКСИДАНТНОЙ СИСТЕМЫ ПРИ ГЕМОРРАГИЧЕСКОЙ ЛИХОРАДКЕ С ПОЧЕЧНЫМ СИНДРОМОМ // Современные проблемы науки и образования. 2026. № 3. ;URL: https://science-education.ru/ru/article/view?id=34506 (дата обращения: 10.06.2026).
DOI: https://doi.org/10.17513/spno.34506



