Введение
Гепатоцеллюлярная карцинома (ГЦК) - шестой по распространённости вид рака и третья по значимости причина смертности от онкологических заболеваний во всём мире. По оценкам Всемирной организации здравоохранения, в 2020 году было зарегистрировано 905677 новых случаев рака печени и 830 180 смертей от этого заболевания. Пятилетняя выживаемость при ГЦК составляет 18%, что указывает на неблагоприятный прогноз и ограниченность доступных методов лечения [1]. Выделение тяжести первичного рака печени имеет решающее значение, занимая шестое место по глобальной распространённости и третье по летальности [1]. Прогнозы предполагают 1,4 миллиона новых случаев и 1,3 миллиона смертных исходов к 2040 году [2].
Цирроз печени, вирусный гепатит, неалкогольная жировая болезнь печени (НАЖБП) или повреждения печени, вызванные алкоголем, - все это хронические заболевания, которые имеют тесную связь с патогенезом ГЦК. Ключевым фактором прогрессирования этих заболеваний до ГЦК является активация сигнального пути рецептора эпидермального фактора роста (EGFR). Семейство рецепторных тирозинкиназ ErbB, которое включает EGFR, необходимо для воспаления, клеточного деления и регенерации печени. При ГЦК экспрессия и гиперактивация EGFR тесно связаны с ростом опухоли, метастазированием и прогнозом пациента [3; 4].
ГЦК у человека обычно развивается на фоне активного воспалительного процесса при циррозе печени. Ежегодно у 1–4% пациентов с циррозом печени развивается ГЦК [5]. Цирроз печени может быть вызван различными причинами, такими как алкогольная болезнь печени, вызванная чрезмерным употреблением алкоголя, и стеатогепатит, связанный с нарушением обмена веществ, вызванный общим употреблением западной диеты, а также прогрессирующими формами алкогольного стеатогепатита и стеатогепатита, связанного с нарушением обмена веществ соответственно [6; 7]. Другими экзогенными факторами, которые могут вызывать хроническое воспаление печени, не обязательно приводящее к циррозу, являются инфекции, вызванные вирусами гепатита, такими как вирус гепатита В (HBV) и вирус гепатита С (HCV), а также такие факторы риска, как воздействие афлатоксинов, курение и генетическая предрасположенность.
По данным ФГБУ «НМИЦ радиологии» Минздрава России, за последнее десятилетие зарегистрирован рост заболеваемости первичными злокачественными новообразованиями печени и внутрипечёночных желчных протоков на 43,36%. Заболеваемость ГЦК в 2024 году в Российской Федерации – 7,47 случая на 100 тыс. населения [8].
Канцерогенез ГЦК
Развитие гепатоцеллюлярной карциномы - многоэтапный процесс, в его основе лежит длительное воздействие факторов риска, приводящее к аккумуляции молекулярных и клеточных нарушений. Длительная экспозиция вирусных, токсических и метаболических агентов изменяет активность внутриклеточных сигнальных каскадов и регуляторов транскрипции, что сопровождается перестройкой экспрессии генов в гепатоцитах и их последующей злокачественной трансформацией [9].
Воздействие тех или иных этиологических факторов ГЦК ассоциировано с активацией определённых сигнальных путей канцерогенеза и формированием уникального спектра геномных изменений. Молекулярные изменения нарушают контроль клеточного цикла, угнетают апоптоз и ускоряют пролиферацию трансформированных клеток, что способствует образованию первичного опухолевого узла [4].
Опухолевая прогрессия является следующим этапом гепатоканцерогенеза, для него характерно усиление злокачественного фенотипа, автономный рост и неоангиогенез, индуцируемый проангиогенными факторами, и эпителиально-мезенхимальный переход (ЭМП), при котором опухолевые клетки лишаются эпителиальных признаков, овладевают способностью передвигаться и ремоделировать внеклеточный матрикс, что обеспечивает инвазию в прилежащие ткани и формирование метастатических очагов [10].
Характеризуется гепатоцеллюлярная карцинома на молекулярном уровне выраженной гетерогенностью молекулярных изменений - результат скопления широкого спектра соматических мутаций, эпигенетических перестроек и нарушений сигнальной регуляции, вследствие воздействия разнообразных этиологических факторов. Именно эти механизмы определяют вариабельность профилей экспрессии генов при ГЦК [11].
Современные исследования демонстрируют, что ГЦК формируется через множество перекрещивающихся молекулярных каскадов, активация которых зависит от конкретного этиологического воздействия. При интеграции ДНК вируса гепатита B в геном клетки-хозяина синтезируются четыре вирусные мРНК, кодирующие семь белков [12], среди которых ключевое значение имеет полипептид HBx (≈17 кДа). Полипептид HBx преобразует активность сигнального пути Wnt/β-катенина, регулирует пролиферацию и апоптоз, усиливает транскрипционную активность NF-κB и одновременно угнетает TNFα-опосредованный апоптоз, что способствует выживанию трансформированных клеток. Индукции митохондриального стресса и повышению образования активных форм кислорода способствуют как ДНК HBV, так и РНК HCV, это способствует запуску стресса эндоплазматического ретикулума и развитию развёрнутого белкового ответа, сопровождающегося аутофагией, что поддерживает персистенцию вируса [13].
Вирус гепатита С является РНК-содержащим (в отличие от вируса гепатита В-ДНК-содержащий), в связи с чем его интеграция в геном вирусоносителя невозможен, чем и обусловлен опосредованный канцерогенез - влиянием вируса на дерегуляцию разных клеточных механизмов, включая усиление пролиферации гепатоцитов и стеатоз, индукцию вирусного воспаления и окислительного стресса, вызывающих геномные мутации и геномную нестабильность, а также путем повреждения митохондрий и индукции иммунного ответа хозяина. Развитие ГЦР на фоне гепатита С происходит только в цирротически измененной печени. Риск возникновения ГЦР у пациентов с HCV-индуцированным ЦП в 17 раз выше, чем в здоровой популяции, и составляет 1–4% в год (в японской когорте – до 8% в год) [14]. Для HCV-ассоциированной ГЦК характерна избыточная экспрессия ряда генов (MMP9, RPS5, KRT8, ATP5F1, IGFBP2, MAP3K5, CCND1, NFKB1, CFLAR, BCL2, Mcl-1, SOCE) и взаимодействие вирусных белков NS5A, E2, NV5a, NS5B с ключевыми сигнальными путями (RAF/MAPK/ERK, E2F1), что изменяет клеточный цикл, пролиферацию и апоптоз [15]. NV5a дополнительно ингибирует p53-зависимый контроль деления клеток.
Употребление алкоголя является третьей по значимости причиной ГЦК. Этанол увеличивает образование железо-индуцированных активных форм кислорода (АФК), нарушающих репарацию ДНК, а образующийся при метаболизме ацетальдегид ковалентно модифицирует белки и нуклеиновые кислоты, усиливая мутагенез [16]. При постоянном и увеличенном употреблении спирта происходит индукция цитохрома P450 2E1 (CYP2E1), которая приводит к чрезмерному производству активных форм кислорода (АФК) в периветозальной зоне печеночной дольки. АФК вызывают окислительный стресс, повреждение гепатоцитов и апоптоз. Ацетальдегид, основной токсический метаболит этанола, является высокореактивным мутагеном, который образует устойчивые соединения с ДНК, вызывает точечные мутации, подавляет репарацию ДНК и в условиях индуцированного CYP2E1 активирует про-канцерогены. Также алкоголь и его метаболиты активируют звёздчатые клетки печени (ЗКП), которые являются основным источником внеклеточного матрикса при печёночном фиброзе. Нарушение баланса между синтезом и деградацией внеклеточного матрикса приводит к чрезмерному накоплению коллагена и прогрессированию фиброза [16].
Процесс онкогенеза в контексте неалкогольного стеатогепатита (НАГС) многогранен и включает несколько этапов, включая различные метаболические характеристики и онкогенную активность. Развитие ГЦК на фоне НАСГ включает одновременную активацию сигнальных путей, вовлеченных в патогенез НАСГ. Это сложное взаимодействие между многочисленными путями приводит к сверхактивации проонкогенных механизмов при одновременном подавлении механизмов, подавляющих опухоль. Таким образом, более глубокое понимание молекулярных сигнальных путей, участвующих в развитии MASH-ГЦК, необходимо для выявления новых молекул-мишеней для терапевтических и профилактических стратегий.
В развитии ГЦК на фоне НАСГ можно выделить 3 отдельные стадии: предопухолевый процесс, онкогенез, состояние после образования опухоли. Первая стадия соответствует прогрессирующему НАСГ, а третья стадия характеризуется видимым ростом опухоли. На второй стадии в результате сильного стресса, пережитого на первой стадии, возникают генетические мутации. Эти мутации продолжают накапливаться, что в итоге приводит к образованию солидной опухоли на третьей стадии [17].
Генетические и эпигенетические нарушения при ГЦР
Современные методы высокопроизводительного секвенирования, включая полноэкзомный и полногеномный анализ, радикально расширили возможности изучения молекулярного ландшафта гепатоцеллюлярной карциномы (ГЦК) и других опухолей печени. Эти технологии позволяют выявлять широкий спектр соматических событий, преобладающих в патогенезе ГЦК: однонуклеотидные замены, изменения числа копий генов (амплификации, потери гетерозиготности), крупные хромосомные перестройки (делеции, дупликации, инверсии, транслокации), малые инсерции и делеции [10]. Мутационная нагрузка повышена на гены, кодирующие компоненты теломеразы, регуляторы клеточного цикла, модификаторы хроматина, а также элементы сигнальных каскадов Wnt/β-катенин и PI3K/Akt/mTOR, p53 [18].
В одном из крупных европейских исследований, проведенном совместно с медицинскими исследователями из Франции, Италии, Испании, при детальном анализе 243 парных образцов опухолевой и здоровой ткани выделено одиннадцать ключевых молекулярных путей, объединяющих регуляцию длины теломер, контроль клеточного цикла, дифференцировку гепатоцитов, эпигенетическую перестройку и ремоделирование хроматина, ответ на окислительный стресс, а также активацию внутриклеточных сигнальных каскадов TGF-β, PI3K/Akt/mTOR, Wnt/β-катенин, MAPK и JAK/STAT [19].
Эпигенетическая дерегуляция составляет особое место в развитии ГЦР. Для ГЦК описаны нарушения ковалентных модификаций гистонов, общее снижение уровня метилирования ДНК, гиперметилирование промоторов опухолевых супрессоров и перестройка экспрессии ферментов-модификаторов хроматина, микроРНК и длинных некодирующих РНК [20]. К хромосомной нестабильности приводит гипометилирование ДНК, что коррелирует с неблагоприятным прогнозом. К наиболее часто метилируемым при ГЦК относят гены опухолевых супрессоров p73, p53, и WT1, регуляторов клеточного цикла (E2F1, pRb, p27, p15, p21CIP1/WAF1, p16INK4a), а также эпителиального маркера E-кадгерина [20]. Эти изменения ассоциированы с прогрессированием заболевания и рассматриваются как потенциальные прогностические маркеры.
Изменение экспрессии генов при гепатоканцерогенезе
Определение дифференциально экспрессируемых генов (ДЭГ) является ключевым этапом полногеномного профилирования экспрессии. Для этого традиционно используют одномерные статистические подходы: Significance Analysis of Microarrays (SAM) или Linear Models for Microarray Data (LIMMA) при работе с кДНК-микрочипами; для данных РНК-seq - модели на основе отрицательного биномиального распределения, реализованные в DESeq, или эмпирические методы анализа цифровой экспрессии в пакете edgeR [21]. Систематическое изучение ДЭГ при канцерогенезе позволяет глубже понять вклад генетических и эпигенетических нарушений в формирование опухолевого фенотипа, что определяет растущий интерес к транскриптомным исследованиям при ГЦК.
По данным NGS-исследования и анализов гибридизации у пациентов с ГЦК ученые предлагают выделить два основных молекулярных класса: пролиферативный и непролиферативный. Характеристики пролиферативного варианта: активация каскадов Ras и mTOR, амплификация локуса FGF19 и частая ассоциация с инфекцией HBV.
В зависимости от молекулярно-генетических изменений выделяют две подгруппы: с преобладанием активации TGF-β-регулируемого пути и Wnt/β-катенина и с транскриптомным профилем клеток-предшественников гепатоцитов.
Характеристиками непролиферативного класса является низкий уровень дифференцировки, сосудистая инвазиея, экспрессия маркера гепатобластов EpCAM, гиперэкспрессия α-фетопротеина (АФП) и активация каскадов Notch и IGF2 и частая ассоциация с HCV-инфекцией или алкогольной болезнью печени, средняя или высокая степень дифференцировки, низкая секреция АФП и активация пути Wnt/β-катенина [10].
Цель исследования: оценить молекулярно-генетические особенности гепатоцеллюлярной карциномы методом NGS с последующим проведением корреляции с развитием рецидива и общей выживаемостью.
Материалы и методы исследования
В работу включены результаты молекулярно-генетических исследований 39 пациентов (соотношение пациентов мужского и женского пола составило 25:14), прооперированных по поводу ГЦР в рамках МНИОИ им. П. А. Герцена с 2010 по 2024 г. Медиана возраста составила 66 лет.
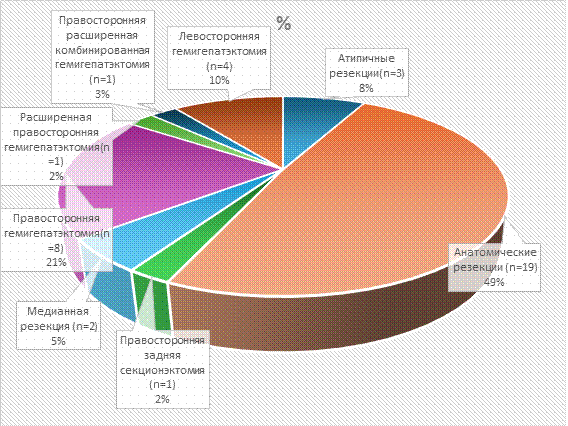
Рис. 1. Распределение пациентов по объемам хирургического вмешательства
Условные обозначения: n - количество пациентов в абсолютных числах
Примечание: составлено авторами по результатам данного исследования.
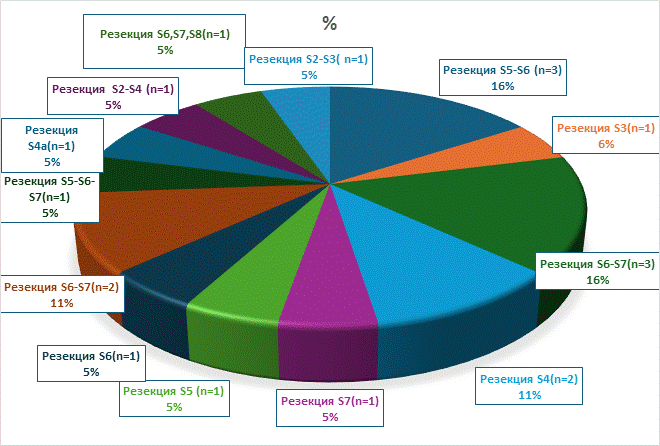
Рис. 2. Распределение пациентов по объемам анатомических резекций
Условные обозначения: n - количество пациентов в абсолютных числах
Примечание: составлено авторами по результатам данного исследования.
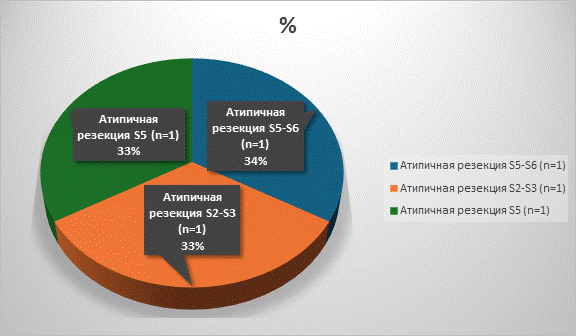
Рис. 3. Распределение пациентов по объемам атипичных резекций
Условные обозначения: n - количество пациентов в абсолютных числах
Примечание: составлено авторами по результатам данного исследования.
В исследование было включено 39 пациентов, которым были проведены хирургические вмешательства в следующих объемах: атипичные резекции - 3 (атипичная резекция S5-S6 сегментов - 1, атипическая резекция II-III сегментов печени - 1, атипичная резекция V сегмента печени - 1), анатомические резекции печени - 19 (резекция S5-S6 сегментов печени - 3, резекция 3-го сегмента печени - 1, резекция S6-S7-3, резекция S4 - 2, резекция S7 - 1, резекция S5 печени - 1, резекция S6 печени - 1, резекция S6-S7 печени - 2, резекция S5-S6-S7 печени - 1, резекция S4A сегмента печени - 1, резекция II-IVA сегментов печени – 1, резекция S6, S7, S8 cегментов печени - 1, резекция II-III сегментов печени - 1), правосторонней задней секционэктомии - 1, медианной резекции - 2, правосторонней гемигепатэктомии - 8, расширенной правосторонней гемигепатэктомии - 1, правосторонней расширенной комбинированной гемигепатэктомии - 1, левосторонней гемигепатэктомии - 4 (рис. 1-3).
В ходе приготовления библиотеки для секвенирования выяснилось, что достаточное количество и качество ДНК было получено из блоков только у 39 пациентов, которые и вошли в исследование. Распределение пациентом по TNM: pT1N0M0 - 6, pT3N0M0 - 9, pT2N0M0 - 12, pT1N0M0 - 2, pT1bN0M0 - 1, pT4N0M0 - 1, pT3bN0M0 - 1, pT2N1M0 - 1, pT2bN1M0 - 1, p T2cN0M0 - 1, ypT1bN0M0 - 1, pT3aN0M0 - 1, pT3bN0M0 - 2 пациента.
Для оценки молекулярно-генетических аспектов прогрессирования были экстрагированы ДНК из парафиновых блоков пациентов, прооперированных с 2010 по 2024 г.
Приготовление библиотек для высокопроизводительного
параллельного секвенирования
Соматическую ДНК выделяли из FFPE-образцов опухолевой ткани с использованием набора Qiagen QIAamp DNA FFPE Tissue Kit в соответствии с инструкцией производителя.
Библиотеки для секвенирования подготавливали с использованием набора VAHTS Universal Plus DNA Library Prep Kit v2 с ферментативной фрагментацией и последующим фракционированием по размеру. После лигирования адаптеров проводили PCR-амплификацию и нормализацию библиотек.
Таргетное обогащение и секвенирование
Таргетное обогащение выполняли с помощью панели Nanodigmbio NanOnco Plus Panel v3.0 (637 генов). Секвенирование проводили на платформе MGI в режиме парных чтений 2×100 п.н. Концентрацию ДНК измеряли флуориметрически с использованием Qubit dsDNA HS Assay Kit (Thermo Fisher Scientific). Чистоту оценивали спектрофотометрически с помощью Nanodrop.
Биоинформатическую обработку данных осуществляли с использованием стандартного пайплайна, схожего с GATK BestPractice (GATK, Broad Institute). Качество исходных прочтений оценивали с помощью FastP, после чего выполняли обрезку адаптерных последовательностей и низкокачественных. Полученные чтения выравнивали на референсный геном человека hg19 с помощью BWA-MEM2. Результирующие BAM-файлы обрабатывали путём маркирования дубликатов (STREAMMD), фильтрации и сортировки (Sambamba), а также выполняли рекалибровку качества оснований (BaseRecalibrator + ApplyBQSR, GATK).
Выявление соматических вариантов проводили с помощью Mutect2 в режиме анализа без герминального образца (single-sample mode), с применением панели нормальных образцов (Panel of Normals, PoN) и баз данных артефактов секвенирования для фильтрации ложноположительных результатов. Фильтрацию и аннотацию вариантов выполняли с использованием FilterMutectCalls (GATK) и инструментов аннотации (VEP, Opencravat).
Для повышения точности интерпретации результатов исключали варианты, расположенные в участках с низким качеством картирования (GQ <30, DP <20). Фильтрация по частотам популяционных баз данных (gnomAD) позволяла исключить вероятные герминальные полиморфизмы. Окончательная валидация клинически значимых находок проводилась экспертным пересмотром.
Результаты исследования и их обсуждение
В когорте из 39 пациентов с гепатоцеллюлярной карциномой были проанализированы мутации в панели из 637 онкогенов. В результате секвенирования и биоинформационного анализа выявлены соматические изменения в 95 различных генах.
По типам вариантов распределение оказалось следующим: миссенс-мутации (missense_variant) - 290 случаев; сдвиги рамки считывания (frameshift_variant) - 16 случаев; мутации, приводящие к преждевременному стоп-кодону (stop_gained) - 10 случаев; варианты в донорных сайтах сплайсинга (splice_donor_variant) - 9 случаев; варианты в акцепторных сайтах сплайсинга (splice_acceptor_variant) - 4 случая; инфрейм-делеции (inframe_deletion) - 6 случаев.
У 39 пациентов был проведён анализ мутационного профиля опухоли. Наиболее часто встречались мутации в генах GATA1 и ATRX, реже определялись изменения в NRG1, RANBP2, KDM6A, FAT1, PTEN, APC.
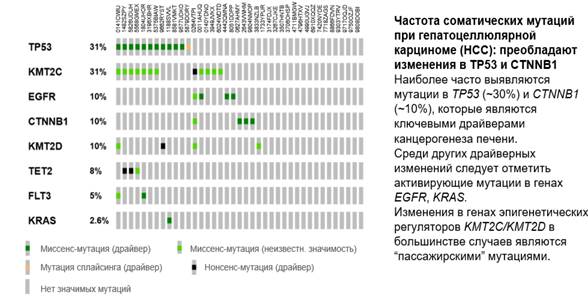
Рис. 4. Частота соматических мутаций при гепатоцеллюлярной карциноме
Инструкция по чтению онкопринта: строки (по вертикали) - отдельные гены (например, TP53, KMT2C, EGFR). Цифра справа от названия гена - доля пациентов, у которых выявлены изменения в этом гене (например, TP53 мутирован у 31% пациентов). Столбики (по горизонтали) - отдельные пациенты. Каждый столбик соответствует одному образцу.
Цвета внутри квадратиков - тип мутации:
○
Конфликт интересов
Благодарности
Финансирование
Библиографическая ссылка
Камалова М.А., Шегай П.В., Трифанов В.С., Шаталов П.А. МОЛЕКУЛЯРНО-ГЕНЕТИЧЕСКИЕ АСПЕКТЫ ПАТОГЕНЕЗА, РЕЦИДИВА ГЕПАТОЦЕЛЛЮЛЯРНОГО РАКА. ОПЫТ ПРОВЕДЕНИЯ СЕКВЕНИРОВАНИЯ НОВОГО ПОКОЛЕНИЯ У ПАЦИЕНТОВ С ГЕПАТОЦЕЛЛЮЛЯРНЫМ РАКОМ // Современные проблемы науки и образования. 2026. № 1. ;URL: https://science-education.ru/ru/article/view?id=34451 (дата обращения: 29.04.2026).
DOI: https://doi.org/10.17513/spno.34451



