Тотальное эндопротезирование тазобедренного сустава (ТЭТБС) является одной из самых успешных операций, выполняемых в последние десятилетия. Одним из наиболее часто используемых хирургических доступов при ТЭПТБС является прямой боковой (чрезъягодичный) по Хардингу. Этот доступ легко выполним, универсален, обеспечивает превосходную визуализацию вертлужной впадины и проксимального отдела бедра, позволяет адекватно ориентировать компоненты эндопротеза [1]. Его недостатком является необходимость отсечения передней части сухожилий средней и малой ягодичных мышц, что нередко приводит к послеоперационному нарушению функции абдукторов, проявляющемуся болевым синдромом и хромотой [2, 3]. В литературе описаны случаи отрыва передней порции сухожилий средней и малой ягодичных мышц от большого вертела в послеоперационном периоде после ТЭПТБС [4–6]. При этом у пациента отмечается положительный симптом Тренделенбурга.
Цель исследования: определить частоту возникновения недостаточности отводящего аппарата бедра после ЭПТБС из прямого бокового доступа и эффективность её лечения.
Материалы и методы исследования
В настоящее проспективное исследование были включены 883 пациента, которым было выполнено первичное тотальное эндопротезирование тазобедренного сустава на базе травматолого-ортопедического отделения НМИЦ ТО им Р.Р. Вредена за период с ноября 2010 г. по апрель 2016 г. по поводу идиопатического либо диспластического (Hartophylakidis A-B1) коксартроза. Из них 518 являлись женщинами и 365 – мужчинами. Средний возраст составил 57±15,8 лет. Во всех случаях применялся прямой боковой хирургический доступ по Хардингу. В послеоперационном периоде применялся стандартный протокол реабилитации, включавший обучение пациентов самостоятельной вертикализации и ходьбе с дополнительной опорой, а также упражнениям для последующих периодов реабилитации методистами ЛФК. Всем пациентам, включенным в исследование, была рекомендована ходьба с помощью костылей с дозированной нагрузкой на оперированную нижнюю конечность (до трети массы тела) в течение шести недель после операции, затем ходьба с помощью трости в течение трех месяцев.
На амбулаторном этапе проводилась клиническая оценка результатов ЭПТБС в срок три месяца после операции. Осмотр включал тест Тренделенбурга, оценку функционального статуса сустава по шкале Харриса, оценку наличия болевого синдрома и его выраженности по визуальной аналоговой шкале (ВАШ). При наличии данных за недостаточность отводящего аппарата пациенты получали рекомендации по консервативному лечению (ЛФК, ФТЛ), эффективность которого оценивалась в динамике на контрольных осмотрах в сроки 6 и 12 месяцев после операции.
При сохранении жалоб на хромоту положительного симптома Тренделенбурга к моменту контрольного осмотра в срок один год после ЭПТБС пациентам проводилось УЗИ области тазобедренного сустава. В случаях обнаружении сонографических признаков повреждения передней порции средней ягодичной мышцы (дефект сухожилия с участками кальцификации по передней поверхности большого вертела, скопление жидкости в области дефекта) при сохранной фиксации основной порции к вертелу предлагалась операция в объёме рефиксации сухожилий средней и малой ягодичных мышц. В итоге данное вмешательство было выполнено у пяти пациентов.
В ходе операции выполнялся доступ к проксимальному отделу бедренной кости по ходу послеоперационного рубца, проводилась визуальная и пальпаторная оценка повреждения отводящего аппарата. Далее выполнялась мобилизация передней порции средней и малой ягодичных мышц, удаление остеофитов области большого вертела при их наличии и механическая обработка склерозированной поверхности кости в зоне дефекта. Сухожилия рефиксировались к большому вертелу с использованием двух либо трех (в зависимости от размера дефекта) якорных фиксаторов 5,0 мм (Fastin, Jhonson & Jhonson), введенных в большой вертел у заднего края дефекта, с дополнительным подшиванием к сохранной порции сухожильного комплекса. После вмешательства иммобилизация не проводилась, пациенты вертикализировались в ранние сроки и получали рекомендацию ходить с помощью костылей с минимальной нагрузкой на оперированную нижнюю конечность в течение шести недель. Клиническую оценку результатов рефиксации абдукторов проводили через полгода с применением тех же методов.
Результаты исследования и их обсуждение
После эндопротезирования тазобедренного сустава в срок 3 месяца у 152 из 747 осмотренных пациентов (20,3 %) отмечался положительный симптом Тренделенбурга. Функциональный статус ТБС у этих пациентов в среднем оценивался как 62,9 SD = 29,3 (40–80) баллов по шкале Харриса. На боль в области ТБС предъявляли жалобы 30 % пациентов, интенсивность болевого синдрома в среднем составила 2,1; SD = 1,2 (1–4) баллов по ВАШ. При наличии жалоб на хромоту и боль в этот срок пациентам рекомендовалось консервативное лечение – ЛФК, ФТЛ, продолжение ходьбы с тростью.
Далее из 152 пациентов 120 были осмотрены повторно в срок 6 месяцев – из них положительный симптом Тренделенбурга сохранялся только у 30 (20 %) пациентов. Средний результат оценки по шкале Харриса у них составил 73,3; SD = 5,9 (62–83) балла, данные пациенты продолжили консервативное лечение.
Наконец, в срок 12 месяцев после ЭПТБС положительный симптом Тренделенбурга сохранялся у 5 пациентов из 28 осмотренных (17,9 %) Частота выявления признаков несостоятельности отводящего аппарата бедра в различные сроки наблюдения представлена в блок-схеме (рисунок).
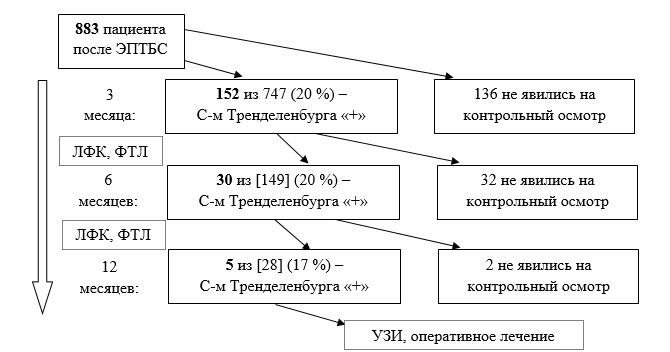
Частота выявления признаков несостоятельности отводящего аппарата бедра
У пяти пациентов, которым потребовалась рефиксация абдукторов бедра, сохранялись жалобы на хромоту, однако болевой синдром в области сустава их не беспокоил. Разность длин нижних конечностей в данной группе пациентов не превышала 1 см. Средняя оценка по шкале Харриса у них составила 79,6 (72–84) баллов (таблица).
|
Пациент |
Пол |
Возраст |
ИМТ |
Харрис до рефиксации (1 год после ЭПТБС) |
Харрис после рефиксации (+ прирост) |
Дополнительная опора после рефиксации |
Симптом Трeнделенбурга после рефиксации |
|
1 |
ж |
74 |
26,7 |
84 |
88 (+4) |
Трость |
Пол |
|
2 |
ж |
68 |
36,4 |
80 |
94 (+14) |
Нет |
Отр |
|
3 |
ж |
72 |
32,7 |
84 |
96 (+12) |
Нет |
Отр |
|
4 |
ж |
64 |
39,6 |
78 |
96 (+18) |
Нет |
Отр |
|
5 |
ж |
67 |
42,8 |
72 |
92 (+20) |
Нет |
Отр |
При УЗИ тазобедренного сустава была выявлена вышеописанная сонографическая картина и проведено оперативное лечение. Интраоперационная оценка отводящего аппарата во всех случаях соответствовала сонографической – отмечалась склерозированная поверхность «оголенного» участка большого вертела и ретрагированная передняя порция сухожилия средней ягодичной мышцы с рубцовым перерождением её края и явления бурсита с небольшим объемом (до 5 мл) серозного содержимого. Помимо этого, у одного из пациентов отмечались остеофиты по передне-боковой поверхности большого вертела, также видимые на предоперационной рентгенограмме. Во всех случаях дефект сухожилия в области большого вертела имел овальную форму с размерами в среднем 3,5±0,5 см в длину и 3±0,5 см в ширину.
При осмотре в срок 6 месяцев после рефиксации у четырех пациентов из пяти симптом Тренделенбурга был отрицательным, они ходили без хромоты и без дополнительной опоры. У одной пациентки сохранялись симптомы недостаточности отводящего аппарата, она использовала в качестве дополнительной опоры при ходьбе трость. Функциональный статус сустава поле рефиксации оценивался в среднем как 93,2 (88–96) балла по шкале Харриса, в среднем после повторного вмешательства результат увеличился на 13,6 (4–20) баллов (таблица). Никто из пациентов не предъявлял жалоб на болевой синдром к моменту осмотра.
Частота встречаемости дефицита функции отводящего аппарата бедра после ЭПТБС может варьировать в широких пределах вплоть до 20 % [7] и данная патология является сложной проблемой современной хирургии тазобедренного сустава [8]. Недостаточность абдукторов может клинически проявляться хромотой, положительным симптомом Транделенбурга и болью в области операции [8, 9], тем самым негативно отражаясь на общем функциональном статусе сустава и качестве жизни пациента [10]. Также она может быть ассоциирована с вывихами головки эндопротеза [7], помимо этого нарушение походки сопряжено с повышенным риском падений пациентов после операции [11].
Использование прямого бокового доступа (чрезъягодичного) в различных его модификациях традиционно считается связанным с повышенным риском недостаточности отводящего аппарата [2, 6, 10]. Первой из причин является возможность прямого интраоперационного повреждения ветвей верхнего ягодичного нерва и повышенный риск тракционного либо компрессионного повреждения при стоянии ретракторов [12], либо при манипуляциях с бедром. Так J. Chomiak с соавт. отметили, что данный доступ сопряжен с развитием электронейромиографических признаков частичной денервации m. gluteus medius в 81,8 % случаев и m. tensor fasciae latae в 48 % случаев [13], а по данным A.S. Baker с соавт. при прямом латеральном доступе в классическом исполнении наблюдалась денервация напрягателя широкой фасции в 10 случаях из 29 в раннем периоде (из них в 5 случаях нарушения сохранялись к сроку 3 месяца) [2].
Второй причиной следует считать собственно необходимость отсечения передней части общего сухожильного апоневроза m. gluteus medius и m. vastus lateralis с возможностью отрыва в месте рефиксации [4, 12]. Эффективность восстановления комплекса тканей, очевидно, может зависеть от качества ушивания на момент выполнения эндопротезирования [6], но при этом у лиц пожилого возраста, чаще у женщин [3], встречаются дегенеративные изменения отводящего комплекса, способные приводить к частичным и полным разрывам в условиях нативного сустава. В нашей серии наблюдений все пациенты, которым потребовалось повторное хирургическое лечение, были женщинами в возрасте 69±5 лет, в ряде других исследовании женщины также превалировали [4, 6].
Стоит отметить, что «золотым стандартом» визуализации повреждения отводящего аппарата бедра считается МРТ [3, 7]. Данный метод не только отличается высокой специфичностью касательно диагностики разрывов [7], но ещё предоставляет возможность градации жирового перерождения мышечной ткани, от степени которой в свою очередь зависит эффективность оперативного восстановления [3]. При этом, однако, МРТ является сравнительно дорогим методом исследования и получение информативной картины мягких тканей, находящихся радом с компонентом эндопротеза может быть сопряжено с дополнительными техническими требованиями [3]. К тому же МР-картина разрыва может не всегда коррелировать с клинической картиной [7], и по данным исследования O. Swensson и соавт. только расхождение краев сухожильного комплекса на большое расстояние (>2,5 см) связано с клиническими проявлениями [12]. В свою очередь УЗИ, на основании результатов которого формировались показания к оперативному лечению в нашем исследовании, можно считать более субъективным методом, и оно уступает МРТ в возможностях оценки жирового перерождения [3], но при этом УЗИ является более доступным методом исследования, позволяющим визуализировать крупный дефект, подлежащий хирургической коррекции.
В литературе описано большое количество различных хирургических методик коррекции недостаточности отводящего аппарата бедра, применяющихся в различных ситуациях в зависимости от степени перерождения m. gluteus medius, возможности низведения оторванного фрагмента к точке фиксации, состояния окружающих мышц, состояния большого вертела и наличия рецидивирующих вывихов [3, 7, 8]. Рефиксация порции отводящего аппарата к месту её изначального крепления, известная в англоязычной литературе под термином «direct repair», также представлена различными вариациями в зависимости от техники шва и выполнения дополнительной аугментации [4–9]. К сожалению, дизайн представленного исследования и количество наблюдений не предполагает анализа сравнительной эффективности использованной хирургической методики с анкерными фиксаторами. Однако мы можем отметить, что она является относительно простой, может снизить риск переломов большого вертела в сравнении с множественными трансоссальными швами и швами через костные туннели (что актуально для костной ткани со сниженной плотностью), не предполагает повреждения окружающих мягких тканей, не требует применения аллографтов и может обеспечивать адекватные клинические результаты при должном подборе пациентов.
Касательно подбора пациентов, следует отдельно отметить, что все пять пациентов, которым в нашем исследовании выполнялась рефиксация абдукторов, предъявляли жалобы на сохраняющуюся на фоне консервативного лечения хромоту, но боли в области сустава они в данный срок после эндопротезирования не отмечали. Эта особенность согласуется с заключением M. Weber и соавт., что пациенты с большей вероятностью будут удовлетворены результатом прямого восстановления абдукторов, если оно выполняется по поводу мышечной слабости как основной жалобы, а не болевого синдрома [6]. С другой стороны, S. Rajkumar с соавт. сообщают о стихании болевого синдрома у пациентов их группы после рефиксации в более поздние сроки после операции [5]. Патогенез болевого синдрома в области тазобедренного сустава может быть не всегда понятен, особенно после эндопротезирования, и в таких случаях целесообразно придерживаться расширенного протокола обследования, включающего МРТ, исключение перипротезной инфекции, патологии, вызванной трунион-коррозией или избыточным износом и других сопутствующих проблем [3]. Помимо этого нужно помнить, что сама слабость отводящего аппарата может быть проявлением не только повреждения сухожилий и мышц, но и следствием недостаточного офсета бедра либо нарушения позиции центра ротации [14].
Также заслуживает внимания отмеченный в представленном исследовании регресс симптоматики в динамике на фоне консервативного исследования у некоторых пациентов. Потеря ряда пациентов для дальнейшего наблюдения на амбулаторном этапе и отсутствие точных сведений об объеме получаемой терапии у всех пациентов не позволяют должным образом оценивать эффективность консервативного лечения, и доказательная база касательно эффективности различных вариантов физиопроцедур и медикаментозной терапии различных поражений абдукторов бедра на сегодняшний день ограничена [3]. Тем не менее касательно последствий эндопротезирования следует учитывать, что порция отводящего аппарата с сохранной фиксацией к большому вертелу сама по себе может обладать достаточной силой [6] и постепенно прогрессирующее расхождение сухожильного комплекса может быть компенсировано [12]. Также электронейромиографически выявленная денервация мышц может иметь преходящий характер [2], и с течением времени может быть достигнута реиннервация и компенсаторная активации оставшихся моторных волокон [13]. Наконец походка в послеоперационном периоде зависит не только от отводящего аппарата, но и от других групп мышц бедра, в частности разгибателей [15], имеющих свой потенциал к восстановлению. По мнению E. Kenanidis и соавт., оперативное лечение показано при полных разрывах сухожилий ягодичных мышц [3], также по данным исследования [4] выполнение рефиксации в более ранние сроки после эндопротезирования может быть сопряжено с лучшими результатами. При этом данные нашего исследования, а также наблюдения M. Weber и соавт. [6] свидетельствуют о целесообразности продолжения лечения и наблюдения в срок для года перед проведением расширенного обследования и решения вопроса об оперативном лечении.
Заключение
Недостаточность функции отводящего аппарата бедра после ЭПТБС из чрезъягодичного доступа встречается часто, но может разрешаться на фоне консервативного лечения в срок до одного года после операции.
В случае неэффективности проводимого восстановительного лечения мы рекомендуем выполнение УЗИ ТБС. При наличии сонографических признаков отрыва сухожилий средней и малой ягодичных мышц оперативное лечение в объеме рефиксации может обеспечивать восстановление ходьбы без хромоты и дополнительной опоры.
Библиографическая ссылка
Андреев Д.В., Гончаров М.Ю., Ефимов Н.Н. ВОССТАНОВЛЕНИЕ АБДУКТОРОВ БЕДРА ПОСЛЕ ТОТАЛЬНОГО ЭНДОПРОТЕЗИРОВАНИЯ ТАЗОБЕДРЕННОГО СУСТАВА // Современные проблемы науки и образования. 2021. № 3. ;URL: https://science-education.ru/ru/article/view?id=30943 (дата обращения: 06.05.2026).
DOI: https://doi.org/10.17513/spno.30943



