В результате внедрения современных технологий интенсивной терапии и реанимации в неонатологии ежегодно увеличивается число выживших недоношенных детей со сроком гестации менее 30 недель [1, 2]. Разработка новых подходов выхаживания и терапевтического ведения таких пациентов является весьма актуальной задачей, поскольку для недоношенных новорожденных характерен рост заболеваемости в неонатальном периоде. Для повышения эффективности выхаживания важно своевременно распознать тяжесть нарушений, происходящих в организме ребенка. Это позволит выбрать правильный режим лечения, снижающий риск возможных осложнений пациентов. Перинатальная патология у недоношенных детей характеризуется большей тяжестью и сочетанностью нарушений вследствие незрелости всех систем организма, развившейся на фоне отсутствия внутриутробного благополучия плода во время беременности [3, 4]. Это приводит к необходимости совершенствования методов оценивания состояния здоровья у таких детей.
В настоящее время накоплен огромный опыт в области моделирования биологических систем, в том числе в медицине. Такое моделирование основано на использовании различных направлений цифровых технологий, которые позволяют врачам независимо от уровня профессиональной подготовки принять правильное решение.
Многие модели успешно зарекомендовали себя и внедрены в лечебный процесс больниц, они являются дополнительным подспорьем для специалиста при принятии решения о выборе той или иной тактики лечения, а также позволяют оценивать имеющийся потенциал здоровья пациента [5]. Другие модели позволяют достоверно распознать возможность развития заболевания в будущем и привлечь дополнительное внимание лечащего врача к конкретному пациенту [6]. Поэтому для выбора оптимального метода выхаживания и реабилитации недоношенных детей важно дать объективный прогноз состояния их здоровья.
Целью исследования явилась разработка прогностического правила для методики прогнозирования в целях оценки степени тяжести состояния здоровья недоношенных новорожденных со сроком гестации менее 30 недель. В качестве инструментария для разработки методики были использованы методы многомерного статистического анализа.
Материалы и методы исследования
Для решения поставленной задачи проведена оценка анамнестических данных и результатов лечебно-диагностических процедур 29 недоношенных новорожденных со сроком гестации менее 30 недель при рождении. Наблюдение за пациентами и их обследование начинались непосредственно в родильном зале, а далее продолжались в отделении анестезиологии и реанимации (с палатами для новорожденных детей) ГУ «РНПЦ “Мать и дитя”», г. Минск. Средний гестационный возраст младенцев составил 28,25±1,03 недели. Масса тела при рождении составила 1094,48±205,63 г. Мальчиков было 15,00 (51,72%), девочек – 14 (48,27%). 20 (68,97%) новорожденных были от одноплодной беременности, 9 (31,03%) – от многоплодной. Через естественные родовые пути родился 1 (1/3,45%) ребенок, при абдоминальном родоразрешении – 28 (96,55%) младенцев (20 (68,97%) – при экстренном и 8 (27,58%) – при плановом родоразрешении). Все дети (29 (100,00%)) в родильном зале получили сурфактантзаместительную терапию в дозе 227,86±72,47 мг/кг. Среди основных клинических диагнозов отмечены следующие состояния: респираторный дистресс-синдром новорожденных, врожденная пневмония, инфекция, специфичная для перинатального периода неуточненная, врожденный сепсис, инфекция, специфичная для перинатального периода.
Проанализированы 20 показателей: анамнестические данные, кислотно-основное состояние (КОС) артериальной крови при рождении и первого дня жизни, спектроскопия в ближней инфракрасной области (Near-infrared spectroscopy, NIRS), респираторная поддержка новорожденного, гемодинамический статус и гидробаланс первых 24 часов жизни ребенка (табл. 1). Метод NIRS успешно применяется для оценки мозгового кровотока и объема крови в сосудах головного мозга как раннего предиктора перинатальных поражений центральной нервной системы у недоношенных новорожденных [7, 8]. Обследуемые пациенты нуждались в проведении респираторной поддержки. Время осмотра: для признаков P0 – P5 – в родильном зале, для признаков P6 – P19 – в первые 24 часа жизни.
Таблица 1
Анамнестические и лабораторные данные
|
Данные |
Признак |
Условное обозначение |
|
Анамнез |
Пол: ж – 0 , м – 1 |
P0 |
|
Масса при рождении (г.) |
P1 |
|
|
Беременность: 0 – одноплодная, 1 – многоплодная |
P2 |
|
|
Метод родоразрешения: 0 – через естественные родовые пути, 1 – плановое кесарево сечение, 2 – экстренное кесарево сечение |
P3 |
|
|
КОС |
pH |
P4 |
|
КОС |
Lac |
P5 |
|
NIRS |
crSO2 (среднее) |
P6 |
|
∆crSO2 (макс-мин)) |
P7 |
|
|
Пульсоксиметрия |
SpO2 MIN при проведении ИВЛ |
P8 |
|
Клиническое наблюдение |
Гемодинамический статус |
P9 |
|
КОС (артериальная кровь) |
pH MIN |
P10 |
|
pH MAX |
P11 |
|
|
pCO2 MIN |
P12 |
|
|
pCO2 MAX |
P13 |
|
|
pO2 MIN |
P14 |
|
|
pO2 MAX |
P15 |
|
|
ctO2 MIN |
P16 |
|
|
ctO2 MAX |
P17 |
|
|
p50 MIN |
P18 |
|
|
p50 MAX |
P19 |
Исследование включало в себя несколько этапов. Вначале необходимо у недоношенных детей найти число групп по степени тяжести состояния здоровья. Предварительная гипотеза состояла в том, что у недоношенных детей имеет место градация на две группы – «тяжелые» и «очень тяжелые». Необходимо было проверить справедливость предположения о двух уровнях степени тяжести. Здесь были использованы методы кластерного анализа данных [9]. На втором этапе была сформирована система информативных диагностических признаков. Эта процедура была выполнена с помощью дискриминантного анализа [10].
Важнейший этап – количественный прогноз степени тяжести состояния детей – осуществим с помощью логистической регрессии. Она удобна тем, что позволяет формировать хорошо интерпретируемый показатель степени тяжести в виде вероятности отнесения пациента к той или иной группе больных. Применительно к двум классам это выглядит следующим образом.
Дана обучающая выборка значений признаков 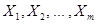
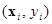 ,
, 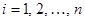 , (1)
, (1)
где 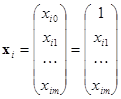 – вектор значений i-го объекта,
– вектор значений i-го объекта, 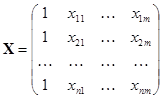 ;
; 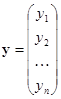 ,
, 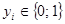 – бинарная переменная, указывающая на принадлежность i-го объекта соответствующему классу. Например, для определенности первому классу при
– бинарная переменная, указывающая на принадлежность i-го объекта соответствующему классу. Например, для определенности первому классу при 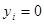 и второму – при
и второму – при 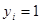 ; m – число признаков у каждого объекта; n – количество наблюдений. Классификация выполняется с помощью логистической функции [11]:
; m – число признаков у каждого объекта; n – количество наблюдений. Классификация выполняется с помощью логистической функции [11]:
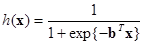 , (2)
, (2)
принимающей значения в интервале (0; 1). Пороговым значением является 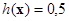 . Вектор
. Вектор 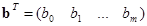 в (2) задает разделяющую линейную границу, описываемую уравнением гиперплоскости
в (2) задает разделяющую линейную границу, описываемую уравнением гиперплоскости 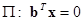 .
.
Введем функцию 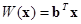 . Зададим область D 1 возможных значений x для первого класса как
. Зададим область D 1 возможных значений x для первого класса как 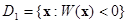 , а для второго класса – как
, а для второго класса – как 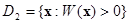 . Тогда
. Тогда 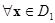
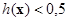 и
и 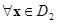
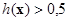 . Если x принадлежит гиперплоскости Õ, то
. Если x принадлежит гиперплоскости Õ, то 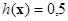 . Следовательно, для произвольного наблюдения x* вероятность его отнесения к первому классу равна
. Следовательно, для произвольного наблюдения x* вероятность его отнесения к первому классу равна 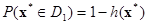 , а ко второму –
, а ко второму – 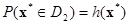 .
.
Для оценивания вектора коэффициентов b был использован алгоритм Ньютона–Рафсона [12]. Представляет интерес также исследование системных свойств каждой из групп пациентов с помощью энтропийного моделирования [6, 13].
Методы многомерного статистического анализа реализованы с помощью статистического пакета программ Statistica. Энтропийное моделирование выполнялось с помощью программы вычисления энтропии случайного вектора [14].
Результаты исследования и их обсуждение
Для уточнения числа групп недоношенных детей по степени тяжести состояния здоровья был использован традиционный в таких задачах кластерный анализ данных. Дендрограмма (рис.) наглядно показывает наличие двух выраженных кластеров.
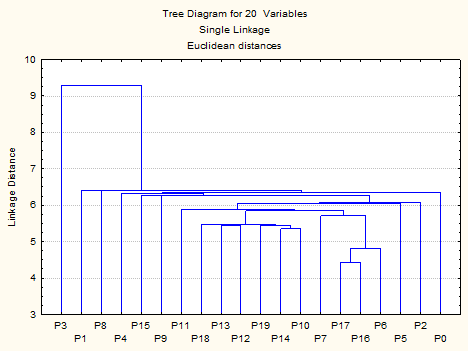
Дендрограмма
Слева на рисунке приводится расстояние между объединяемыми на данном этапе кластерами (объектами), внизу указаны признаки. С учетом результатов кластерного анализа все пациенты (n=29) были разделены на две группы: к группе «тяжелые» (D1) отнесены 17 пациентов, к группе «очень тяжелые» (D2) отнесены 12 пациентов.
Решение задачи состоит в попытке различить между собой группы пациентов D1 и D2 и в случае успеха построить решающее правило классификации. Для этого нужно было решить задачу многомерной классификации (распознавания) двух групп (кластеров) по показателям анамнестических данных и результатов лечебно-диагностических процедур. Суть решения состояла в нахождении такой совокупности показателей из исходного множества, которая позволила бы (если это в принципе возможно) статистически достоверно распознать различия в этих группах. Данная задача решалась в два этапа. На первом этапе с помощью дискриминантного анализа формировалась система информативных признаков, а на втором с помощью логистической регрессии строилось решающее правило классификации. Строилась дискриминантная функция с минимальным p-уровнем, который составил 0,0004. Информативными признаками явились следующие качественные и количественные показатели: X1 – масса тела ребенка при рождении в граммах; X2 – метод родоразрешения (0 – через естественные родовые пути, 1 – плановое кесарево сечение, 2 – экстренное кесарево сечение); X3 – pH КОС при рождении, X4 – уровень лактата крови КОС при рождении, X5 – минимальная SpO2 при проведении искусственной вентиляции легких, зафиксированная за первые 24 часа жизни, X6 – гемодинамический статус (0 – нет терапии; 1 – допамин ≤ 5 мкг/кг мин; 2 – допамин > 5 и ≤ 10 мкг/кг мин; 3 – допамин > 10 мкг/кг мин или допамин+добутамин ≤ 10 мкг/кг мин; 4 – допамин+добутамин > 10 мкг/кг мин; 5 – эпинефрин или норэпинефрин и/или глюкокортикостероиды; X7 – минимальное значение общего содержания кислорода (ctO2) крови КОС первых 24 часов жизни; X8 – максимальное значение ctO2 крови КОС первых 24 часов жизни; X9 – минимальное значение парциального давления кислорода (p50) крови КОС первых 24 часов жизни.
Распознавание двух групп (D1) и (D2) выполнено формально недостаточно достоверно, поскольку признаки pH крови КОС при рождении и p50 крови КОС первых 24 часов жизни имеют недостаточную статистическую надежность (менее 95%). Однако расчетное значение F-статистики статистически значимо со статистической надежностью 0,9996 (выше требуемой величины 0,95). Данные спектроскопии в ближней инфракрасной области (NIRS) оказались неинформативными показателями для решения поставленной задачи. Средняя вероятность правильного распознавания составила 96,552%, что выше требуемой величины 95%. Это означает, что сформированная система признаков в достаточной степени различает «тяжелых» и «очень тяжелых» пациентов.
Решающее правило построено по обучающему множеству признаков X0 и Y0, которое образуют пациенты с известными диагнозами. Решающее правило предназначено для классификации состояний новых пациентов.
Учитывая существенные признаки, полученные ранее с помощью дискриминантного анализа, мы рассчитали интегративный прогностический индекс (ИПИ) по формуле:
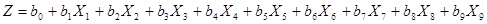 , (4)
, (4)
где b0 = –11,591, b1 = 9,333 b2 = 6,808, b3 = –3,056, b4 = –14,060, b5 = 13,964, b6 = –11,353, b7 = 19,082, b8 = –18,484, b9 = –5,997.
Если рассчитанный по прогностическому правилу (4) результат будет меньше нуля, то у ребенка прогнозируется «очень тяжелое» состояние с вероятностью 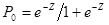 . Если результат Z будет больше нуля, то у ребенка прогнозируется «тяжелое состояние» с вероятностью
. Если результат Z будет больше нуля, то у ребенка прогнозируется «тяжелое состояние» с вероятностью 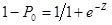 .
.
Все пациенты правильно классифицированы. В таблице 2 приведены результаты распознавания. Здесь обозначены: № – номер наблюдения (порядковый номер ребенка в общей выборке; IND – принадлежность наблюдений к одной из групп (IND=0 – группа «тяжелые», IND=1 – группа «очень тяжелые»); P0 – вероятность отнесения наблюдения (ребенка) к группе «очень тяжелые» (IND=1); 1 – P0 – вероятность отнесения наблюдения (ребенка) к группе «тяжелые» (IND=0).
Таблица 2
Вероятности отнесения пациентов к группам «тяжелые» и «очень тяжелые»
|
№№ |
IND |
Z |
P0 |
1 – P0 |
№№ |
IND |
Z |
P0 |
1 – P0 |
|
1 |
1 |
–37,233 |
1,00000 |
0,00000 |
16 |
1 |
–9,655 |
0,99994 |
0,00006 |
|
2 |
1 |
–23,257 |
1,00000 |
0,00000 |
17 |
0 |
36,913 |
0,00000 |
1,00000 |
|
3 |
0 |
8,145 |
0,00029 |
0,99971 |
18 |
0 |
17,338 |
0,00000 |
1,00000 |
|
4 |
0 |
7,214 |
0,00074 |
0,99926 |
19 |
0 |
5,414 |
0,00443 |
0,99557 |
|
5 |
1 |
–27,895 |
1,00000 |
0,00000 |
20 |
0 |
16,257 |
0,00000 |
1,00000 |
|
6 |
1 |
–7,465 |
0,99943 |
0,00057 |
21 |
0 |
10,433 |
0,00003 |
0,99997 |
|
7 |
1 |
–5,686 |
0,99662 |
0,00338 |
22 |
0 |
32,437 |
0,00000 |
1,00000 |
|
8 |
0 |
6,101 |
0,00224 |
0,99776 |
23 |
0 |
21,573 |
0,00000 |
1,00000 |
|
9 |
0 |
25,104 |
0,00000 |
1,00000 |
24 |
1 |
–36,413 |
1,00000 |
0,00000 |
|
10 |
0 |
8,310 |
0,00025 |
0,99975 |
25 |
0 |
5,734 |
0,00322 |
0,99678 |
|
11 |
0 |
36,550 |
0,00000 |
1,00000 |
26 |
1 |
–30,228 |
1,00000 |
0,00000 |
|
12 |
1 |
–5,974 |
0,99746 |
0,00254 |
27 |
0 |
16,309 |
0,00000 |
1,00000 |
|
13 |
0 |
10,513 |
0,00003 |
0,99997 |
28 |
0 |
22,199 |
0,00000 |
1,00000 |
|
14 |
1 |
–7,951 |
0,99965 |
0,00035 |
29 |
1 |
–47,549 |
1,00000 |
0,00000 |
|
15 |
1 |
–30,438 |
1,00000 |
0,00000 |
– |
– |
– |
– |
– |
Результаты энтропийного анализа по статистически значимым признакам приведены в таблице 3. Видно, что в группе «очень тяжелые» по сравнению с группой «тяжелые» энтропии хаотичности и самоорганизации меньше. Это означает, что в целом у «очень тяжелых» пациентов в целом вариация показателей, их изменчивость ниже, а теснота взаимосвязи между показателями выше.
Таблица 3
Результаты энтропийного анализа групп «тяжелые» и «очень тяжелые»
|
IND |
Энтропия хаотичности HV |
Энтропия самоорганизации HR |
Общая энтропия H |
|
0 |
11,108 |
–2,732 |
8,376 |
|
1 |
10,411 |
–3,803 |
6,609 |
Заключение
Использование методов многомерного статистического анализа позволило разработать алгоритм оценки степени тяжести недоношенных детей. Достоверность классификации выборки пациентов по полученному разделяющему правилу составила 100%. Это позволяет использовать данное решающее правило для создания методики в целях прогнозирования степени тяжести состояния недоношенных новорожденных со сроком гестации менее 30 недель. Использование доступных анамнестических, а также лечебно-диагностических данных дает возможность имплементировать разработанное правило после его апробации в практическую деятельность неонатальных отделений интенсивной терапии различных уровней оказания перинатальной помощи, что явится дополнительным критерием для врача при оценке степени тяжести новорожденного пациента и дальнейшем выборе персонифицированной тактики терапевтических манипуляций и медикаментозного лечения.
Благодарности. Работа выполнена при поддержке совместного российско-белорусского проекта РФФИ (грант № 20-51-00001) и БРФФИ (грант № М20Р-008).
Библиографическая ссылка
Тырсин А.Н., Улезко Е.А., Остроушко Д.В., Свирская О.Я., Санковец Д.Н. ПРОГНОЗИРОВАНИЕ СТЕПЕНИ ТЯЖЕСТИ СОСТОЯНИЯ НЕДОНОШЕННЫХ НОВОРОЖДЕННЫХ СО СРОКОМ ГЕСТАЦИИ МЕНЕЕ 30 НЕДЕЛЬ // Современные проблемы науки и образования. 2020. № 6. ;URL: https://science-education.ru/ru/article/view?id=30288 (дата обращения: 15.05.2026).
DOI: https://doi.org/10.17513/spno.30288



