Биологические мембраны очень уязвимы к воздействию на них тяжелых металлов, в связи с этим на сегодняшний день актуальны исследования влияния ионов тяжелых металлов на живые объекты.
По данным литературных источников, загрязнение окружающей среды различными соединениями кобальта и кадмия происходит попаданием данных тяжелых металлов в атмосферу вместе с промышленной пылью, продуктами некоторых производств (стекольная, цементная и металлургическая промышленность, производства аккумуляторов, содержащих кадмий). Наибольшему риску воздействия данных металлов и их соединений подвержены работники вышеупомянутых производств. Наибольший процент тяжелых металлов попадает в организм человека через дыхательные пути, а также через ЖКТ, откуда вследствие абсорбции проникает в кровяное русло. Воздействие растворимых соединений кобальта приводит к повышению концентрации металла в крови и моче. Кадмий циркулирует в крови, главным образом в связанном состоянии в эритроцитах [1-3].
Механизм токсического действия кадмия заключается в том, что он связывает все серосодержащие аминокислоты и ферменты, при этом поражаются цитоплазма и ядра клеток. При интоксикации кадмием происходит поражение ЦНС, печени и почек, а также нарушается фосфорно-кальциевый обмен, что приводит к разрушению костей и развитию анемии.
Токсичность кобальта связывают с инактивацией тиоловых групп (например, липоевой кислоты) в тканях. Для человека наиболее высокой токсичностью обладают растворимые соли: карбонат кобальта, хлорид кобальта, а также металлический кобальт [4]. Избыток кобальта в организме проявляется в виде кровотечений, отёка лёгких, нарушений работы щитовидной железы, повышения кровяного давления, ухудшения работы нервной системы и сердечной мышцы.
М.О. Трусевич в своих исследованиях доказал, все тяжелые металлы в концентрации свыше 0,008 мМ оказывают токсическое воздействие на устойчивость мембран эритроцитов [5].
Устойчивость эритроцитов к различным повреждающим действиям, характеризующаяся совокупностью физико-химических свойств клеток, во многом зависит от их состояния. Так, в норме мембрана клеток крови устойчива к окислительному стрессу. Это достигается как за счет структурной организации мембраны, так и за счет наличия в ней липофильных антиоксидантов. Установлено, что устойчивость эритроцитов к окислительному гемолизу является показателем индуцибельности перекисного окисления мембранных фосфолипидов [6].
Способность эритроцитов к гемолизу под действием гемолитических веществ используется в качестве критерия, определяющего стойкость клеток. При этом величиной для оценки стойкости служит время гемолиза. Время гемолиза эритроцитов находится в прямой зависимости от концентрации гемолитического агента. Неорганические кислоты в ряду гемолитиков являются наиболее стабильными. Именно поэтому стойкость эритроцитов к кислотному гемолитику является важнейшим критерием, который связан с их физиологическим состоянием и возрастом, а также отражает состояние мембраны клетки. Известно, что гемолиз эритроцитов человека, вызываемый 0,002М раствором HCl, в норме протекает от 6 до 8 минут.
Цель исследования: изучение влияния солей кобальта и кадмия на кислотную устойчивость эритроцитов, а также сравнение оказываемых эффектов.
Материалы и методы исследования
Суть методики исследования кислотной резистентности заключается в фотометрической регистрации кинетики лизиса эритроцитов под действием кислот, построении кислотных эритрограмм резистентности.
Принцип метода эритрограмм заключается в фотометрической регистрации кинетики лизиса эритроцитов под действием 0,002 или 0,001 н НСl при длине волны 670 нм [7].
В качестве реактивов нами использовался физиологический раствор NaCl 0,9%; соляная кислота (НСl) 0,001 и 0,002 н. Для проведения исследования использовали центрифугу и фотоэлектроколориметр.
В ходе исследования в одну из кювет вносили физиологический раствор, относительно которого и производились измерения во второй кювете, в которую помещали 1,5 мл 0, 002 н раствор НСl и 0,7 мл 1% суспензии эритроцитов. Далее производились измерения оптической плотности на КФК при длине волны 670 нм взвеси эритроцитов с интервалом 10–30 секунд до тех пор, пока не будет зафиксировано окончание гемолиза. Затем выполнялись все необходимые расчеты по методу химических (кислотных) эритрограмм, описанному И.А. Терсковым, И.И. Гительзоном. В опытные образцы дополнительно были добавлены соли кобальта и кадмия с концентрацией 1 мМ [8].
Протекание гемолиза графически было изображено нами в виде временной зависимости, отражающей нарастающий процент гемолизированных эритроцитов. Построенная интегральная эритрограмма имела S-образный вид.
Достоверность полученных результатов оценивалась с помощью t-критерия Стьюдента.
Результаты исследования и их обсуждение
В ходе исследования нами были получены значения, характеризующие изменения процента гемолиза с течением времени при воздействии солей кобальта и кадмия на мембраны эритроцитов.
Анализируя данные, мы установили, что в контрольном образце гемолиз достигает 100% через 8 минут. Увеличение каждого последующего значения происходит в небольшом диапазоне величин.
В образце, содержащем ацетат кобальта, наибольшее возрастание показателей происходит на 210-й и 360-й секунде в 5 раз и 76% соответственно. Уменьшение данных показателей отмечаются на 30; 60; 90; 150; 240; 330 и 390-й секунде на 7,5%; 15%; 9%; 9%; 13%; 8% и 9%. Полный гемолиз происходит через 7 минут, что на 1 минуту раньше, чем в контрольном образце.
При воздействии на эритроциты сульфата кобальта отмечается уменьшение процента гемолиза в сравнении с предыдущими показаниями на 120-й секунде на 16,4%. В остальных случаях наблюдается повышение значений, наибольшее из которых составляет 23% и происходит на 30-й секунде. Гемолитические процессы достигают максимума через 4 минуты после начала исследования, что на 4 минуты ранее, чем в контрольном образце.
В образце с оксидом кобальта наибольшее повышение процента гемолиза в сравнении с предыдущими показателями происходит на 20; 30; 60 и 90-й секундах на 48%; 52%; 66,7% и 29,5%. Наименьшее повышение этих значений происходят с 300-й по 450-ю секунду. Снижение на 1,7% зафиксировано на 420-й секунде. Процесс гемолиза останавливается через 8 минут, как и в контрольном образце.
При воздействии хлорида кобальта полный гемолиз происходит через 2 минуты, что на 5 минут ранее контрольного образца, это говорит о высокой токсичности данного соединения. На 20-й и 30-й секунде отмечается уменьшение показателей гемолиза в 2 и 4 раза соответственно. На протяжении всего оставшегося времени наблюдается увеличение процента гемолизированных клеток и наибольшее повышение зафиксировано на 60-й секунде и составляет 1,5 раза.
В образце с нитратом кобальта наблюдается равномерное постепенное увеличение процента гемолиза с течением времени и в целом составляет 4%. Процесс достижения полного гемолиза занимает 3,5 минуты, что на 4,5 минуты раньше, чем в контрольном образце.
Для визуализации данных нами был построен график, на котором отображен процент гемолизированных эритроцитов в зависимости от времени, прошедшего после добавления в образцы раствора HCl (рис. 1).
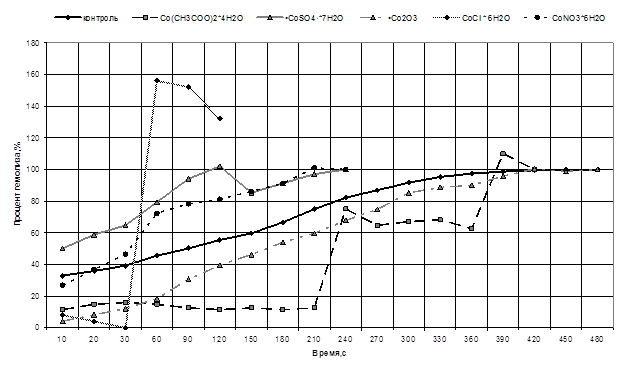
Рис. 1. Интегральная кислотная эритрограмма устойчивости эритроцитов в отношении солей кобальта
В результате исследований кислотной резистентности эритроцитов установлено, что наибольшие повреждения мембране наносят соли хлорида кобальта, так как полный гемолиз достигается на 6,5 минут раньше, чем в норме, что говорит о высоком повреждающем действии на устойчивость мембраны к воздействию кислот. Наименее токсичным оказалось соединение оксида кобальта, при воздействии данного соединения 100% гемолиз происходит через такой же промежуток времени, что и в контрольном образце.
В образце с ацетатом кадмия гемолитические процессы завершаются через 1,5 минуты, что на 6,5 минут быстрее, чем в норме. Наибольшее повышение показателей гемолиза в сравнении с предыдущими происходит главным образом на 30-й и 60-й секунде на 11% и 10% соответственно. В образце с сульфатом кадмия 100% гемолиз достигается через 5 минут, что на 3 минуты раньше контрольного. Наибольшее повышение показателей гемолиза зафиксировано на 20-й секунде на 33,5%, а наименьшее – на 180-й и 210-й секундах на 1,3%.
При воздействии на эритроциты оксидом кадмия гемолиз достигает максимальных значений через 8,5 минут, что на 0,5 минуты позднее, чем в контрольном образце. Наибольшее увеличение показателей гемолиза установлено в интервале от 20-й до 60-й секунды и в среднем составляет 40%. Наименьшее же увеличение зафиксировано во временном интервале с 360-й по 480-ю секунду.
В образце с хлоридом кадмия установлено, что 100% гемолиз достигается через 9,5 минут, что на 1,5 минуты позднее контрольного образца. Наибольшее повышение процента гемолиза в 1,3 раза установлено на 30-й секунде.
Для визуализации полученных данных нами был построен график оценки кислотной резистентности эритроцитов в отношении солей кадмия с учетом уровня диссоциации соединений (рис. 2).
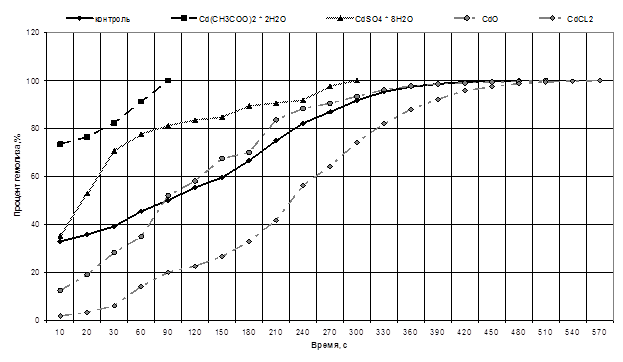
Рис. 2. Интегральная кислотная эритрограмма устойчивости эритроцитов в отношении солей кадмия
Анализируя данные, представленные на рисунке 2, установлено, что наибольшей токсичностью обладает ацетат кадмия, при воздействии которого 100% гемолиз происходит на 6,5 минут ранее, чем в контрольном образце. Наименьшим токсическим действием на кислотную устойчивость мембран эритроцитов характеризуются хлорид и оксид кадмия, так как полный гемолиз происходит позднее, чем в контрольном образце.
Для сравнения эффектов, оказываемых на мембрану солями Co и Cd, нами был построен график оценки кислотной устойчивости эритроцитарных мембран в отношении солей данных тяжелых металлов (рис. 3).
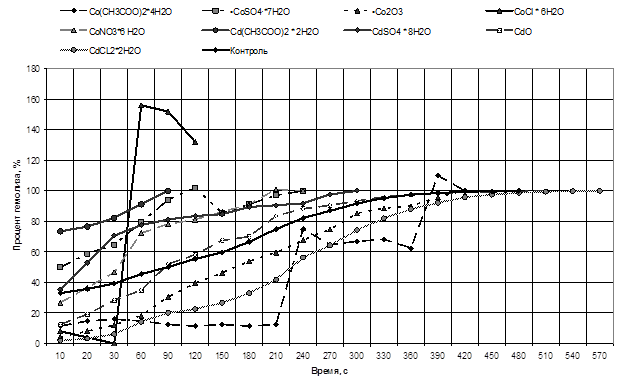
Рис. 3. Оценка кислотной резистентности эритроцитов в отношении солей кадмия и кобальта с учетом уровня диссоциации соединений. Интегральная эритрограмма
Анализируя данные рисунка 3, мы пришли к выводу, что наибольшим повреждающим эффектом на устойчивость мембран эритроцитов в отношении кислот обладает соль Cd(CH3COO)2×2H2O, поскольку данный образец достигает 100% гемолиза за 1,5 минуты, что на 6,5 минут ранее контрольного образца, и это говорит о низкой устойчивости мембран при воздействии ацетата кадмия.
Заключение
В ходе выполнения экспериментальных исследований по оценке влияния катионов кобальта и кадмия в составе солей с различными анионными компонентами нами было установлено, что наименьшим токсическим действием обладает хлорид кадмия, так как процесс гемолиза прекращается через 9,5 минут, что на 1,5 минуты позднее контрольного образца. Также наименьшим токсическим эффектом на устойчивость мембран эритроцитов к кислотам обладают оксиды кобальта и кадмия, что, на наш взгляд, связано с низким уровнем диссоциации данных соединений.
Библиографическая ссылка
Сизенцов А.Н., Филончикова Е.С., Быкова Л.А., Сальникова Е.В., Бибарцева Е.В., Побегайлова И.Г. ИЗУЧЕНИЕ ВЛИЯНИЯ РАЗЛИЧНЫХ СОЛЕЙ КОБАЛЬТА И КАДМИЯ НА КИСЛОТНУЮ УСТОЙЧИВОСТЬ ЭРИТРОЦИТОВ // Современные проблемы науки и образования. 2018. № 6. ;URL: https://science-education.ru/ru/article/view?id=28300 (дата обращения: 10.05.2026).



