Скоординированная походка требует согласованного функционирования костно-мышечной и центральной нервной системы, поэтому тест «туннель» (footprint test), который позволяет оценить моторную активность животного по отпечаткам лап, широко применяется в экспериментах in vivo, моделирующих различные заболевания человека, связанные с повреждением центральной нервной системы [1, 2]. Однако данный тест не получил широкого распространения при изучении особенностей старения. Ограниченный набор регистрируемых параметров существующих модификаций теста не позволил выявить значимых возрастных изменений походки [3, 4], поэтому в исследованиях, посвященных изучению процесса старения, авторы стремятся расширить набор измеряемых показателей [5]. В связи с этим представляет интерес новая интерпретация теста «туннель», которая могла бы кардинально расширить спектр регистрируемых параметров и выявить различия в походке у молодых и старых мышей стандартных и оригинальных линий, проявляющих признаки нейродегенеративных заболеваний в старости.
Тест «туннель» неинвазивен и информативен, что позволяет применять его не только в кроссекциональных, но и в лонгитюдных исследованиях. Иногда исследователи используют сложную аппаратуру для фиксации отпечатков лап мыши (или крысы) и силы нажима во время ходьбы [1], но чаще только анализируют следы, оставленные окрашенными лапами животного на бумаге [2, 6, 7]. Как правило, изучают отпечатки передних и задних лап и оценивают перекрытие этих следов между собой; иногда ограничиваются только следами задних лап [8]. Набор измеряемых параметров теста в каждой модификации свой, но в нем неизменно присутствуют длина шага левых и правых задних и/или передних лап и ширина постановки лап при ходьбе. Иногда авторы сообщают, что для измерения этих параметров используют линейку [2], реже – специально написанное приложение [8]. Шаткость походки при изучении особенностей старения (в том числе вызванную нейродегенеративными заболеваниями), не всегда заметную при визуальном наблюдении, трудно оценить количественно на основании перечисленных показателей.
Ранее мы показали, что у самок мышей оригинальной инбредной линии CBRB в возрасте 80 недель и старше постепенно развивается ряд симптомов паркинсонизма [9, 10], аналогичных соответствующим проявлениям паркинсонизма у пациентов с болезнью Паркинсона (брадикинезия, экстрапирамидная мышечная ригидность, тремор покоя с последующей постуральной неустойчивостью [11]). Самцы этой линии, как правило, не доживают до возраста проявления этой симптоматики [9, 10]. Даже при явном проявлении тремора покоя задних конечностей у мышей CBRB признаки постуральной неустойчивости, очевидно, не так заметны. Возможно, поэтому не встречается описаний выявления признаков постуральной неустойчивости в мышиных моделях.
Целями работы были создание новой модификации теста «туннель» (footprint test), которая, сохраняя спонтанность поведения мыши и учитывая значимость каждого шага, позволит оценить изменения походки, связанные как с процессом старения, так и с симптомами паркинсонизма, а также разработка программного обеспечения, позволяющего расширить спектр регистрируемых параметров.
Материалы и методы исследования. Работа выполнена на молодых и старых самках мышей линий CBRB-Rb(8.17)1Iem с гомозиготной транслокацией Робертсоновского типа на генетической основе мышей линии CBA/CaLаc [9, 10] и стандартной линии BALB/cJCitMoise (BALB/c) из коллекции Е.В. Моисеевой в ИБХ РАН. Мышей содержали по 6–10 особей в клетках в конвенциональных (не-СПФ) условиях при естественном освещении, температуре 22–25оC, влажности 40–60%, кормили полноценными гранулированными кормами, в качестве стандартной подкормки использовали зерновые каши с подсолнечным маслом и витаминами A, E, D, F; воду предоставляли без ограничений.
В экспериментах использовали интактных мышей без предварительного обучения (табл. 1). Старых мышей линии CBRB разделили на две подгруппы по отсутствию (тремор–) или наличию (тремор+) тремора задних конечностей. Исследования всегда проводили в промежутке времени между 18:00 и 22:00 часами. Для проведения теста мышам окрашивали ступни обеих задних лап крахмальным клейстером с добавлением красителя с антисептическим действием (бриллиантового зеленого или фукорцина). Затем животных запускали в цилиндрический туннель длиной 225 мм и диаметром 43 мм, на нижней внутренней стороне которого находилась полоска белой бумаги (70 х 290 мм). В результате проведения теста получали не менее семи четких следов; время прохождения туннеля фиксировали для вычисления средней скорости движения мыши в туннеле (мм/с).
Таблица 1
Экспериментальные группы мышей
|
Линия |
CBRB |
BALB/c |
|||
|
Группа |
Подгруппа |
Количество, шт. |
Возраст, недель |
Количество, шт. |
Возраст, недель |
|
Молодые |
|
15 |
8–13 |
15 |
8–11 |
|
Старые |
Тремор– |
10 |
88–97 |
12 |
85–104 |
|
Тремор+ |
19 |
88–97 |
– |
– |
|
Для обработки полученного массива данных нами была написана программа RecognitionOfSteps.exe [12] (рис. 1A). Полоски бумаги с отпечатками лап мышей были отсканированы в формате JPG и отражены по вертикали (на одном из образцов с помощью линейки измеряли в миллиметрах фактическое расстояние между двумя произвольными следами). Файлы, подготовленные таким образом, открывали в программе RecognitionOfSteps.exe. На основании фактического расстояния между парой отпечатков лап производили калибровку изображения. Затем, для введения в программу координат следов, отмечали центр каждого следа нажатием левой кнопки компьютерной мыши. Используя векторный анализ, программа производила необходимые вычисления и выводила результаты в MS Excel (рис. 1Б).
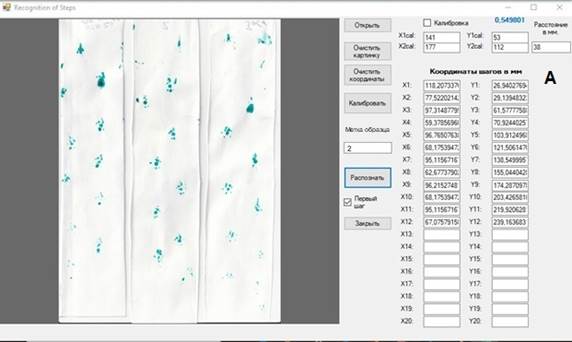
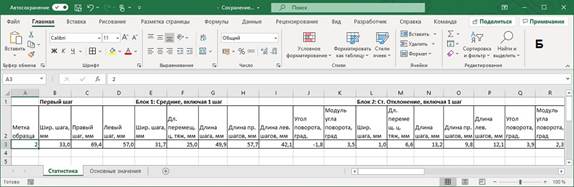
Рис. 1. Иллюстрация работы программы RecognitionOfSteps.exe: А – отображение диалогового окна программы; Б – пример вывода результата работы программы: параметры первого шага и блоки 1 и 2 (блоки 3–8 не показаны)
Таким образом, для каждого образца получали ширину первого шага, длину правого и левого первого шага и восемь блоков статистических показателей для ширины шага, длины перемещения центра тяжести, длины шага, длины правых шагов, длины левых шагов, угла поворота, модуля угла поворота. Статистические блоки включали: средние значения, стандартные отклонения, максимальные и минимальные значения, включая первые шаги и без учета первых шагов (всего 59 параметров).
Соответствие параметров нормальному распределению оценивали по критерию Шапиро–Уилка. Распределение модуля угла поворота, скорости и ширины первого шага значимо отличалось от нормального, поэтому для оценки достоверности отличий между группами и подгруппами был использован непараметрический критерий Манна–Уитни.
Результаты исследования и их обсуждение
В основу авторской интерпретации теста «туннель» положены следующие принципы: фиксация первичной реакции животного (при отсутствии обучения) наиболее информативна, параметры всех шагов значимы, направление движения животного соответствует направлению движения его центра тяжести, поэтому движения левых и правых конечностей взаимозависимы. На образце отпечатков лап центры четырех подряд идущих следов отмечены точками A, B, C, D (рис. 2).
В оценке ширины постановки лап мнения экспериментаторов расходятся. Большинство измеряют расстояние между двумя ближайшими отпечатками левой и правой лапы [2, 6, 7]. На рисунке 2 это отрезки AC, CB, BD. Альтернативный вариант предполагает измерение ширины шага как наименьшего расстояния между центром опорной лапы и линией перемещения противоположной лапы [13, 14]. Геометрически это соответствует высоте треугольника, вершиной которого служит след от одной лапы, а основанием – отрезок прямой между двумя ближайшими отпечатками противоположной лапы (рис. 2, отрезки BH2 и CH1). На 17 самках BALB/c в возрасте 51–65 недель были измерены оба этих параметра. Выяснилось, что расстояние между двумя ближайшими отпечатками левой и правой лап положительно связано с шириной шага коэффициентом корреляции Пирсона r=0,88 (p<0,01). Однако, если коэффициент корреляции между расстоянием между двумя ближайшими отпечатками левой и правой лап и средней длиной шага составляет 0,31, то между средней шириной шага и средней длиной шага – вдвое меньше (0,14). Таким образом, ширина шага, измеренная как наименьшее расстояние между центром опорной лапы и линией перемещения противоположной лапы, является менее зависимым параметром, чем расстояние между двумя ближайшими отпечатками левой и правой лап, что и определило наш выбор оценки ширины шага.
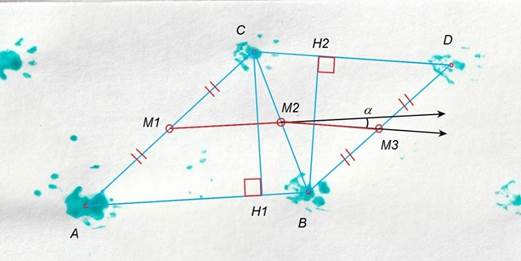
Рис. 2. Оценка параметров отпечатков задних лап мыши. Центры четырех подряд идущих следов отмечены точками A, B, C, D. Центры отрезков обозначены M1, M2 и M3. Высоты треугольников – отрезки CH1 и BH2
Длину левого шага оценивали как расстояние между соседними отпечатками левой лапы (рис. 2, отрезок CD). Длину правого шага определяли аналогично, но для правых следов (рис. 2, отрезок AB). Такой способ определения длины шагов применяется во всех работах, где используют тест «туннель». Перемещения центра тяжести животного обозначены на рисунке 2 отрезками M1M2 и M2M3, представляющими собой средние линии треугольников с вершиной на опорной лапе и основанием на линии перемещения противоположной лапы. Угол поворота на каждом шагу определяли как угол между векторами перемещения центра тяжести, который обозначен как угол α между M1M2 и M2M3 на рисунке 2. Отрицательные значения угла соответствуют повороту направо, положительные – налево. Усреднение этого показателя характеризует общее направление движения. Модуль угла α характеризует изменение направления на каждом шагу. Вычисление вышеперечисленных параметров с помощью линейки и транспортира возможно, но является трудоемким.
Большинство исследователей учитывают только усредненные показатели теста, часто не упоминая о включении в выборку или исключении первых шагов. Некоторые авторы [14] сообщают, что использовали только «среднюю порцию» следов, исключая несколько первых и последних. Разработанная нами программа RecognitionOfSteps.exe обладает опцией, позволяющей вычислить параметры первого шага отдельно (ширину и длину правого и левого шагов, рис. 1Б), а также получить значения всех остальных параметров с учетом первого шага и без него. С помощью программы были выявлены изменения характеристик походки с возрастом для мышей линий BALB/c и CBRB (табл. 2). Большинство усредненных показателей теста «туннель» оказались достоверно зависимыми от возраста самок обеих линий. Так, средняя ширина шагов без учета первого шага для обеих линий возрастала к старости, а средняя длина шага сокращалась с возрастом, что согласуется с данными в работе Lores-Arnaiza S. с соавторами [5]. Средняя скорость прохождения через туннель уменьшалась у самок обеих линий, средний угол поворота для линии CBRB также уменьшался, средний модуль угла поворота без учета первого шага увеличивался для самок линии BALB/c.
Таблица 2
Средние значения показателей теста «туннель» для молодых и старых мышей линий CBRB и BALB/c и достоверность их отличий по критерию Манна–Уитни между группами
|
Группа |
#1 (CBRB, молодые) |
#2 (CBRB, старые) |
Дост. отличий внутри линии CBRB |
#3 (BALB/c, молодые) |
#4 (BALB/c, старые) |
Дост. отличий внутри линии BALB/c |
Дост. отличий м/ мол. мышами |
Дост. отличий м/ стар мышами |
||||
|
Показатель |
M± SE |
n |
M± SE |
n |
p (#1,#2) |
M± SE |
n |
M± SE |
n |
p (#3,#4) |
p (#1,#3) |
p (#2,#4) |
|
Ширина шага без 1-го шага, мм |
32±1 |
14 |
35±1 |
29 |
<0,01 |
32±1 |
15 |
35±1 |
12 |
=0,01 |
НД |
НД |
|
Длина шага, мм |
56±1 |
14 |
48±1 |
29 |
<0,01 |
53±2 |
15 |
42±2 |
12 |
<0,01 |
НД |
<0,01 |
|
Скорость, мм/с |
187± 25 |
15 |
82± 10 |
28 |
<0,01 |
104± 15 |
15 |
65± 10 |
12 |
<0,05 |
<0,01 |
НД |
|
Угол поворота, град |
0,6± 0,5 |
14 |
–1,4± 0,5 |
29 |
<0,05 |
-0,3± 0,6 |
15 |
–0,9± 0,6 |
12 |
НД |
НД |
НД |
|
Модуль угла поворота без 1-го шага, град |
4,6± 0,4 |
14 |
6,2± 0,6 |
29 |
НД |
4,3± 0,5 |
15 |
5,4± 0,5 |
12 |
<0,05 |
НД |
НД |
|
Ширина 1-го шага, мм |
42±2 |
14 |
38±2 |
29 |
НД |
38±2 |
15 |
34±3 |
12 |
НД |
<0,05 |
=0,05. |
|
Длина 1-го правого шага, мм |
74±4 |
14 |
61±3 |
29 |
<0,01 |
50±3 |
15 |
39±3 |
12 |
<0,01 |
<0,01 |
<0,01 |
|
Длина 1-го левого шага, мм |
69±6 |
14 |
60±4 |
29 |
НД |
61±4 |
15 |
52±4 |
12 |
НД |
НД |
НД |
Полученные нами средние значения ширины и длины шагов сопоставимы с литературными данными. В работе Brooks S.P. с соавторами измерения проводились на молодых самцах BALB/c в возрасте 4 недель [13]. Авторы получили следующие результаты: средняя ширина шага 21 мм, что меньше, чем наши результаты для 8–11-недельных самок (32±1 мм), средняя длина шага 70 мм, что больше, чем полученные нами данные для 8–11-недельных самок (53±2 мм). Отличия легко объяснимы разницей в возрасте, весе и поле. Однако аналогичные данные для 4-недельных самцов BALB/c, приведенные в работе Burket J.A. с соавторами, гораздо ближе к полученным нами результатам (средняя ширина шага 26 мм, средняя длина шага 70 мм) [14].
Средняя скорость движения мыши через туннель также согласуется с данными других исследователей. В работе Brooks S.P. с соавторами измерено время прохождения коридора длиной 600 мм самцами BALB/c в возрасте 4 недели [13], а в другой работе Caballero-Garridoa E. с соавторами измерялась непосредственно скорость движения двухмесячных самцов линии C57BL/6 [1]. В обеих работах скорость передвижения, характерная для молодых мышей, была порядка 200 мм/с. Вдвое меньшая скорость самок BALB/c, полученная нами, может объясняться различиями в линии, возрасте и поле мышей.
Два из трех показателей первого шага самок CBRB и BALB/c оказались независимыми от возраста. Только длина первого правого шага достоверно уменьшалась с возрастом для мышей обеих линий. Также обнаружены достоверные различия по этому показателю между линиями внутри обеих возрастных групп. У мышей линии BALB/c первый правый шаг и в молодом, и в старом возрасте был достоверно меньше, чем у мышей линии CBRB. Аналогичные значимые отличия между линиями животных наблюдали для ширины первого шага. Интересным представляется тот факт, что если усредненная ширина шага увеличивалась с возрастом, то ширина первого шага на уровне тенденции (p=0,15) уменьшалась. Отличие первого шага от прочих объяснимо тем, что вклад разных структур мозга в инициацию движения и его продолжение различен [15]. Таким образом, обнаружено, что именно первый шаг характеризует линию и может быть включен в поведенческий профиль линии CBRB. Если учесть, что самки линии CBRB в позднем возрасте характеризуются проявлением тремора покоя, то на основе показателей первого шага следует оценивать степень постуральной неустойчивости (табл. 3).
Таблица 3
Средние значения показателей первого шага старых мышей линий CBRB с тремором и без тремора и достоверность отличий между подгруппами по критерию Манна–Уитни
|
Подгруппа |
Тремор– |
Тремор+ |
Достоверность отличий |
|
Показатель |
M±SE |
M±SE |
p |
|
Ширина 1-го шага, мм |
38±4 |
38±3 |
недостоверно |
|
Длина 1-го правого шага, мм |
63±5 |
60±5 |
недостоверно |
|
Длина 1-го левого шага, мм |
48±7 |
66±4 |
<0,01 |
Обнаружено, что развитие тремора у мышей приводит к увеличению более чем на треть длины первого левого шага. Не выявлено значимых различий между подгруппами «тремор+» и «тремор–» в других показателях первого шага и усредненных параметрах теста «туннель».
Заключение
Таким образом, разработанные нами модификация теста «туннель» и программное обеспечение позволяют оценивать возрастные изменения походки и выявлять постуральную неустойчивость при изучении естественного процесса старения и в модельных экспериментах по исследованию нейродегенеративных заболеваний.
Библиографическая ссылка
Соловьева А.С., Аронов Д.А., Шубернецкая О.С., Соловьева О.А., Семушина С.Г., Моисеева Е.В. ВЫЯВЛЕНИЕ ВОЗРАСТНОЙ ПОСТУРАЛЬНОЙ НЕУСТОЙЧИВОСТИ У МЫШЕЙ ДВУХ ЛИНИЙ С ПОМОЩЬЮ МОДИФИЦИРОВАННОГО ТЕСТА «ТУННЕЛЬ» (FOOTPRINT TEST) // Современные проблемы науки и образования. – 2020. – № 5. ;URL: https://science-education.ru/ru/article/view?id=30105 (дата обращения: 20.04.2024).



