Печень является одним из органов, который наиболее часто повреждается при травмах. За последние десятилетия рекомендации по лечению травм печени значительно изменились [1–3]. Высокие показатели повреждения печени обусловлены ее размерами, анатомическим строением и расположением. Правая доля печени часто повреждается при травмах брюшной полости [2].
Со временем произошли значительные изменения в подходе к лечению травмы печени. Тем не менее повреждение данного органа остается основной причиной летальности у пациентов с тяжелой травмой живота, а показатели смертности при травмах печени колеблются от 5 до 42% [2, 4]. Несмотря на технический прогресс в диагностике и лечении, смертность при травмах печени остается высокой, особенно у пациентов с открытой травмой брюшной полости. Основной причиной смерти у пациентов с повреждением печени является неконтролируемое кровотечение [1, 2, 4].
В настоящее время у хирургического сообщества растет понимание того, что наиболее важным шагом в лечении травм печени служит диагностика. В зависимости от степени тяжести неоперативное лечение пациентов является основным методом лечения данной патологии при наличии соответствующих условий. При этом пациенты с серьезной травмой и нестабильной гемодинамикой должны оперироваться в экстренном порядке [5, 6].
Независимо от хирургических вариантов лечения врачи должны контролировать степень тяжести повреждения пациентов и пытаться предотвратить осложнения. Новые методы лечения, такие как эмболизация печеночной артерии и трансплантация печени, все чаще используются для лечения серьезных повреждений печени в ведущих клиниках [5, 6, 7]. Результаты печеночной ангиоэмболизации были в целом благоприятными с высокой частотой успеха, однако данная методика лечения сопровождалась различными осложнениями [7, 8].
Несколько десятилетий назад хирургическое лечение было стандартной процедурой практически для всех видов травм печени и основывалось на предположении, что операция необходима для контроля объема кровотечения и предотвращения осложнений, связанных с повреждением желчевыводящих путей [9-11].
Мировая тактика лечения повреждений печени привела к значительному улучшению результатов. В ряде работ [7, 12, 13] изучались современные тенденции и результаты лечения пациентов с травматическими повреждениями печени. Было выявлено, что на сегодняшний день все больше клиник склоняются к консервативному ведению травм печени у пациентов со стабильной гемодинамикой, если пациент находится в условиях реанимационного отделения под динамическим наблюдением. Неоперативное лечение следует предпринимать в отношении тех пациентов, которые реагируют на интенсивную терапию, независимо от степени выраженности травмы печени. Сопутствующие внутрибрюшные повреждения паренхиматозных органов не исключают консервативное лечение [9].
Учитывая, что на современном этапе развития медицины в лечении травматических повреждений паренхиматозных органов, в частности печени, большинство специалистов отдают предпочтение неоперативным методам лечения [7], хирургическое лечение тяжелых травм печени в настоящее время все еще остается актуальным [9, 14].
Представленное нами исследование направлено на разработку новой щадящей методики хирургического лечения тяжелых травм печени.
Цель исследования: изучить патоморфологические особенности репарации паренхимы печени в ответ на повреждение при традиционной методике (ушивании) и при инновационной методике (тампонаде салфетками с гемостатическим препаратом и модифицированным пакетированием).
Задачи исследования:
1. Сравнить абсорбирующие свойства различных гемостатических препаратов in vitro.
2. Осуществить эксперимент на крысах по традиционной и инновационной технологиям.
3. Выявить различия процессов восстановления в ткани печени при использовании существующей технологии (ушивании) и разработанной авторами оригинальной методики.
Материалы и методы исследования
Начальный этап нашего исследования предполагал эксперимент, показывающий, как различные гемостатические материалы, в частности гелевые сорбенты, выполняют абсорбцию крови. Данный эксперимент стал частью доказательной базы по разработке и применению в клинической практике новой технологии оперативного лечения травматических повреждений печени. На конечном этапе разработки перспективных технологий оперирования при оценке пригодности новых материалов их экспериментальные исследования являются определяющими. В качестве испытуемых сорбентов были выбраны препараты, широко используемые в медицинской хирургической практике отечественного здравоохранения. Это гемостатическая губка, Тахокомб, Сургитамп и Молселект. Эксперимент заключался в том, что в пробирки с одинаковым количеством крови по 30 мл помещались материалы (гемостатическая губка, Тахокомб, Молселект, Сургитамп) одинаковой формы и размеров. Для оценки эффективности использования материалов произвольной формы необходимо математическое описание зависимости объема впитываемой крови от объема используемого вещества. По результатам проведенных испытаний нами был выбран наиболее перспективный материал Молселект. Его мы и использовали в эксперименте на лабораторных животных.
Экспериментальные работы проведены в соответствии с требованиями Европейской конвенции по защите экспериментальных животных 86/609 ЕЕС, эвтаназию животных осуществляли путем декапитации под эфирным наркозом. Содержание животных, выполнение различных процедур и вывод из опыта осуществлялись в соответствии с требованиями Европейской конвенции о защите позвоночных животных, используемых для экспериментов или в иных научных целях (Страсбург, 18.03.1986, ETS № 123).
Экспериментальное исследование проводилось в научно-исследовательском институте биологических проблем Воронежского государственного медицинского университета. Для экспериментальных исследований было отобрано 60 беспородных крыс массой 150–200 г, получавших стандартное питание. Животные были разделены на 2 группы по 30 крыс – контрольную и экспериментальную. 30 крысам проведено экспериментальное моделирование травмы печени по предложенной методике и 30 – по стандартной методике с применением ушивания (рис. 1). Животные содержались в стандартных условиях вивария, каждая крыса отдельно. Вывод из эксперимента в каждой группе крыс проводился на 4-е, 14-е и 28-е сутки от момента травмы (выбранные сроки соответствуют этапам репарации ткани печени). Затем у животных под наркозом производилось изъятие печени для гистологического исследования.
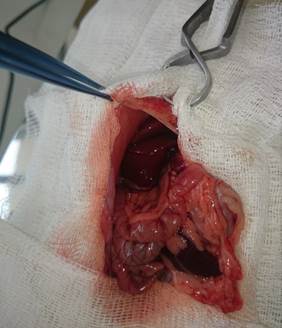
Рис. 1. Вид операционного поля
Эксперимент проводился в асептических условиях. Животные фиксировалась в положении на спине к специальному станку. Под общим эфирным наркозом в течение 10–15 минут после обработки 0,5%-ным спиртовым раствором хлоргексидина и обкладки операционного поля стерильными салфетками выполняли лапаротомию. В рану выводили долю печени, которую помещали на специальную подставку, и полым металлическим цилиндром диаметром 1 см наносили травму с извлечением части паренхимы печени для получения активного паренхиматозного кровотечения.
Для гемостаза раневой поверхности в контрольной группе использовали стандартный шовный материал, применяемый в хирургической практике: мононить ПГА 3,0. В экспериментальной группе применяли разработанную нами методику, суть которой заключалась в тампонаде гемостатическим материалом раны печени и окутывании ее полосками полипропиленового сетчатого эндопротеза. Операцию заканчивали осушением брюшной полости, для профилактики гнойных осложнений внутримышечно вводили антибиотик (цефотаксим 0,25 г), затем лапаротомную рану ушивали наглухо.
Удаленную часть печень взвешивали, измеряли, фотографировали. Кусочки ткани печени размером 1,0х1,0х0,5 см подвергали стандартной гистологической обработке (ткань печени толщиной 0,5 см помещали в стандартные кассеты, фиксировали в 10%-ном нейтральном забуференном формалине, обезвоживали через спирты восходящей плотности, заливали в парафин).
Микротомирование осуществляли на роторном микротоме фирмы «Орион-медик», Санкт-Петербург. Срезы толщиной 3–5 микрон окрашивали обзорной окраской – гематоксилин-эозином. Гистологические препараты со стандартной окраской исследовали с помощью световой микроскопии с последующей морфометрией. Готовые гистологические препараты исследовали на 4-й, 14-й и 28-й день эксперимента.
Проводили морфометрическое исследование размеров гепатоцитов, ядер и их объема около зоны некроза и в удалении от нее на два поля зрения при увеличении микроскопа х100. Исследовали 30 полей зрения в каждом препарате.
Полученные данные обрабатывали с использованием стандартных методов статистического анализа: рассчитывали средние значения (M), стандартные ошибки средних (m); t-критерий Стьюдента использовали для проверки статистической значимости отклонений. Также проверяли нормальность распределения по критерию Хи-квадрат Пирсона (c2), она оказалась достаточной (p=0,05).
Результаты исследования и их обсуждение
В микропрепаратах контрольной и экспериментальной групп на 4-й день эксперимента в паренхиме печени около зоны некроза и в удалении от нее на два поля зрения микроскопа (увеличение х100) отмечались морфологические изменения, характеризующиеся следующей микроскопической картиной.
Вокруг очага травматического повреждения обнаруживались кровоизлияния, запустевание печеночной паренхимы, отек и инфильтрация ткани печени клетками воспалительного ряда. Просматривались фокальные и массивные некрозы гепатоцитов, вакуольная и гидропическая дистрофия. Данные изменения, но в меньшей степени, отмечались и в паренхиме печени, удаленной от зоны некроза.
Существенных визуальных отличий в двух сравниваемых группах отмечено не было.
На 14-й день опыта в препаратах контрольной группы отмечались выраженные изменения воспалительного характера с явлениями образования демаркационного воспаления вокруг зоны повреждения (рис. 2). Имело место образование хронического воспалительного ответа с наличием клеток-гигантов «инородных тел» вокруг шовного материала с гипоксической реакций гепатоцитов в зоне повреждения и по периферии. Просматривались клетки различной величины, с нечеткой клеточной мембраной, ядрами различной интенсивности окраски, цитоплазмой, содержащей зернистые включения, гидропической и вакуольной дистрофией. Отмечалась слабо выраженная инфильтрация клетками лимфогистиоцитарного ряда ткани, окружающей зону повреждения. Вдали от повреждения имели место локальные инфильтраты в паренхиме печени с выраженным кариопикнозом гепатоцитов и расширением пространств Диссе. Компенсаторные реакции печени на повреждение в контрольной группе были слабо выражены.
Микроскопическая картина препаратов экспериментальной группы характеризовалась образованием воспалительного вала вокруг губчатой массы (геля). Процессы дистрофии гепатоцитов (зернистой, вакуольной, гидропической) и очаговая лимфогистиоцитарная инфильтрация в зоне повреждения и вдали от нее были менее выражены, чем в контрольной группе.
На 28-й день опыта отмечалось усиление процессов репарации (рис. 3). Появлялись молодые, меньшего размера с гипехромным ядром гепатоциты с большим количеством двуядерных гепатоцитов. В свою очередь исчезали инфильтраты клеток воспалительного ряда в зонах, отдаленных от очага повреждения печени. Отмечался выраженный неоангиогенез вокруг зоны фиброзной капсулы, окружающей зону повреждения печени.
Морфологическая картина свидетельствовала о том, что компенсаторно-репаративные процессы в экспериментальной группе протекали более активно по сравнению с контрольной (рис. 2, 3).
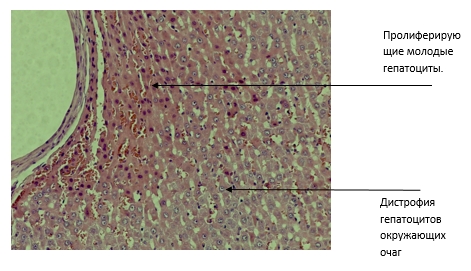
Рис. 2. 28-й день опыта в контрольной группе.
Просматривается очаговая пролиферация молодых гепатоцитов на фоне зернистой дистрофии гепатоцитов, окружающих участок повреждения
(окраска гематоксилин-увеличение х200)
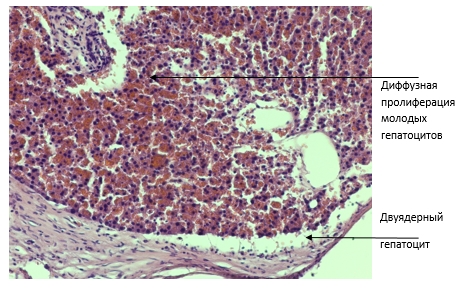
Рис. 3. 28-й день опыта в экспериментальной группе. Просматривается диффузная пролиферация молодых гепатоцитов около очага повреждения с большим количеством двуядерных гепатоцитов (окраска гематоксилин-увеличение х200)
Результаты морфометрических исследований представлены в таблицах 1–3.
Таблица 1
Результаты морфометрических исследований в контрольной группе
|
Группы |
Около зоны некроза |
В стороне от зоны некроза |
||||||
|
Размер клетки, мкм |
Размер ядра, мкм |
Размер клетки, мкм |
Размер ядра, мкм |
|||||
|
Min |
Max |
Min |
Max |
Min |
Max |
Min |
Max |
|
|
К4 |
12,7±0,43 |
19,2±0,37 |
5,8±0,35 |
6,8±0,32 |
12,2±0,39 |
19,1±0,66 |
5,6±0,33 |
6,8±0,26 |
|
К14 |
12,9±0,45 |
20,2±0,90 |
5,8±0,47 |
7,6±0,26 |
12,2±1,11 |
19,7±1,04 |
5,7±0,51 |
7,4±0,16 |
|
К28 |
13,3±0,50 |
20,3±1,00 |
6,5±0,22 |
7,7±0,18 |
13,8±0,50 |
20,5±0,78 |
6,5±0,30 |
7,6±0,33 |
Примечание1: р<0,05
1Различия между минимальным размером клетки около некроза и в стороне от некроза в группе К4.
Согласно данным, приведенным в таблице 1, не установлено статистически значимых различий как по размеру клетки и ядра около зоны некроза, так и в стороне от зоны некроза в контрольной группе. Исключение составляют показатели между минимальным размером клетки около зоны некроза и в стороне от зоны некроза в группе К4.
Таблица 2
Результаты морфометрических исследований в экспериментальной группе
|
Группы |
Около зоны некроза |
В стороне от зоны некроза |
||||||
|
Размер клетки, мкм |
Размер ядра, мкм |
Размер клетки, мкм |
Размер ядра, мкм |
|||||
|
Min |
Max |
Min |
Max |
Min |
Max |
Min |
Max |
|
|
Э4 |
12,6±0,18 |
19,2±0,29 |
6,2±0,43 |
7,6±0,33 |
12,2±0,22 |
18,6±0,30 |
6,1±0,04 |
7,3±0,10 |
|
Э14 |
12,3±0,46 |
18,1±0,97 |
6,1±0,50 |
7,4±0,62 |
12,9±0,31 |
18,3±0,44 |
5,9±0,33 |
7,1±0,38 |
|
Э28 |
12,2±0,39 |
17,4±0,86 |
5,8±0,30 |
7,0±0,32 |
12,5±0,48 |
17,8±1,02 |
6,0±0,37 |
7,4±0,35 |
Примечание1,2,3: р < 0,05
1Различия между минимальным размером клетки около некроза и в стороне от некроза в группах Э4 и Э14;
2Различия между максимальным размером клетки около некроза и в стороне от некроза в группе Э4;
3Различия между максимальным размером ядра около некроза и в стороне от некроза в группе Э4 и Э28.
В результате морфометрических исследований в экспериментальной группе, представленных в таблице 2, установлены статистически значимые различия (р<0,05) между минимальным размером клетки около зоны некроза и в стороне от зоны некроза в группах Э4 (12,6±0,18 и 12,2±0,22) и Э14 (12,3±0,46 и 12,9±0,31); максимальным размером клетки около зоны некроза и в стороне от зоны некроза в группе Э4 (19,2±0,29 и 18,6±0,30); максимальным размером ядра около зоны некроза и в стороне от зоны некроза в группе Э4 (7,6±0,33 и 7,3±0,10) и Э28 (7,0±0,32 и 7,4±0,35).
Следует отметить, что наиболее важным является не морфометрический анализ внутри контрольной или экспериментальной групп, а сравнительная оценка размера клеток и ядер между ними, представленная в таблице 3.
Таблица 3
Результаты морфометрических исследований в контрольной и экспериментальной группах на 28-й день эксперимента
|
Группы |
Около зоны некроза |
В стороне от зоны некроза |
||||||
|
Размер клетки, мкм |
Размер ядра, мкм |
Размер клетки, мкм |
Размер ядра, мкм |
|||||
|
Min |
Max |
Min |
Max |
Min |
Max |
Min |
Max |
|
|
К28 |
13,3±0,50 |
20,3±1,00 |
6,5±0,22 |
7,7±0,18 |
13,8±0,50 |
20,5±0,78 |
6,5±0,30 |
7,6±0,33 |
|
Э28 |
12,2±0,39 |
17,4±0,86 |
5,8±0,30 |
7,0±0,32 |
12,5±0,48 |
17,8±1,02 |
6,0±0,37 |
7,4±0,35 |
Примечание1: р<0,001
1Различия между морфометрическими показателями в группах К28 и Э28
Примечание2: р>0,05
2Различия между максимальным размером ядра в стороне от некроза в группах К28 и Э28.
В результате морфометрических исследований в контрольной и экспериментальной группах на 28-й день эксперимента установлены существенные различия практически между всеми показателями размера клеток и ядер как около зоны некроза, так и в стороне от зоны некроза на уровне значимости р<0,001 (за исключением максимального размера ядра в стороне от зоны некроза). В экспериментальной группе наблюдается снижение как минимального, так и максимального размера клетки около зоны некроза и в стороне от зоны некроза. Так, в контрольной группе минимальный размер клетки около зоны некроза составляет 13,3±0,50, а в экспериментальной – 12,2±0,39, а максимальный размер клетки около зоны некроза – 20,3±1,00 и 17,4±0,86 (р<0,001). В контрольной группе минимальный размер клетки в стороне от некроза – 13,8±0,50, в экспериментальной – 12,5±0,48, максимальный – 20,5±0,78 и 17,8±1,02 соответственно (р<0,001).
Также регистрируется значимое снижение минимального и максимального размеров ядра около зоны некроза и минимального размера ядра в стороне от зоны некроза (р<0,001). Так, в контрольной группе минимальный размер ядра около зоны некроза составляет 6,5±0,0,22, а в экспериментальной – 5,8±0,30, а максимальный – 7,7±0,18 и 7,0±0,32 соответственно. В контрольной группе минимальный размер ядра в стороне от зоны некроза 6,5±0,30, в экспериментальной – 6,0±0,37.
Полученные результаты указывают на лучшие процессы репарации при применении разработанной методики.
На сегодняшний день нет универсального гемостатического препарата, который бы удовлетворял всем требованиям оперирующего хирурга для остановки кровотечения при данной патологии. У всех препаратов имеются свои достоинства и недостатки. Каждый из них может занять свою нишу в различных разделах хирургического лечения повреждений органов брюшной полости, в том числе и печени [11, 14]. Однако отсутствие универсального гемостатического препарата обусловливает необходимость продолжения работы в данном направлении, потому что кровотечения при травмах печени являются важным показателем летальности пациентов [2, 4].
В ходе исследований отмечено, что процесс абсорбции крови представленными гемостатическими препаратами напрямую зависит от максимальной площади их поверхности. После аппроксимации экспериментальных данных было установлено, что для гемостатической губки, материалов Тахокомб и Сургитамп зависимость объема впитываемой крови от объема используемого вещества носит близкий к линейному характер, а в случае с материалом Молселект – нелинейный. В проблеме поиска оптимального гемостатического препарата мы получили следующие результаты: наибольший объем крови впитан материалом Молселект (до 30% исходного объема), что подтверждает перспективность его применения в клинической практике. Установлено, что материал имеет наименьший период набухания в крови, так как данный сорбент впитал большее количество крови за меньший промежуток времени, что важно для остановки внутрибрюшного кровотечения.
С целью проверки правильности выбора гемостатического препарата выполнена серия экспериментов на лабораторных животных.
В результате гистологических и морфометрических исследований в контрольной и экспериментальной группах наиболее статистически достоверные различия обнаруживаются на 28-й день эксперимента практически между всеми показателями размера клеток и ядер как около зоны некроза, так и в стороне от него на уровне значимости р<0,001. В контрольной и экспериментальной группах минимальный размер клеток 13,8±0,50 и 12,5±0,48 соответственно, максимальный – 20,5±0,78 и 17,8±1,02 соответственно. Морфологические признаки репаративных процессов в паренхиме печени после травмы подтверждают эффективность применения Молселекта в предложенной новой методике хирургического лечения травматических повреждений печени.
Выводы
1. В результате эксперимента гемостатические свойства препарата Молселект по сравнению с другими препаратами были более выражены.
2. Гистологическая картина паренхимы печени в сравниваемых группах на 4-й день опыта существенных отличий в группах не имела и характеризовалась очагами некроза с густой лимфолейкоцитарной инфильтрацией, кровоизлияниями и полнокровием, значительным межтканевым отеком и нарастающими процессами дистрофии гепатоцитов, выраженными в большей степени около очага травмы.
3. Дистрофические изменения паренхимы печени около очага повреждения на 14-й день опыта визуально были более выражены в контрольной группе животных в сравнении с экспериментальной. Это указывает на замедление процессов репарации в области травмы при технологии ушивания раны печени.
4. Микроскопическая картина изменений на 28-й день опыта характеризовалась активной репарацией, проявляющейся в выраженной пролиферации молодых гепатоцитов около очага повреждения в экспериментальной группе. В контрольной группе данные процессы были менее выражены.
5. В результате морфометрических исследований в экспериментальной группе на 28-й день эксперимента, где применялась разработанная авторами методика, установлено существенное (р<0,001) снижение практически всех показателей размера клеток и ядер как около зоны некроза, так и в стороне от нее по сравнению с группой, где использовалась стандартная методика ушивания паренхимы печени.
6. При экстраполяции полученных морфологических и морфометрических данных на клинический материал можно предположить, что применение нового подхода к методике лечения травматических повреждений печени будет способствовать более быстрому ее восстановлению.
Заключение
В проблеме хирургического лечения травматических повреждений печени существенную роль играют характер, скорость и объем кровопотери, поэтому поиск оптимального гемостатического препарата является краеугольным камнем успешной ликвидации (минимизации) данного серьезного осложнения в судьбе пациента.
Экспериментальная проверка традиционного метода ушивания и инновационного подхода в лечении травматических повреждений печени выявила схожие морфологические картины на ранних сроках эксперимента. Однако различия в репаративных процессах при травме печени лабораторных животных при традиционной и инновационной методиках имели место с середины эксперимента и были особо заметны при его завершении.
Библиографическая ссылка
Воронцов А.К., Трошин В.П., Пархисенко Ю.А., Корсаков А.В., Климашевич А.В. ОСОБЕННОСТИ РЕГЕНЕРАЦИИ КЛЕТОК ПЕЧЕНИ ПОСЛЕ ТРАВМЫ В ЭКСПЕРИМЕНТАЛЬНОМ ИССЛЕДОВАНИИ // Современные проблемы науки и образования. – 2020. – № 4. ;URL: https://science-education.ru/ru/article/view?id=29941 (дата обращения: 18.04.2024).



