Сахарный диабет (СД) стал эпидемией мирового масштаба, приводящей к серьезным микро- и макрососудистым осложнениям, что в дальнейшем снижает качество и продолжительность жизни, способствует развитию ранней инвалидизации пациентов. В связи с этим прогнозирование риска осложнений при сахарном диабете является одной из приоритетных задач диабетологии [1].
Многие исследования продемонстрировали, что плохой контроль уровня глюкозы является одним из факторов риска, непосредственно связанных с микрососудистыми осложнениями при СД 1 типа [2-4] и смертностью при СД 1 типа [5].
Основным показателем компенсации СД является определение уровня гликированного гемоглобина (HbA1c), который оценивается один раз в три месяца. Такая частота выполнения теста обусловлена международными стандартами достижения высокой степени контроля заболеванияи предотвращения микро- и макрососудистых осложнений [6; 7]. На каждый 1% улучшения показателя HbA1c - пропорционально снижается скорость развития поздних осложнений СД: инсультов, инфарктов, сердечной недостаточности, катаракты, микрососудистых осложнений и ампутаций, связанных с микроангиопатией [8]. За последние два десятилетия HbA1c стал целевым стандартом для измерения уровня общего гликемического контроля и оценки риска осложнений диабета, определяющим выбор терапевтической тактики врачом [9].
Несмотря на то что HbA1c является основным маркером риска осложнений и смертности от диабета, он отображает лишь средний уровень гликемии и не дает возможности оценки колебаний в течение различных периодов времени. Эта реальность побудила клиницистов и исследователей изучить, есть ли другие показатели помимо HbA1c, которые могли быспрогнозировать риск развития осложнений сахарного диабета и содействовать более эффективному принятию клинических решений [10].
Сегодня появились качественно новые технические возможности для анализа и контроля гликемических кривых у пациентов с сахарным диабетом 1 типа: инсулиновые помпы с функцией обратной связи, непрерывный мониторинг гликемии, флеш-мониторинг и др. Непрерывный мониторинг гликемии (НМГ) - наиболее объективный метод диагностики нарушений углеводного обмена и оценки степени его компенсации у больных сахарным диабетом. Система постоянного мониторинга глюкозы и данные, полученные с ее помощью, позволяют выявить определенные тенденции суточных колебаний гликемии – вариабельность гликемии (ВГ), с регистрацией всех эпизодов гипо- и гипергликемий, выяснить причины их возникновения, которые невозможно оценить при определении гликемии с помощью глюкометра [11; 12].
В настоящее время пристальное внимание в диабетологии уделяется индексам вариабельности гликемии (ИВГ), и ряд исследований доказывает взаимосвязь данных индексов с уровнем контроля и компенсации сахарного диабета [13; 14].
Так как стандартные методы оценки уровня контроля и компенсации сахарного диабета не всегда точны, то именно анализ индексов вариабельности гликемии позволит практическому врачу принимать верное и правильное решение относительно тактики лечения пациента с СД для достижения компенсации заболевания.
Цель исследования: провести сравнительный анализ гликированного гемоглобина и индексов вариабельности гликемии для прогнозирования компенсации сахарного диабета 1 типа.
Материалы и методы исследования. Исследование являлось проспективным, открытым, контролируемым, клиническим, в параллельных группах и выполнялось на базе Федерального государственного бюджетного образовательного учреждения высшего образования «Сибирский государственный медицинский университет» Министерства здравоохранения Российской Федерации (ФГБОУ ВО «СибГМУ» Минздрава России), г. Томск, при поддержке Фонда развития филантропии (Договор № 57/ТФ-14/315 от 14.05.2014) [15].
В исследование было включено 120 пациентов с сахарным диабетом 1 типа, которым проводилось непрерывное мониторирование гликемии в начале и в конце исследования. Все участники исследования были разделены на три группы:
1. Группа А (n=40 чел.) – в группу включались пациенты, использующие инсулинотерапию в помповом режиме с возможностью дистанционного мониторинга.
2. Группа В (n=40 чел.) – данную группу составили пациенты, получающие инсулинотерапию в помповом режиме без возможности дистанционного мониторинга.
3. Группа С (n=40 чел.) – сравнительная группа – больные с базисно-болюсной инсулинотерапией.
Средний возраст всех обследуемых составил 13,6 (10-17) года. Из них девочек 63 чел. (52,5%), мальчиков 57 чел. (47,5%). Длительность заболевания варьировалась от 3 до 17 лет, и в среднем составила 7,3 года. Все пациенты были сопоставимы по полу и возрасту. Обследованные находились под наблюдением в течение 24 недель, каждые 12 недель проводилось 3 очных визита и 24 дистанционные консультации.
Все участники исследования подписали добровольное информированное согласие. Протокол исследования одобрен Этическим комитетом ФГБОУ ВО «СибГМУ» Минздрава России (№ 5004 от 28.11.2016).
Больные в ходе исследования отправляли данные своих отчетов об уровне глюкозы крови, полученных благодаря различным устройствам НМГ и специализированного программного обеспечения. В начале и в конце исследования с помощью калькулятора EasyGV [16] рассчитывались индексы вариабельности гликемии, которые были выбраны в качестве независимых параметров прогнозирования уровня HbA1c: стандартное отклонение (SD), индекc длительного повышения гликемии (CONGA), индекc лaбильности гликемии (LI), индекcы риcкa гипо- и гипергликемии (LBGI, HBGI), среднее значение общего риска (ADRR), средняя амплитуда колебаний гликемии (MAGE), качество контроля гликемии (M-value), скорость изменения гликемии (MAG). Характеристика ИВГ в начале исследования в каждой группе приведена в таблице 1.
Таблица 1
Характеристика индексов вариабельности гликемии у пациентов в начале исследования
|
Индексы вариабельности гликемии |
Группа дистанционного мониторинга (n=40) |
Группа очного наблюдения (n=40) |
Сравнительная группа (n=40) |
р1-2 |
р2-3 |
р1-3 |
|
HbA1c, % |
9,1 [8,2; 9,7] |
9,5 [8,7; 10,9] |
9,05 [8,2; 10] |
0,061 |
0,279 |
0,134 |
|
Средний уровень гликемии (Mean), ммоль/л |
8.48±1.89 |
9.8±1.71 |
8.95±1.4 |
0,051 |
0,067 |
0,205 |
|
Стандартное отклонение (SD), ммоль/л |
2,57 [1,57; 3,38] |
2,75 [2,1; 3,58] |
2,65 [2,12; 3,29] |
0,367 |
0,378 |
0,820 |
|
Индекc длительного повышения гликемии (CONGA), ммоль/л |
9,19 [8,21; 10,75] |
10,21 [9,32; 11,63] |
9,72 [8,94; 11,9] |
0,062 |
0,577 |
0,204 |
|
Индекc лaбильности гликемии (LI), (ммоль/л)2/час |
6,37 [4,92; 10,72] |
9,37 [7,24; 14,28] |
10,34 [9,21; 12,03] |
0,001* |
0,294 |
0,000* |
|
Индекc риcкa гипогликемии (LBGI) |
5,88 [3,56; 8,05] |
7,33 [6,12; 9,33] |
3,41 [2,45; 5,08] |
0,004* |
0,000* |
0,000* |
|
Индекc риcкa гипергликемии (HBGI) |
12,17 [8,88; 14,7] |
11,24 [8,94; 14,28] |
17,75 [12,45; 20,15] |
0,476 |
0,000* |
0,000* |
|
Среднее значение общего риска (ADRR) |
28,38 [15,96; 36,95] |
24,76 [19,76; 48,84] |
26,26 [18,37; 31,23] |
0,115 |
0,168 |
0,199 |
|
Оценка межсуточной вариабельности гликемии (MODD), ммоль/л |
3,97 [3,25; 5,52] |
5,08 [3,59; 6,59] |
6,47 [4,5; 8,55] |
0,108 |
0,061 |
0,001* |
|
Средняя амплитуда колебаний гликемии (MAGE), ммоль/л |
5,12 [4,66; 7,15] |
7,32 [6,36; 8,26] |
7,81 [6,24; 9,14] |
0,000* |
0,366 |
0,000* |
|
Качество контроля (M-value), ммоль/л |
14,2 [4,54; 12,79] |
15,02 [9,88; 22,28] |
13,52 [10,79; 17,97] |
0,071 |
0,501 |
0,072 |
|
Скорость изменения гликемии (MAG), ммоль/л/час |
3,36 [1,5; 2,75] |
3,55 [2,12; 4,85] |
4,3 [2,53; 5,8] |
0,002* |
0,075 |
0,000* |
Примечание: * – значимость различий между группами (Z-критерий Манна–Уитни, различия значимы при p<0,05); Me – медиана, Q1; Q3 – нижний; верхний квартили.
Для оценки метаболической эффективности всем пациентам в начале и в конце исследования был проведен анализ HbA1c методом жидкостной хроматографии на анализаторе DS5 Glycomat (фирма DrewScientific, Нидерланды).
Для исследования взаимосвязи между ИВГ и уровнем компенсации сахарного диабета на основе HbA1c было построено две нейросетевые модели: регрессионная и классифицирующая. Регрессионная модель позволяет прогнозировать риск развития сосудистых осложнений на основе ИВГ. Классифицирующая модель дает возможность оценить уровень компенсации сахарного диабета. Обучение модели проводилось на всех включенных пациентах, 70 из которых были случайным образом выбраны для включения в обучающую выборку, 10 пациентов составили тестовую, данные которой не использовались для обучения нейронной сети.
Регрессионная нейросетевая модель была построена в среде статистических вычислений типа R с помощью программного пакета Neuralnet [17]. Структура модели была выбрана путем сравнения более чем 20 тыс. тестовых моделей, имеющих различное количество скрытых слоев и нейронов в этих слоях. Критерием выбора модели служила минимальная сложность, отсутствие переобучения и высокое значение коэффициента детерминации. При построении нейросетевого классификатора компенсации сахарного диабета на основании данных ВГ и концентрации HbA1c были проведены численные исследования на моделях без внутреннего слоя (линейный классификатор) с количеством внутренних слоев от 1 до 3.
Статистический анализ проводился с помощью программы SPSS 23.0 (IBM SPSS Statistics, США). Для оценки вида распределения количественных показателей использовался критерий Шапиро-Уилка. Описательная статистика для ненормально раcпределенных количественных пaраметров представлена медианой и первым и третьим квартилями Me [Q1; Q3], для нормально распределенных количественных параметров приводились значения Xср±σ. Статистическую значимость различий для независимых данных оценивали по U-критерию Манна-Уитни, для зависимых данных - по критерию Уилкоксона. Рaзличия считали знaчимыми при p<0,05.
Результаты исследования и их обсуждение. В отчетах НМГ у пациентов группы А в конце исследования было отмечено достоверное снижение всех показателей ВГ по сравнению с началом исследования: индекса стандартного отклонения (SD), который в начале исследования составил 2,57 [1,57; 3,38] ммоль/л, а в конце – 2,08 [1,07; 2,59] ммоль/л (р<0,001); индекса длительного повышения гликемии (CONGA), отражающего внутрисуточные колебания глюкозы, имел тенденцию к снижению к концу исследования - 9,19 [8,21; 10,75] ммоль/л и 6,16 [5,62; 6,96] ммоль/л, р=0,001. Значительное снижение показал индекс среднего общего риска (ADRR) с 28,38 [15,96; 36,95] до 19,97 [13,34; 27,02] (р≤0,000), в 1,5 раза, что свидетельствует об уменьшении риска возникновения микро- и макрососудистых осложнений у пациентов с сахарным диабетом 1 типа на дистанционном мониторинге. Показатель M-value, характеризующий качество контроля заболевания, на визите 1 составил 14,2 [4,54; 12,79] ммоль/л, а на визите 3 - 6,7 [3,23; 10,02] ммоль/л (р=0,005).
В группе В показатель SD к концу исследования снизился незначительно в сравнении с началом исследования: 2,75 [2,1; 3,58] ммоль/л и 2,37 [1,68; 3,28] ммоль/л (р<0,001) в начале и в конце наблюдения соответственно. Индекс CONGA имел достоверную тенденцию к уменьшению: на последнем визите составил 8,32 [7,51; 9,17] ммоль/л при р=0,005. Индекс среднего общего риска (ADRR) в данной группе снизился незначительно - 23,2 [16,32; 35,82] (р≤0,000), в сравнении с дистанционной моделью наблюдения.
Большая часть показателей ВГ в группе пациентов, получающих базисно-болюсную терапию (группа С), имели тенденцию к увеличению индексов к концу исследования. Отмечалось резкое увеличение индекса среднего общего риска (ADRR) с 26,26 [18,37; 31,23] до 39,68 [30,79; 44,26] (р≤0,000), в 1,5 раза, что свидетельствовало о высоком риске возникновения ангиопатий вследствие сахарного диабета. Показатель качества контроля (M-value) в начале исследования в данной группе составлял 13,52 [10,79; 17,97] ммоль/л, а в конце исследования 16,13 [13,84; 19,79] ммоль/л (р≤0,000), что говорит о потере контроля гликемии у пациентов на стандартной терапии СД. При этом следует отметить незначительное увеличение индекса скорости изменения гликемии (MAG), который является предиктором летальных событий (тяжелые гипогликемии, кетоацидотические комы) с 4,3 [2,53; 5,8] ммоль/л/час до 4,48 [3,1; 5,57] ммоль/л/час, что свидетельствует о возможности развития жизнеугрожающих состояний у данной когорты пациентов (р= 0,048).
При проведении сравнительного анализа данных во всех трех группах было выявлено достоверное различие некоторых показателей ВГ в течение исследования. Так, показатель SD имел достоверное увеличение в группе базисно-болюсной терапии - 2,51 [2,06; 3,11] ммоль/л в сравнении с группой дистанционного наблюдения 2,08 [1,07; 2,59] ммоль/л (р=0,006), что показывает значимые колебания уровня глюкозы у пациентов с СД 1 типа. Отмечается достоверная разница индекса длительного повышения гликемии (CONGA) между группами в конце исследования: 6,16 [5,62; 6,96] ммоль/л, 8,32 [7,51; 9,17] ммоль/л и 10,54 [9; 12,5] ммоль/л в группе А, В и С соответственно (во всех группах р≤0,000). Значительная разница выявлена при сравнении индекса ADRR в группе дистанционного мониторинга 19,97 [13,34; 27,02] и группе очного наблюдения 23,2 [16,32; 35,82] в сравнении с группой С 39,68 [30,79; 44,26] (в обоих случаях р≤0,000) – увеличение риска возникновения микро- и макрососудистых событий почти в 2 раза выше у больных, получающих базисно-болюсную инсулинотерапию, в отличие от обследованных на помповой инсулинотерапии с использованием НМГ. Такая же тенденция была выявлена с индексом MAG: 1,64 [1,14; 2,05] ммоль/л/час в группе А, 2,36 [1,37; 4,28] ммоль/л/час в группе В и 4,48 [3,1; 5,57] ммоль/л/час в группе С (р1-2=0,003, р2-3=0,001 и р1-3≤0,000), что ассоциировано с высокой скоростью изменения уровня глюкозы крови и может привести к летальному исходу. Данные приведены в таблице 2.
Таблица 2
Сравнение индексов вариабельности гликемии во всех группах на последнем визите исследования
|
Индексы вариабельности гликемии |
Группа дистанционного мониторинга (n=40) |
Группа очного наблюдения (n=40) |
Сравнительная группа (n=40) |
р1-2 |
р2-3 |
р1-3 |
|
Cтандартное отклонение (SD), ммоль/л |
2,08 [1,07; 2,59] |
2,37 [1,68; 3,28] |
2,51 [2,06; 3,11] |
0,019* |
0,686 |
0,006* |
|
Индекc длительного повышения гликемии (CONGA), ммоль/л |
6,16 [5,62; 6,96] |
8,32 [7,51; 9,17] |
10,54 [9; 12,5] |
0,000* |
0,000* |
0,000* |
|
Индекc лaбильности гликемии (LI), (ммоль/л)2/час |
4,9 [3,3; 7,99] |
8,32 [6,85; 11,64] |
12,47 [10,85; 13,7] |
0,000* |
0,000* |
0,000* |
|
Индекc риcкa гипогликемии (LBGI) |
4,3[2,99; 5,87] |
7,2 [6,42; 7,85] |
3,81 [2,97; 5,43] |
0,000* |
0,000* |
0,498 |
|
Индекc риcкa гипергликемии (HBGI) |
5,46 [3,04; 8,03] |
8,34 [6,56; 10,32] |
18,52 [15,54; 22,33] |
0,000* |
0,000* |
0,000* |
|
Среднее значение общего риска (ADRR) |
19,97 [13,34; 27,02] |
23,2 [16,32; 35,82] |
39,68 [30,79; 44,26] |
0,077 |
0,000* |
0,000* |
|
Оценка межсуточной вариабельности гликемии (MODD), ммоль/л |
3,03 [2,21; 4,13] |
3,85 [2,91; 5,58] |
7,74 [6,26; 9,36] |
0,020* |
0,000* |
0,000* |
|
Средняя амплитуда колебаний гликемии (MAGE), ммоль/л |
4,76 [4,03; 6,32] |
6,17 [5,54; 7,03] |
9,98 [7,9; 11,02] |
0,000* |
0,000* |
0,000* |
|
Качество контроля (M-value), ммоль/л |
6,7 [3,23; 10,02] |
11,2 [6,35; 16,53] |
16,13 [13,84; 19,79] |
0,002* |
0,003* |
0,000* |
|
Скорость изменения гликемии (MAG), ммоль/л/час |
1,64 [1,14; 2,05] |
2,36 [1,37; 4,28] |
4,48 [3,1; 5,57] |
0,003* |
0,001* |
0,000* |
Примечание: * – значимость различий между группами (Z-критерий Манна–Уитни, различия значимы при p<0,05); Me – медиана, Q1; Q3 – нижний; верхний квартили.
Гликированный гемоглобин (HbA1c) в группе дистанционного наблюдения к визиту 3 снизился на 1,95% (р≤0,000), в группе очного наблюдения уменьшился на 0,8% (р≤0,000), а в группе стандартной терапии увеличился на 0,05% при р=0,546. При этом средний уровень гликемии в группе А уменьшился на 1,97 ммоль/л (р=0,043), в группе В отмечалось уменьшение на 1,55 ммоль/л (р=0,585), а в группе С было выявлено достоверное повышение данного показателя на 0,54 ммоль/л (р=0,042). Значительное снижение гликированного гемоглобина в группе дистанционного мониторинга согласуется с другими зарубежными исследованиями и говорит о клинико-метаболической эффективности данного метода [18; 19]. Данные представлены в таблице 3.
Таблица 3
Сравнение гликированного гемоглобина и среднего уровня гликемии у пациентов с сахарным диабетом 1 типа
|
Группа |
HbA1c в начале исследования, % |
HbA1c в конце исследования, % |
р |
Средний уровень гликемии (Mean) в начале исследования, ммоль/л |
Средний уровень гликемии (Mean) в конце исследования, ммоль/л |
р |
|
Группа дистанционного мониторинга (n=40) |
9,1 [8,2; 9,7] |
7,15 [6,7; 7,7] |
0,000* |
8,48±1,89 |
6,51±1,63 |
0,043* |
|
Группа очного наблюдения (n=40) |
9,5 [8,7; 10,9] |
8,8 [7,8; 9,8] |
0,000* |
9,8±1,71 |
8,25±2,43 |
0,585 |
|
Сравнительная группа (n=40) |
9,05 [8,2; 10] |
9,1 [8,4; 10,05] |
0,546 |
8,95±1,4 |
9,49±1,79 |
0,042* |
Примечание: * – значимость различий между группами (критерий Уилкоксона, различия значимы при p<0,05); Me – медиана, Q1; Q3 – нижний; верхний квартили.
Для выявления взаимосвязи между ИВГ и уровнем компенсации сахарного диабета на основе HbA1c был выбран метод построения нейросетевой модели с одним или несколькими скрытыми слоями, которые позволяют описывать сложные нелинейные взаимосвязи. При построении нейросетевых моделей оптимальной оказалась модель на основе многослойного перцептрона с тремя скрытыми слоями и количеством нейронов в каждом слое (рисунок 1).
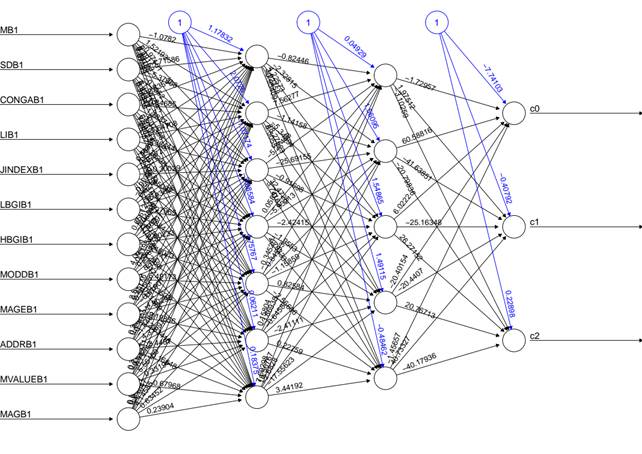
Рис. 1. Нейросетевая модель регрессионного типа на основе многослойного перцептрона прогнозирования компенсации на основе данных вариабельности гликемии
Построенная модель показала очень высокое значение коэффициента детерминации R2=0,987, что свидетельствует о высокой достоверности прогнозирования компенсации заболевания по показателям вариабельности гликемии, что отображено на рисунке 2. При создании традиционной модели на основе множественной регрессии коэффициент детерминации составил R2=0,254, что ассоциировано с низкой точностью прогнозирования степени компенсации СД только по HbA1c и большей остаточной ошибке (рисунок 3).
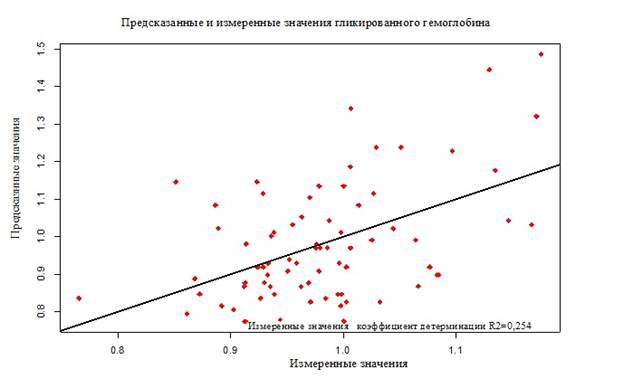
Рис. 2. Результаты прогностического моделирования уровня гликированного гемоглобина по данным вариабельности гликемии
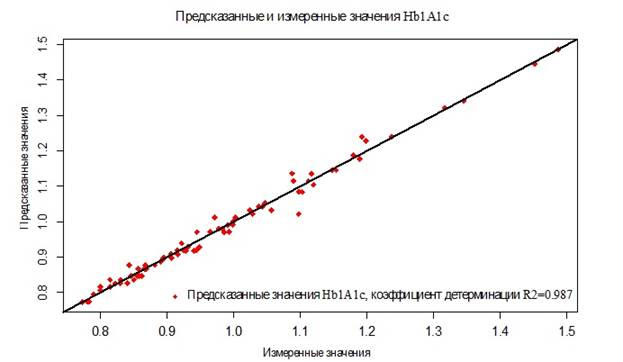
Рис. 3. Результаты прогностического моделирования уровня гликированного гемоглобина на основе модели множественной регрессии
Заключение. При проведении исследования вариабельности гликемии в группе дистанционного мониторинга показатели достоверно улучшились в сравнении со сравнительной группой и очного наблюдения, что можно расценивать как положительную динамику.
Уменьшение гликированного гемоглобина на 1,95% и среднего уровня гликемии на 1,97 ммоль/л в группе дистанционного мониторинга на последнем визите свидетельствует о клинико-метаболической эффективности данного метода в сравнении с другими моделями наблюдения пациентов с сахарным диабетом 1 типа.
Следует отметить значительное ухудшение показателей риска развития сосудистых событий у группы пациентов, находящихся на базисно-болюсном режиме, что заставляет обратить пристальное внимание на данную когорту пациентов для достижения компенсации заболевания.
Нейросетевая модель с высоким индексом детерминации на основе индексов вариабельности гликемии демонстрирует существенно более высокую точность прогнозирования компенсации заболевания в сравнении со стандартным методом оценки (HbA1c), что позволяет спрогнозировать осложнения и обеспечить персонализированный подход в лечении пациентов с сахарным диабетом 1 типа.
Библиографическая ссылка
Самойлова Ю.Г., Кошмелева М.В., Кобякова О.С., Бразовский К.С., Назаренко В.В., Толмачев И.В., Олейник О.А., Филиппова Т.А., Подчиненова Д.В., Сиволобова Т.В. НЕЙРОСЕТЕВАЯ МОДЕЛЬ ПРОГНОЗИРОВАНИЯ КОМПЕНСАЦИИ САХАРНОГО ДИАБЕТА НА ОСНОВЕ ИНДЕКСОВ ВАРИАБЕЛЬНОСТИ ГЛИКЕМИИ // Современные проблемы науки и образования. – 2019. – № 3. ;URL: https://science-education.ru/ru/article/view?id=28922 (дата обращения: 23.04.2024).



