Рак гортани составляет 2,2% в общей структуре заболеваемости населения злокачественными новообразованиями, и частота его выявления ежегодно повышается. Согласно статистическим исследованиям, за последние 10 лет заболеваемость раком гортани в России увеличилась на 20% [1]. Ранняя диагностика рака гортани находится на низком уровне: с некоторых скачков в 1986 г. (46,4%) и в 2002 г. (42,2%) этот показатель по России снизился в 2012 г. до 34,2% [2]. Органосохраняющее хирургическое лечение занимает важное место в комплексном лечении больных раком гортани. При выполнении открытых резекций гортани важнейшими аспектами являются онкологическая адекватность выполненной операции и восстановление утраченных функций органа, что снижает процент неудовлетворительных функциональных результатов и уменьшает число отказов больных от хирургического лечения по стандартной методике – ларингэктомии [3]. Суммируя все органосохраняющие методики лечения распространенного рака гортани, следует отметить, что они позволяют сохранить гортань у 67,7% больных [4]. Расширение показаний к органосохраняющим операциям в настоящее время произошло за счет больных с распространенностью процесса T3N0-1M0 при определенных вариантах локализаций опухолевого поражения, а также за счет пациентов, у которых выявлен ограниченный местный рецидив опухоли после лучевого лечения [5].
Цель исследования: улучшить результаты лечения больных местнораспространенным раком гортани путем использования органосохранной операции как этапа комбинированного лечения.
Материалы и методы исследования. Для реализации цели за период 2012-2017 гг. были проведены исследования на 50 больных местнораспространенным раком гортани. Основную группу составили 20 больных раком гортани стадии III (T3N0-1M0), им проведено органосохраняющее лечение с реконструкцией утраченных частей гортани с использованием аутотканей: сохраненной части пластины щитовидного хряща, прямых мышц шеи и деэпидермизированного шейного кожно-жирового лоскута по оригинальной методике, разработанной в Отделении опухолей головы и шеи ФГБУ «РНИОИ» МЗ РФ. В контрольную группу вошли 30 больных раком гортани в стадии III (T3N0-1M0), им в ходе комбинированного лечения выполнялась экстирпация гортани.
Между группами не было значимых различий по полу, возрасту, характеру основной и сопутствующей патологии. Все больные были мужчинами в возрасте 40 до 70 лет. До начала лечения производился отбор больных по строгим показаниям, диагноз подтверждался результатами фиброларингоскопии с гистологическим исследованием биоптата опухоли гортани. Для определения распространенности опухолевого процесса выполняли СРКТ гортани; ультразвуковое исследование шеи с целью выявления или исключения метастатического поражения региональных шейных лимфатических узлов, органов брюшной полости, рентгенографию органов грудной клетки. В обеих группах имел место плоскоклеточный рак. У 2 (10±6,7%) больных основной группы и 1 (3,3±3,3%) контрольной группы были выявлены одиночные шейные метастазы. Распределение больных по распространенности процесса представлено в таблице 1.
Таблица 1
Распределение больных в соответствии с классификацией TNM в основной и контрольной группах
|
Классификация по системе TNM |
T3N0M0 |
T3N1M0 |
Ур. стат. зн. р |
||
|
Абс. ч. |
%±SE |
Абс. ч. |
%±SE |
||
|
Основная группа (n=20) |
18 |
90±6,7 |
2 |
10±6,7 |
0,331 |
|
Контрольная группа (n=30) |
29 |
96,7±3,3 |
1 |
3,3±3,3 |
|
Всем больным основной и контрольной групп проводилось комбинированное лечение. В основной группе пациентов, в 2 случаях, первым этапом комбинированного лечения был проведен курс лучевой терапии в суммарной очаговой дозе 60 Гр.
У всех 20 больных основной группы реализовано органосохраняющее лечение с применением разработанной нами методики операции. Основным пластическим материалом для реконструкции была оставшаяся после резекции верхняя 1/3 пластины щитовидного хряща, прямые мышцы шеи и шейный кожно-жировой лоскут. Первым этапом определяли объем удаляемых тканей и рассчитывали примерный объем шейного кожно-жирового лоскута, производили разметку шеи в положении больного лежа. Отмечали планируемую линию кожного разреза с одномоментным выкраиванием кожно-жирового лоскута для последующей реконструкции. Далее выполняли трахеостомию, обнажали щитовидный хрящ по средней линии, выполняли тиреофиссуру. Выполняли резекцию фрагмента пластины щитовидного хряща с подлежащими мягкими тканями гортани и опухолью с сохранением верхней 1/3 пластины щитовидного хряща в виде перекладины. Заготовленный и предварительно деэпидермизированный шейный кожно-жировой языкообразный лоскут перекидывали через сохраненную часть пластины щитовидного хряща, служащую опорой для последнего, и подшивали по периметру к сохраненным мягким тканям гортани. Оформляли плановую ларингостому не более 2х1 см. Полость неогортани тампонировали тампоном-обтуратором с раствором антисептика на срок до 7 суток. Больным с метастазами в региональные лимфоузлы шеи выполняли шейную лимфодиссекцию I-III уровня. Больным, не получавшим лучевое лечение, курс конформной дистанционной гамма-терапии на область гортани и пути лимфооттока до СОД 40 Гр проводился спустя 14-20 суток после выполнения реконструктивной операции. Численные данные анализировали с помощью приложений Excel и Statistiсa 6.0. Статистическую значимость различий оценивали непараметрическим U-критерием (Манна-Уитни) и параметрическим – Т-тест Стьюдента. Различия считали статистически значимыми при p<0,05. Бессобытийную выживаемость в основной и контрольной группах больных оценивали методом Каплана-Мейера.
Результаты исследования и их обсуждение
В ходе исследования нами произведена оценка осложнений, функциональных и онкологических результатов лечения рака гортани с применением разработанной нами методики расширенной резекции гортани с реконструкцией. У пациентов основной группы ранние послеоперационные осложнения представлены 2 (10±6,7%) случаями послеоперационного хондроперихондрита и 1 (5±4,9%) случаем краевого некроза перемещенного кожно-жирового лоскута у пациентов после проведения предоперационного курса лучевого лечения по радикальной программе в СОД 60 Гр. У 1 пациента в возрасте 70 лет возник краевой некроз перемещенного кожного лоскута. Ему была выполнена некрэктомия без последствий для функциональных результатов предложенного нами метода хирургического вмешательства.
С учетом травматичности вмешательства у всех больных наблюдался отек мягких тканей здоровой сохраненной ½ гортани, надгортанника, перемещенного кожно-жирового лоскута в течение 2-3 суток после операции. Это способствовало нарушению эвакуации слюны.
Уменьшение отека и наличие самостоятельных движений надгортанника было показанием к удалению носо-пищеводного зонда. В таблице 2 приведены данные по срокам удаления носо-пищеводного зонда больных основной группы.
Таблица 2
Сроки восстановления функции глотания в ближайшем послеоперационном периоде у больных основной группы
|
Сроки удаления носо-пищеводного зонда после операции |
Уровень компенсации функции глотания |
|||||
|
Без поперхивания |
Поперхивание жидкой пищей |
Самостоятельное питание в определенном положении |
||||
|
абс. ч. |
%±SE |
абс. ч. |
%±SE |
абс. ч. |
%±SE |
|
|
2-3-й день |
18 |
90±6,7 |
- |
- |
- |
- |
|
4-6-й день |
2 |
10±6,7 |
1 |
5±4,9 |
- |
- |
|
7 и более дней |
- |
- |
2 |
10±6,7 |
2 |
10±6,7 |
|
Всего |
20 |
100 |
5 |
25±9,7 |
2 |
10±6,7 |
Согласно таблице 2 у 18 (90±6,7%) больных основной группы носо-пищеводный зонд удален на 3-и сутки послеоперационного периода, и они переведены на питание естественным путем в сроки 2-3 суток после операции, однако при этом у 3 (15±4,9%) больных в течение 7 дней наблюдалось поперхивание жидкой пищей. В контрольной группе удаление носо-пищеводного зонда производилось в сроки 21-28 дней с момента выполнения операции.
Мы намеренно оставляли канюленосителями всех пациентов основной группы до выполнения пластического закрытия ларингостомы, так как эта операция выполнялась под эндотрахеальным наркозом и интубация больного осуществлялась через трахеостому. На 2-3-и сутки после выполнения этого этапа хирургического лечения все больные были деканулированы.
Канюленосительство в ближайшие сутки после пластики ларингостомы местными тканями позволяло добиться обеспечения достаточной санации трахеобронхиального дерева через трахеостомическую трубку и тем самым предотвратить возникновение послеоперационных осложнений со стороны дыхательной системы в виде аспирационных пневмоний. Сроки деканулирования больных основной группы приведены в таблице 3.
Таблица 3
Сроки и качество восстановления функции дыхания у больных основной группы
|
Сроки деканулирования (n=20), месяцев |
Качество дыхания |
|||
|
Дыхание свободное |
Компенсированный стеноз гортани |
|||
|
абс. ч. |
%±SE |
абс. ч. |
%±SE |
|
|
2 |
2 |
10±6,7 |
- |
- |
|
3 |
5 |
25±9,7 |
- |
- |
|
4 |
5 |
25±9,7 |
1 |
5±4,9 |
|
5 |
4 |
20±8,9 |
1 |
5±4,9 |
|
6 |
- |
- |
1 |
5±4,9 |
|
Всего |
16 |
80±8,9 |
3 |
15±8,0 |
Примечание: *SE - стандартная ошибка доли.
Таблица 3 показывает, что в сроки до 6 месяцев с момента органосохраняющей операции на гортани 16 (80±8,9%) больных основной группы были деканулированы. Функция дыхания естественным путем была компенсирована в полном объеме у 13 человек, что составило 65±10,7% от всех деканулированных больных. У 3 (15±8,0%) пациентов, соответственно, наблюдались явления компенсированного стеноза гортани. Ларингоскопически голосовая щель при этом была сужена не более чем на 30%.
Рассматривая результаты функционально-щадящих операций при раке гортани, следует учитывать, что истинные данные можно получить только при оценке уровня реабилитации основных функций гортани не ранее чем через 6 месяцев. Этот срок определяется тем, что необходимость этапных пластических операций, связанных с восстановлением структур органа (в нашем случае это пластическое закрытие ларингостомы), вызывает вынужденное запаздывание компенсации функций органа. Этот же период времени необходим для ликвидации сопутствующих воспалительных изменений в виде вялотекущих хондроперихондритов, отеков слизистой оболочки гортани, избыточного разрастания грануляционной и рубцовой ткани. Таблица 4 показывает сроки выполнения пластического закрытия ларингостомы больным основной группы.
Таблица 4
Сроки выполнения пластики ларингостомы
|
Сроки выполнения пластики (месяцев после резекции) |
Количество больных |
|
|
абс. ч. |
%±SE |
|
|
2 |
2 |
10±6,7 |
|
3 |
5 |
25±9,7 |
|
4 |
6 |
30±10,2 |
|
5 |
2 |
10±6,7 |
|
6 |
1 |
5±4,9 |
|
Всего |
16 |
80±8,9 |
Можно отметить, что максимальный срок реабилитации функций гортани подвергшихся операции на гортани по разработанной нами методике составил 6 месяцев (таблица 4).
Подводя итог нашей работы, представляем онкологические результаты лечения больных основной группы, подвергнутых органосохраняющей операции на гортани, в сравнении с результатами контрольной группы больных, пролеченных комбинированным методом с включением экстирпации гортани. У 2 (10±6,7%) больных основной группы в течение 4 и 6 месяцев возник местный рецидив, им выполнена ларингэктомия. У 1 (5±4,9) больного спустя 7 месяцев после реконструктивной операции на гортани был выявлен метастаз в региональные лимфатические узлы шеи, ему выполнена расширенная шейная лимфодиссекция.
Для оценки онкологических результатов, а, следовательно, показаний к выполнению предложенной нами методики резекции гортани с реконструкцией, мы избрали основным критерием пятилетние показатели общей кумулятивной выживаемости и бессобытийной выживаемости (метод Каплана-Мейера), представленные на рисунке 1. Под событием понимается возникновение любого из перечисленных моментов: рецидив, начало прогрессирования опухоли и смерть.
Общая кумулятивная выживаемость в группах сравнения (Kaplan-Meier) представлена на рисунке.
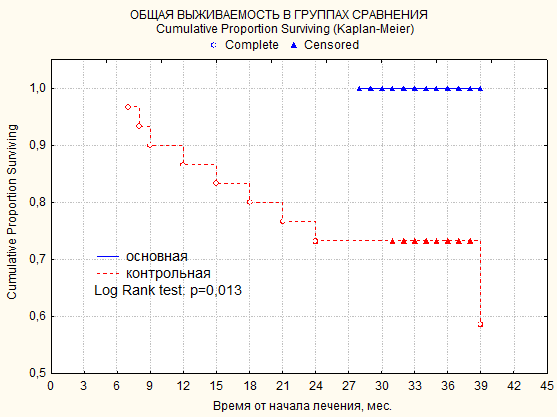
Показатели общей выживаемости больных двух групп лечения: основной (n=20) и контрольной (n=30)
В соответствии с рисунком различия статистически значимы, р=0,013 (LogRank test). Медианы выживаемости в основной группе и контрольных группах не достигнуты. 3-летняя общая выживаемость в основной группе – 100%, в контрольной группе – 73%. Средняя продолжительность жизни в контрольной группе за время наблюдения составила 29,7±1,9 месяца.
Вывод. Использование предлагаемого метода обеспечивает радикальное удаление опухоли, а также выполнение одномоментной хирургической реабилитации путем реконструкции утраченных частей гортани. Бессобытийная 5-летняя выживаемость в основной группе больных составила 80±4,5% за весь период наблюдения, в контрольной – 64±4,2%. Пластика ларингостомы (окончательный этап реконструкции гортани) выполнена в сроки до 4 месяцев 13 больным (65%), а в сроки до 6 месяцев – всем пациентам основной группы. То есть максимальный срок реабилитации функций гортани составил 6 месяцев с момента выполнения резекции гортани.
Таким образом, метод реконструктивной операции на гортани как этап комбинированного лечения демонстрирует лучшие результаты лечения и сокращение сроков реабилитации функций прооперированной гортани в сравнении с ларингэктомией.
Библиографическая ссылка
Светицкий П.В., Волкова В.Л., Аединова И.В., Чертова Н.А., Ульянова Ю.В., Баужадзе М.В. ВОЗМОЖНОСТИ ОРГАНОСОХРАНЯЮЩЕГО ЛЕЧЕНИЯ МЕСТНОРАСПРОСТРАНЕННОГО РАКА ГОРТАНИ // Современные проблемы науки и образования. – 2018. – № 6. ;URL: https://science-education.ru/ru/article/view?id=28383 (дата обращения: 23.04.2024).



