Одним из наиболее эффективных методов преодоления бесплодия, обусловленного различными факторами, в том числе и аденомиозом, в настоящее время является метод экстракорпорального оплодотворения (ЭКО) преовуляторных ооцитов и переноса эмбрионов (ПЭ) в полость матки. Результативность ЭКО зависит как от фолликулярного резерва яичника, его способности отвечать на гормональную стимуляцию, так и от зрелости и готовности эндометрия и от качества эмбрионов [1]. Успех имплантации во многом зависит от молекулярных взаимодействий между тканями и клетками эндометрия, экспрессии эффекторных молекул, факторов роста и цитокинов, осуществляющих паракринную, аутокринную и интракринную регуляцию процесса [2]. Доказано, что при аденомиозе даже ранних степеней у ряда пациенток наблюдается выраженное снижение имплантационного потенциала эндометрия [3]. Предгравидарная подготовка у пациенток с аденомиозом во многом устраняет цитокиновые дисфункции и благоприятно влияет на имплантационный потенциал эндометрия. Однако при выраженном дисбалансе цитокиновых взаимодействий иммунотропных эффектов диеногеста недостаточно, поэтому мы включили в комплекс предгравидарной подготовки к циклу ЭКО дополнительную специфическую иммунотропную терапию дезоксирибонуклеинатом натрия. Натрия дезоксирибонуклеинат обладает противовоспалительной эффективностью, иммуномодулирующим и иммунокорригирующим эффектом. Механизм иммуномодулирующего действия связывают со стимуляцией В-лимфоцитов и активацией Т-хелперов, отмечается повышение количества Т-хелперов и значение иммунорегуляторного индекса (Т-хелперы/Т-супрессоры). В процессе активирующего воздействия на фагоциты стимулируется синтез хемокинов, ангиобластных, фибробластных, эпидермальных факторов, активно участвующих в процессах имплантации, под влиянием препарата происходят изменения цитотоксической активности натуральных киллерных клеток, нормализуется баланс цитокинов IL-6/IL-10 в сыворотке крови [4], что не может опосредованно не влиять на качество имплантационного фактора эндометрия. Также многочисленными исследованиями доказано отсутствие мутагенного, тератогенного, эмбриотоксического, канцерогенного действий, аллергизирующих свойств, цитогенетических эффектов дезоксирибонуклеината натрия [5]. Препарат разрешен к применению даже во время беременности и является одним из лекарственных средств (по данным РЛС), применяемых при эндометриозе [6]. Поэтому мы предположили, что сочетание дезоксирибонуклеината натрия с диеногестом, чьи гормонопосредованные иммуномодулирующие свойства уже неоднократно освещались [7; 8], позволит взаимопотенцировать влияние на имеющийся у пациенток с аденомиозом и бесплодием цитокинозависимо сниженный имплантационный потенциал эндометрия и улучшит результативность ЭКО у пациенток с аденомиозом ранних степеней.
Цель: оценить результативность ЭКО в зависимости от вида предгравидарной подготовки у пациенток с аденомиозом 1-2 степеней и выраженным снижением цитокинзависимого имплантационного потенциала эндометрия.
Материалы и методы
Сформирована основная группа исследования, включающая 133 пациентки с бесплодием и аденомиозом 1-2 степени. Возраст женщин составил в среднем 31,2±2,1 года. Все пациентки дали информированное согласие на участие в исследовании. Исследование одобрено локальным этическим комитетом. Предварительно согласно Приказу Министерства здравоохранения РФ от 30 августа 2012 г. № 107н «О порядке использования вспомогательных репродуктивных технологий, противопоказаниях и ограничениях к их применению» проводили обследование супружеской пары в рамках подготовки к программе ЭКО с использованием общеклинических и специальных методов обследования. Когорта пациенток была сформирована согласно параметрам имплантационного потенциала, оцененного как выраженно сниженный (увеличение провоспалительного индекса периферической крови, определяемого как отношение IL1β/RAIL1*100 более 36, снижение уровня LIF цервикальной слизи менее 24,5 пг/мл при расчетном ПВИ1 цервикальной слизи, определяемого отношением IL6/IL10 более 52). Все пациентки разделены на группы согласно способу проведенной предгравидарной подготовки:
1 группа - 45 пациенток - микронизированный прогестерон с 16 по 25 день менструального цикла в течение трех циклов, предшествующих циклу ЭКО.
2 группа - 43 пациентки - диеногест в дозе 2 мг сутки в непрерывном режиме в течение трех циклов, предшествующих циклу ЭКО.
3 группа - 45 пациенток - диеногест в дозе 2 мг в сутки в течение 3 циклов и внутримышечное введение дерината в дозе 75 мг (5 мл 1,5% раствора) с интервалом 48 часов, 5 инъекций на курс, во второй фазе цикла, предшествующего фертильному с ЛГ+3.
4 группа (контроль) - 45 здоровых фертильных женщин, имеющих в анамнезе благополучную беременность и роды здоровым плодом и в данный момент наблюдавшихся по программе суррогатного материнства. Для сравнительного анализа параметров индуцированного цикла ЭКО при всех видах предгравидарной подготовки, группы были разделены на дополнительные по принципу удачной попытки ЭКО (клиническая беременность Б+) и неудачной попытки ЭКО (отсутствие клинической беременности Б-).
В качестве единого протокола для всех женщин, включенных в исследование, применяли протокол суперовуляции с первоначальным введением антагониста ГнРГ (гонал-Ф, пурегон) на 2-3 день цикла. Стартовая доза препарата составила 200 мг. Триггером овуляции послужил рекомбинантный хорионический гонадотропин, доза которого составляла 5000-10000 ЕД. Трансвагинальную пункцию (ТВП) проводили через 35-40 после введения индуктора овуляции, оплодотворение полученных ооцитов проводили через 4-5 часов после ТВП яичников. Для преинкубации, оплодотворения ооцитов и культивирования эмбрионов использовали среды для культивирования фирмы Cook Group, Inc. (США). Наличие 2 пронуклеусов через 14-16 часов после оплодотворения расценивали как успешное оплодотворение. Преимплантационную генетическую диагностику эмбрионов «хорошего» качества на 3-й и 5-й день культивирования выполняли с использованием зондов фирмы ABBOT (Vysis). Подсчет количества полученных ооцитов проводили по общепринятой шкале. Для оценки качества эмбрионов использовали классификацию J.W. Lens. К эмбрионам «хорошего» качества относили эмбрионы, содержащие 6-8 бластомеров и не более 10% фрагментации. Пациентки с неудовлетворительным качеством эмбрионов были исключены из данного исследования. Перенос эмбрионов выполняли по стандартизованной методике, при этом количество переносимых эмбрионов не превышало 2-х. Посттрансферный период вели стандартно с применением препаратов натурального прогестерона, введение которого начинали через 24 часа после ТВП, средняя доза 400 мг/сутки.
Диагностика беременности осуществлялась путем проведения исследования уровня хорионического гонадотропина в крови через 12-14 дней от момента переноса эмбрионов (биохимическая беременность) и ультразвуковым подтверждением маточной беременности на 21-23 день после переноса эмбрионов. Осуществлялось наблюдение за гестационным процессом и исходом родов с подсчетом вида и количества осложнений беременности, способа, срока и исхода родоразрешения.
Математическую обработку результатов проводили методами описательной и непараметрической статистики на персональном компьютере. Использовалась описательная статистика: частота в процентах, средняя арифметическая (М), ошибка среднего (m), среднее квадратичное отклонение (σ). Методы непараметрической статистики: Манна-Уитни, χ2, различия считали статистически значимым при p<0,05.
Результаты и обсуждение
На основании проведенного сравнительного анализа результатов индукции овуляции не было выявлено статистически значимых различий между длительностью стимуляции, средней ежедневной дозой индуктора и суммарной дозой препарата между основными и дополнительными группами. Среднее число полученных эмбрионов на пациентку составило в среднем 6,17±1,2 в «Б+» группах и 6,3±0,8 в «Б-» группах, что не имело статистически достоверной межгрупповой разницы и достоверной статистической разницы с группой контроля.
Всем пациенткам, включенным в исследование, была проведена оценка параметров раннего эмбриогенеза в программе ЭКО. На третьи сутки после оплодотворения доля эмбрионов хорошего качества группе 1Б+ составила 47,1%, а 1Б- 47,2%, в группе 2Б+ и 2Б- – 46,2% и 45,9%, в группе 3Б+и 3Б- - 45,6% и 46,2% соответственно. В контрольной группе 4Б+ и 4Б- у здоровых женщин доля эмбрионов с нормальным оплодотворением составила 46,2% и 46,8% (табл. 1)
Таблица 1
Характеристики эмбрионов 3-го дня культивирования у пациенток с аденомиозом в цикле ЭКО
|
Параметр |
1 группа, n=45 |
2 группа, n=43 |
3 группа, n=45 |
4 группа, n=45, контроль |
|||||
|
1Б+- n=8 |
1Б- n=37 |
2Б+ n=11 |
2Б- n=32 |
3Б+ n=16 |
3Б- n=29 |
4Б+ n=20 |
4Б- n=25 |
||
|
Эмбрионы хорошего качества |
% |
47,1 |
47,2 |
46,2 |
45,9 |
45,6 |
46,2 |
46,2 |
46,8 |
|
Эмбрионы удовл. качества |
% |
40,1 |
40,2 |
40,7 |
41,2 |
41,3 |
41,9 |
41 |
41,6 |
|
Эмбрионы плохого качества |
% |
12,8 |
12,6 |
13,1 |
12,9 |
12,9 |
11,9 |
12,5 |
11,4 |
Статистически достоверной разницы между группами по количеству полученных эмбрионов хорошего качества обнаружено не было. При анализе эмбрионов, остановившихся в развитии до 5-х суток культивирования, статистических различий между исследуемыми группами также выявлено не было (p>0,08). В группе пациенток с наступившей беременностью остановка эмбрионов в развитии до 5-х суток культивирования наблюдалась в среднем в 28,1% случаев, в группе женщин с отсутствием беременности – в 30,2% случаев, как у пациенток с аденомиозом, так и в группе контроля. В целом процент оплодотворения составил 74,3% и достоверно по основным и дополнительным группам не различался. Всем пациенткам основных и контрольной групп было перенесено по 2 эмбриона хорошего качества.
Таким образом, по данным нашего исследования, у пациенток с аденомиозом ранних степеней по сравнению с фертильными здоровыми женщинами отсутствовали статистически значимые отклонения в фолликуло- и эмбриогенезе, которые могли бы повлиять на частоту удачных попыток ЭКО.
Сравнительный анализ результативности ЭКО показал, что, несмотря на отсутствие статистической разницы параметров эмбриогенеза, частота наступления биохимической беременности была статистически значимо ниже в 1-й группе - 22,2%, по сравнению с группой контроля - 46,6%, р<0,01. Во 2-й группе, при проведении предгравидарной подготовки диеногестом, биохимическая беременность состоялась у 12 женщин (27,9%), что составило статистически значимую положительную разницу с 1-й группой, но при этом относительно группы контроля показатель наступления биохимической беременности был статистически значимо ниже, р<0,01. Такая же тенденция прослеживалась при анализе частоты имплантации и наступления клинической беременности (рисунок).
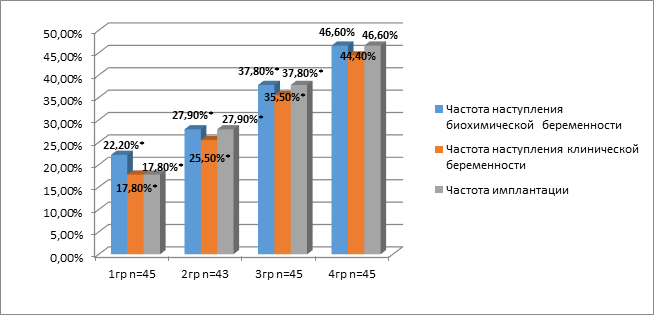
Характеристики раннего эмбриогенеза, результативности ЭКО и исходов гестации у пациенток с аденомиозом в зависимости от вида предгравидарной подготовки
Примечание: символ «*» соответствует статистически значимому различию показателей по сравнению со средними значениями аналогичных показателей в контроле, р<0,05.
При проведении сочетанной предгравидарной подготовки дезоксирибонуклеинатом натрия и диеногестом у пациенток с максимально сниженным имплантационным потенциалом (3-я группа) частота биохимической беременности достигла 37,7%. Частота наступления клинической беременности у пациенток 3-й группы составила 35,5%, что максимально приблизилось к показателям контрольной группы и соответствовало средней частоте наступления клинической беременности от переноса, по данным отчета РАРЧ за 2015 год. Частота имплантации 37,8% и живорождения 35,5% при проведении предгравидарной подготовки диеногестом и дезоксирибонуклеинатом натрия также существенно превышала соответствующие показатели в 1-й и 2-й клинических группах, соответствуя средним показателям, представленным в отчете РАРЧ - 37,6%, и приближалась к показателям контрольной группы (табл. 3).
При анализе течения гестационного процесса и исхода родов выявлено, что в группе контроля беременность завершилась срочными родами у 20 (44,4%) пациенток, в том числе двойня. Преждевременных родов и выкидышей в контрольной группе не было, родилось 20 детей, то есть частота живорождения составила 46,6% (табл. 2)
Таблица 2
Сравнительная характеристика исходов гестации у пациенток с аденомиозом в цикле ЭКО
|
Исход беременности и родов |
1 группа, n=45 |
2 группа, n=43 |
3 группа, n=45 |
4 группа - контроль, n=45 |
Данные отчета РАРЧ за 2015 г. |
|
|
Клиническая беременность |
Абс. |
8* |
11* |
16* |
20 |
|
|
% |
17,8* |
25,5* |
35,5* |
44,4* |
37,6 |
|
|
Частота живорождения |
Абс. |
5* |
10* |
16* |
20 |
|
|
% |
11,1 |
23,2 |
35,5* |
44,4 |
||
|
Родов всего: |
6 |
9 |
13* |
20 |
||
|
13,3 |
20,9 |
28,8* |
44,4 |
27,5 |
||
|
Роды в срок/доля срочных родов |
4 |
6 |
11* |
18 |
||
|
66,6 |
66,6 |
84,6* |
90 |
79,9 -90,1% |
||
|
Из них: естественные роды |
Абс. |
2* |
4* |
6* |
14 |
|
|
% |
50* |
66,6* |
50* |
77,7 |
||
|
Из них: к/сечение |
Абс. |
2* |
2* |
5* |
4 |
|
|
% |
50* |
33,3* |
50* |
22,2 |
||
|
Двойни |
Абс. |
- |
1* |
1* |
1 |
|
|
% |
2,3* |
2,2* |
2,2 |
|||
|
Замершая беременность |
Абс. |
0 |
1* |
1* |
0 |
|
|
% |
0 |
2,3* |
2,2* |
0 |
||
|
Самопроизвольный выкидыш |
Абс. |
1* |
0 |
0 |
0 |
|
|
% |
2,2* |
0 |
0 |
|||
|
Очень ранние преждевременные роды |
Абс. |
1* |
0 |
0 |
||
|
% |
2,2* |
0 |
0 |
|||
|
Ранние преждевременные роды |
Абс. |
0 |
0 |
0 |
||
|
% |
0 |
0 |
0 |
|||
|
Преждевременные роды |
Абс. |
1* |
4* |
2* |
1* |
|
|
% |
2,2* |
9,3* |
2,2* |
3,5* |
||
Примечание: символ «*» соответствует статистически значимому различию показателей по сравнению со средними значениями аналогичных показателей в контроле, р<0,05.
В 1-й группе беременность завершилась родами в доношенном сроке у 4 (50,%) пациенток. У 1 (2,2%) пациентки состоялись преждевременные роды в сроке 34-35 недель, у 1 (5,8%) - очень ранние преждевременные роды на сроке 25 недель. Всего в 1-й группе родилось 5 (11,1%) условно здоровых детей. Совокупные потери беременности составили 4,4% - 1 самопроизвольный выкидыш на сроке 7-8 нед, и 1 - очень ранние преждевременные роды (ребенок умер на 3 сутки после родов).
Во 2-й группе беременность завершилась родами у 9 (20,9%) пациенток, роды в срок составили 18,6%, преждевременные роды – 9,3%, в том числе двойней на сроке 34 недели, в итоге родилось 10 детей (23,2%). Потери беременности составили 2,3% - 1 замершая беременность в сроке 7-8 недель.
Наиболее позитивные результаты показали пациентки 3-й группы (ПГП диеногест + дезоксирибонуклеинат натрия). Частота наступления клинической беременности у них составила 35,5%, частота живорождения – 35,5%. Имели место одни преждевременные роды в сроке 35 недель (двойня). Имела место 1 (2,2%) замершая беременность на сроке 12 недель.
Известно, что течение беременности у пациенток после ЭКО характеризуется высокой частотой развития акушерской патологии и невынашивания беременности, что может нивелировать успех репродуктивных технологий [9]. В нашем исследовании также отмечено высокое статистически значимо отличающееся от группы контроля (р<0,005) увеличение частоты угрозы прерывания беременности, часто сопровождающейся возникновением ретрохориальной гематомы (23,5%) у пациенток с аденомиозом 1 и 2 степени, которым использовался стандартный протокол (35,5% против 5% в контроле) (табл. 3).
Таблица 3
Сравнительная характеристика течения беременности исходов гестации у пациенток с аденомиозом в цикле ЭКО
|
Осложнения беременности |
1 группа, n=45 |
2 группа, n=43 |
3 группа, n=45 |
4 группа - контроль, n=45 |
|
|
Угрожающий с/выкидыш |
Абс. |
8* |
5* |
2* |
1 |
|
% |
100* |
45,5* |
12,5* |
5 |
|
|
Ретрохориальная гематома |
Абс. |
4* |
4* |
2* |
1 |
|
% |
50* |
36,3* |
12,5* |
5 |
|
|
Угрожающие преждевременные роды |
Абс. |
6* |
4* |
3* |
1 |
|
% |
75* |
36,3* |
18,7* |
5 |
|
|
Маловодие |
Абс. |
5* |
3* |
2* |
1 |
|
% |
62,5* |
27,2* |
12,5* |
5 |
|
|
Многоводие |
Абс. |
1* |
1* |
0 |
0 |
|
% |
12,5* |
9,9* |
0 |
0 |
|
|
СЗРП |
Абс. |
3* |
1* |
0 |
0 |
|
% |
37,5* |
9,0* |
0 |
0 |
|
|
Преэклампсия |
Абс. |
1* |
0 |
0 |
0 |
|
% |
12,5* |
0 |
0 |
0 |
|
Примечание: символ «*» соответствует статистически значимому различию показателей по сравнению со средними значениями аналогичных показателей в контроле, р<0,05.
Частота плацентарной недостаточности у пациенток 1-й группы составила 75% с выявлением маловодия (62,5%) и задержки внутриутробного развития в 37,5%, что статистически высоко значимо превышало частоту данных осложнений у пациенток контрольной группы (маловодие - 5%) (р<0,005). Умеренной преэклампсией гестационный процесс у пациенток 1-й группы осложнился у 1 (12.5% случаев) беременности. У пациенток, получивших в качестве предгравидарной подготовки диеногест (2-я группа), процент осложнений беременности был достоверно ниже (р<0,005), чем в 1-й клинической группе, но не достигал показателей группы контроля. Наиболее часто беременность у них осложнялась плацентарной недостаточностью (45,5% против 5% в группе контроля) с развитием СЗРП в 1 (9,0%) случае (табл. 4).
При применении сочетанной предгравидарной подготовки (дезоксирибонуклеинат натрия и диеногест) – 3-я группа - гестационный процесс протекал с минимальным количеством осложнений по сравнению с пациентками 1 и 2 клинических групп. Так, угрожающий самопроизвольный выкидыш у них регистрировался в 12,5% случаев, угрожающие преждевременные роды в 18,7%, плацентарная недостаточность с развитием маловодия в 12,5%, случаев СЗРП отмечено не было.
Оценка доношенных новорожденных по шкале АПГАР не выявила достоверных различий между клиническими группами и группой контроля, а также выраженных межгрупповых различий. Так, в 1-й группе новорожденные на первой минуте были оценены на 7,4±1,3 балла, во 2-й группе 7,6±1,2 балла, в 3-й группе 7,8±1,6 балла, при показателях группы контроля 7,8±1,1 балла. На пятой минуте также достоверных различий с группой контроля и межгрупповой разницы выявлено не было (1-я группа - 8,5±1,3 балла, 2-я группа - 8,4±1,4 балла, 3-я группа 8,3±1,8 балла). Средний вес детей по группам составил: в 1-й группе 3100,±400,0, во 2-й группе 3250,0±150,0, в 3-й группе - 3150±200,0 и в группе контроля 3400±300,0.
Таким образом, у пациенток с аденомиозом на фоне предгравидарной подготовки микронизированным прогестероном наблюдалось статистически значимое снижение частоты зачатия и живорождения (χ2, р=0,059) и статистически значимое увеличение частоты осложнений беременности по сравнению с группой контроля (χ2, р=0,062). На фоне предгравидарной подготовки диеногестом (2 группа), показатели зачатия и живорождения статистически значимо увеличивались (χ2, р=0,062), а частота осложнений гестационного процесса достоверно значимо уменьшалась относительно 1 группы, однако показатели не достигали таковых в группе контроля. На фоне предгравидарной подготовки (3 группа) с параллельным применением диеногеста и иммуномодуляцией дезоксирибонуклеинатом натрия отмечались наиболее высокие, максимально приближающиеся к показателям группы контроля (4 группа) и среднестатистическим показателям отчета РАРЧ частота зачатия и живорождения, при этом выявлено минимальное (для пациенток с аденомиозом и ЭКО) количество осложнений беременности.
Таким образом, изолированное применение диеногеста в качестве препарата для предгравидарной подготовки у пациенток с аденомиозом позволило улучшить результативность методов ЭКО у части пациенток. Однако при наличии у пациенток с аденомиозом выраженного снижения имплантационного потенциала к улучшению результативности ЭКО привела лишь патогенетически обоснованная сочетанная терапия диеногестом и дезоксирибонуклеатом натрия. Проведенный анализ в целом показал, что пациентки с аденомиозом, даже в случае удачной попытки ЭКО, относятся к группе высокого риска по развитию акушерской и перинатальной патологии. Аденомиоз, снижая качество имплантационного фактора, ведет к развитию первичной хориальной и вторичной плацентарной недостаточности, что приводит к развитию различных осложнений беременности, повышает риск невынашивания и неонатальной заболеваемости. Таким образом, совершенно очевидна необходимость индивидуального ведения пациенток с бесплодием, ассоциированным с аденомиозом даже ранних степеней, что в свою очередь приведет к уменьшению осложнений во время беременности и улучшению перинатальных исходов.
Библиографическая ссылка
Куценко И.И., Авакимян В.А., Кравцова Е.И., Батмен С.К. ОЦЕНКА ЭФФЕКТИВНОСТИ ЭКО, ТЕЧЕНИЯ БЕРЕМЕННОСТИ И ИСХОДА РОДОВ В ЗАВИСИМОСТИ ОТ ВИДА ПРЕДГРАВИДАРНОЙ ПОДГОТОВКИ ПРИ АДЕНОМИОЗЕ 1-2 СТЕПЕНИ С НИЗКИМ ИМПЛАНТАЦИОННЫМ ПОТЕНЦИАЛОМ ЭНДОМЕТРИЯ // Современные проблемы науки и образования. – 2018. – № 4. ;URL: https://science-education.ru/ru/article/view?id=27779 (дата обращения: 20.04.2024).



