В системе стресс-лимитирующих механизмов определенное место занимают антиоксидантные факторы неспецифической защиты [1,2], в частности, при кровопотерях [3,4]. В целях выяснения характера неспецифического действия на систему крови относительно низких концентраций химических веществ с антиокислительными свойствами, нами изучалось влияние гидроксиметил-1,3-диоксалана (ГМД) на организм. Препарат ГМД (молекулярная формула: С4 Н6О4; молекулярный вес-118,09) относится к группе ацеталей [5], которая применяется в парфюмерной промышленности. Известно, что при действии химических реагентов имеет значение характер исходного состояния организма. В связи с этим нами применялась одна и та же доза ГМД в интактном состоянии животных и в условиях гипоксии. Одновременно была выявлена и доза ГМД, которая оказывала положительное действие при стресс-состоянии, вызванном постгеморрагической анемией.
Материал и методы исследования
В качестве гипоксии использовалась экспериментальная модель – постгеморрагическая анемия, которая вызывалась путем одномоментной некомпенсированной кровопотери. Кровопускание производилось из краевой ушной вены кроликов породы «Шиншилла» способом надреза из расчета 20 % от массы крови. Общее количество крови в организме кролика определялось исходя из массы тела (5,4 %). Экспериментальные животные получали небольшие дозы препарата внутримышечно в течение 10 дней ежедневно. В совокупности были составлены следующие группы: I-группа: вводилась доза ГМД равная 100 мг/кг до кровопотери (п=10). II-группа: вводилась доза ГМД равная 100 мг/кг после кровопускания (п=10). III-группа: вводилась доза ацетат-токоферола (вит. Е) равная 10 мг/кг после кровопускания (п=10). IV – группа: доза ГМД равная 20 мг/кг после кровопускания (п=10). V – группа: животные после кровопотери (контроль) (п=10).
Используемые концентрации ГМД были ориентированы наустановление эффекта в трех позициях: 1 – интактная доза в норме (100 мг/кг), 2 – токсическая доза при кровопускании (100 мг/кг), 3 – корректирующая доза при кровопускании (20 мг/кг). Применение ацетата-токоферола была направлена на определение возможности использования антиоксидантов в стресс-состояниях, а также для сравнительной оценки действия на организм ГМД в дозе 20мг/кг.
Исследование крови производилось в исходном состоянии и через 1, 3, 5, 7, 9, 10 суток при ежесуточной инъекции изучаемого вещества. Концентрация форменных элементов определялась при помощи гематологического анализатора марки «Максим». Установление статистической достоверности различий количественных показателей проводилось параметрически по t-критерию Стьюдента по программе М. Exell («статистика»).
Результаты исследования и их обсуждение
Количественные параметры периферической крови V-группы (контрольной) анемизированных животных в динамике составляли следующие средние значения (табл.1, рисунок). Максимальные показатели эритоцитопении наблюдались через 3 суток. В последующие сроки наблюдения уровень эритроцитопении уменьшался. Для большей наглядности был выведен показатель дефицита эритроцитов, который соответствовал
Таблица1
Сводные данные крови кроликов после кровопотери (М±m; n-10; * – Р<0,05 в сравнении с исходным уровнем)
|
Показатели крови |
Исходный уровень |
Ч Е Р Е З |
||||
|
1 сут |
3 сут |
5 сут |
7 сут |
10 сут. |
||
|
Эритроциты.(х10 12/л |
4,7±0,09 |
3,4±0,10* |
3,1±0,07* |
3,3±0,08* |
3,8±0,09* |
3,9±0,10* |
|
Лейкоциты.(х10 9/л) |
6,5±0,12 |
3,6±0,17* |
2,2±0,15* |
3,3±0.19* |
4,7±0,17 |
4,3±0,18* |
|
Гемоглобин (г%) |
10,3 |
3,7 |
5,1 |
6,5 |
6,8 |
7,1 |
|
Тромбоциты.(х10 9/л-) |
361,2 ±6,1 |
305.4±6,3* |
262,7±6,5* |
292,0±5,8* |
309,9±5,7* |
260,0±5,8* |
|
Дефицит эритроцитов (х10 12/л) |
- |
1,3±0,08* |
1,6±0,09* |
1,4±0,07* |
0,9±0,06* |
0,8±0,09* |
|
Дефицит гемоглобина (г%) |
- |
6,6±0,19 |
5,2±0,17* |
3,8±0,19* |
3,5±0,19* |
3,2±0,16* |
|
Величина лейкопении (х10 9/л) |
- |
2,9±0,16* |
4,3±0,18* |
3,2±0,19* |
1,8±0,21* |
2,2±0,19* |
|
Дефицит тромбоци-тов (х10 9/л) |
- |
55,8±7,5* |
98,5±7,1 |
69,2±7,5* |
51,3±6,3* |
101,2±6,1* |
|
Ретикулоциты (%о) |
28,1 |
29,5±0,53 |
35,1±0,59* |
38,5±0,61* |
44,5±0,64* |
36,1±0,51* |
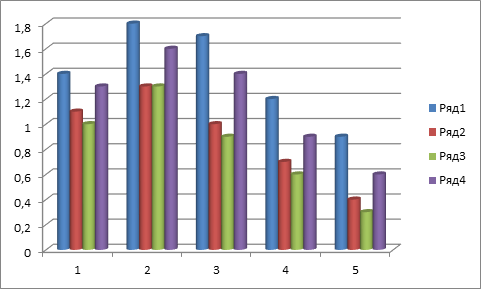
Показатели величины дефицита эритроцитов (х1012).
Ряд 1. При введении ГМД 100 мг/кг после кровопотери.
Ряд 2. При введении ГМД 20 мг/кг после кровопотери.
Ряд 3. При введении ацетат-токоферола 10 мг/кг после кровопотери.
Ряд 4. Состояние после кровопотери без вмешательств.
1 – после 1 сут; 2 – после 3 сут; 3 – после 5 сут; 4 – после 7 сут; 5 – после 10 сут
разнице между числом эритроцитовв исходном уровне и числом эритроцитов в конкретный срок исследования после кровопускания. Естественно, наибольшее среднее значение рассматриваемого показателя наблюдалось через 3 сутки после кровопотери. В последующие сроки происходило постепенное уменьшение среднего значения этого показателя. В условиях кровопотери определенные сдвиги наблюдались и со стороны ретикулоцитов крови. Исходное количество их перед кровопотерей равнялось в среднем 28,1 %о. В период после кровопотери значение этого показателя прогрессирующим образом повышалось и на 10 сутки достигло 31, 6%о, отражая эритропоэтическую активность. Динамика изменений общего количества гемоглобина крови была аналогична сдвигам количества эритроцитов. Однако в отличие от показателей дефицита эритроцитов максимальное значение гипогемоглобинемии наблюдалось через 3 суток после кровопотери, что, конечно, связано с фактом компенсаторного разжижения крови после кровопотери. В последующие сроки после кровопускания происходило постепенное повышение содержания гемоглобина. Динамика лейкопении после кровопотери имела аналогичную направленность характеру эритроцитопении.
Наименьшее среднее значение количества лейкоцитов наблюдалось на 3 сутки после кровопотери. Для большей наглядности был выведен показатель – «величина лейкопении», то есть разница между исходным показателем лейкоцитов и через определенные сроки после кровопотери. Понятно, максимальное среднее значение величины лейкопении соответствовало 3 суткам после кровопотери.
Количество тромбоцитов в исходном состоянии составляло в среднем 361, 2 х 109/л. Динамика тромбоцитопении в постгеморрагический период имела волнообразный характер. Наибольшие значения дефицита тромбоцитов соответствовали 3 и 10 суткам после кровопускания (табл. 1).
С целью установления последствия одних и тех же доз химических реагентов в интактном состоянии животных и при присутствии стресс-реакции была введена доза ГМД, равная 100мг/кг животным после кровопускания и контрольной группе кроликов без кровопотери. При введении интактным животным данной дозы статистически достоверных сдвигов со стороны форменных элементов крови не было выявлено. При введении ГМД в той же концентрации после кровопускания были зарегистрированы вполне достоверные гематологические сдвиги негативного характера (табл. 2).
Таблица 2
Сводные данные крови кроликов при введении ГМД -100 мг/кг после кровопотери (М ±m; n-10; * – Р< 0,05 в сравнении с уровнем 1 сут)
|
Показатели крови |
ЧЕРЕЗ |
||||
|
1 сут |
3 сут |
5 сут |
7 сут |
10 сут |
|
|
Дефицит эритрона (х1012/л) |
1,3±0,024 |
1,6±0,027* |
1,4±0,025* |
0,9±0,021* |
0,6±0,0170 |
|
Дефицит эритрона (х1012/л) – ГМД |
1,4±0,025 |
1,8±0,028* |
1,7±0,026* |
1,2±0,027* |
0,9±0,023* |
|
Дефицит гемоглобина (г%) |
4,6±0,09 |
5,2±0,10* |
3,8±0,07* |
3,5±0,07* |
2,9±0,06 |
|
Дефицит гемоглобина (г%) – ГМД |
4,9±0,10 |
5,8±0,12* |
4,4±0,11* |
4,1±0,08* |
3,4±0,07* |
|
Дефицит тромбоцитов (х109/л) |
55,4±1,3 |
98,5±1,4* |
69,2±1,6* |
51,3±1,2* |
34,8±1,1* |
|
Дефиц. тромбоцитов (х109/л) – ГМД |
78,9±1,4 |
125,0±1,5* |
89,6±1,6* |
91,1±1,3* |
86,8±1,3* |
|
Уровень лейкопении (х109/л) |
2,9±0,06 |
4,3±0,08* |
3,2±0,07* |
1,8±0,05 |
2,5±0,09* |
|
Уровень лейкопении (х109л) – ГМД |
3,4±0,07 |
6,1±0,09* |
5,9±0,06* |
6,2±0,08* |
5,8±0,08* |
|
Показатель и индекс «вторичной анемизации» (х1012 /л) |
0,36 (8.2%) |
0,68 (14,7%) |
0,48 (10.4%) |
0,0 |
0,0 |
|
Показатель и индекс «вторичной анемизации» (х1012/л) –ГМД |
0,38 (8.2%) |
0,72 (15,6%) |
0,68 (14,7%) |
0,51 (11,0%) |
0,52 (11,3%) |
Был установлен более высокий уровень дефицита эритрона по сравнению с показателями анемизированных животных без дополнительного введения ГМД во всех сроках наблюдения максимально выраженными значениями через 1 сутки после кровопотери. Отрицательный характер действия ГМД в дозе 100 мг/кг, который усугублял тяжесть состояния после кровопотери, отражался и в значениях так называемого показателя – «вторичной анемизации», то есть в разнице между величиной кровопотери, дефицитом числа эритроцитов в конкретный срок исследования. Одновременно усилились негативные сдвиги и со стороны лейкоцитов и тромбоцитов при комплексном действии ГМД (100 мг/кг) и кровопотери (табл. 2).
В то же время ГМД в другой значительно низкой дозировке в условиях постгеморрагической анемии оказывал благоприятный эффект. Так, при введении ГМД в концентрации 20 мг/кг после кровопотери снизился уровень дефицита эритрона, гемоглобина, тромбоцитов, лейкопении, показателя «вторичной анемизации» по сравнению с данными животных, которым после кровопускания не вводили ГМД (табл. 3, рис.).
Таблица 3
Сводные показатели крови кроликов при введении ГМД (20 мг/кг) и ацетат-токоферола (вит. Е) (10 мг/кг) после кровопотери (М±m; n-10; * – р<0,05 в сравнении с данными через 1 сут)
|
Показатели крови |
ЧЕРЕЗ |
||
|
1 сут |
5 сут |
10 сут |
|
|
Дефицит эритрона (х1012л) |
1,3±0,024 |
1,4±0,025* |
0,6±0,017* |
|
Дефицит эритрона(х1012л)-ГМД |
1,1±0,019 |
1,0±0,017 |
0,4±0,011* |
|
Дефицит эритрона (х1012л) – вит. Е |
1,0±0,016 |
0,9±0,0015* |
0,3±0.011* |
|
Дефицит гемоглобина (г%) |
4,6±0,09 |
3,8±0,07* |
2,9±0,06* |
|
Дефицит гемоглобина (г%) – ГМД |
3,6±0,07 |
3,4±0,05* |
2,3±0,04* |
|
Дефицит гемоглобина (г%) – вит. Е |
3,5±0,06 |
3,2±0,05* |
2,1±0.04* |
|
Ретикулоциты (%о) |
29,5±0,53 |
38,5±0,61* |
36,1±0,51* |
|
Ретикулоциты (%о) –ГМД |
37,1±0,54 |
39,3±0,61* |
32,2±0,54* |
|
Ретикулоциты (%о) – вит. Е |
38,6±0,61 |
39,6±0,62 |
31,8±0,48* |
|
Дефицит тромбоцитов (х109 /л) |
55,4±1,3 |
2,3±0,04* |
34,2±1,1* |
|
Дефицит тромбоц. (х109 /л)-ГМД |
44,1±0,9 |
1,0 |
29,1±0,6* |
|
Дефицит тромбоц. (х109 /л)-вит.Е |
43,4±1,1 |
0,9 |
26,7±0,5* |
|
Уровень лейкоцитопении (х109 /л) |
2,9±0,06 |
3,2±0,07* |
2,5±0,04* |
|
Уровень лейкоцитопении (х109 /л) – ГМД |
2,0±0,05 |
2,2±0,04* |
1,4±0,03* |
|
Уровень лейкоцитопении (х109 /л) – вит. Е |
1,2±0,05 |
2,3±0,03* |
1,6±0,02* |
Более значительное содержание ретикулоцитов в крови при введении ГМД 20 мг/кг после кровопускания, вероятно, отражало благоприятный эффект на гемопоэз. В целом степень положительного эффекта дозы ГМД, равной 20 мг/кг, была близка к характеру положительного действия при введении ацетата-токоферола после кровопускания (табл. 3). Коэффициент парной корреляции (r) данных дефицита эритроцитов на сроке через 3 суток после кровопускания при введении животным (4 – группа) ГМД (20 мг/кг) и животным (5 – группа) ацетат-токоферола (10 мг/кг) равнялся 0,8965, что больше 0, 707 (по таблице граничного значения коэффициента корреляции для 5 %-ного уровня значимости). Следовательно, связь между положительным эффектом ГМД (20 мг/кг) и ацетата-токоферола (10мг/кг) достоверна (табл. 4).
Таблица 4
Показатели парной корреляции между данными дефицита эритрона через 3 суток после кровопотери при введении ГМД (20мг/кг) и ацетат-токоферола (10 мг/кг) исходя из количества эритроцитов (х1012/л)
|
C |
D |
F |
G |
H |
I |
J |
|
2,55 |
3,2 |
-0,46 |
-0,51 |
0,2116 |
0,2601 |
0,2346 |
|
2,57 |
3,5 |
-0,44 |
-0,21 |
0,1936 |
0,0441 |
0,0924 |
|
2,77 |
3,36 |
-0,24 |
-0,35 |
0,0576 |
0,1225 |
0,084 |
|
2,88 |
3,7 |
-0,13 |
-0,01 |
0,0169 |
1E-04 |
0,0013 |
|
2,92 |
3,58 |
-0,09 |
-0,13 |
0,0081 |
0,0169 |
0,0117 |
|
2,98 |
3,6 |
-0,03 |
-0,11 |
0,0009 |
0,0121 |
0,0033 |
|
3,29 |
3,78 |
0,28 |
0,07 |
0,0784 |
0,0049 |
0,0196 |
|
3,35 |
3,88 |
0,34 |
0,17 |
0,1156 |
0,0289 |
0,0578 |
|
3,39 |
4,2 |
0,38 |
0,49 |
0,1444 |
0,2401 |
0,1862 |
|
3,4 |
4,3 |
0,39 |
0,59 |
0,1521 |
0,3481 |
0,2301 |
|
|
|
|
|
0,9792 |
1,0778 |
0,921 |
|
|
|
|
|
|
|
|
|
3,01 |
3,71 |
|
|
|
r-0,8965 |
|
Выводы
1. Введение ГМД (100 мг/кг) внутримышечно ежедневно в течение 10 суток достоверных изменений со стороны форменных элементов крови не выявило. Однако введение такой же концентрации ГМД в таком же режиме, но в условиях однократного кровопускания приводило к усилению проявлений постгеморрагической анемии.
2. Введение ГМД20 мг/кг ежедневно в течение 10 дней после кровопотери снижало уровень изменений со стороны форменных элементов крови. Уровень корреляции ГМД в 20 мг/кг по степени и характеру проявлений был близок таковой при использовании ацетата-токоферола в дозе 10 мг/кг.
Библиографическая ссылка
Хисамов Э.Н., Еникеев Д.А., Еникеев О.А., Идрисова Л.Т. КОРРЕКЦИЯ ПОСТГЕМОРРАГИЧЕСКОЙ АНЕМИИ ГИДРОКСИМЕТИЛ-1,3-ДИОКСАЛАНОМ // Современные проблемы науки и образования. – 2017. – № 6. ;URL: https://science-education.ru/ru/article/view?id=27145 (дата обращения: 25.04.2024).



