В настоящем сообщении представляются некоторые результаты 24-летнего применения в клинической нейрокардиологии неинвазивного метода ритмокардиографии высокого разрешения (РКГ) для диагностики периферических вегетативных дизрегуляций синоатриального узла сердца (СУ) на основе анализа вариабельности сердечного ритма (ВСР) и оценки различных вариантов изменчивости волновой структуры межсистолических интервалов [1-3]. Актуальность исследования и адаптации метода в практической медицине обосновывались необходимостью ранней диагностики сердечно-сосудистых заболеваний (ССЗ) в периоде их обратимости и вегетативных нарушений, являющихся фоном для многих болезней. В этом отношении оправдан был поиск инструментального выявления дизрегуляций основной сократительной деятельности сердца. Прежде всего, автономной регуляции пейсмекерной активности СУ сердца, являющегося главным пейсмекером первого порядка, регулируемого двумя отделами вегетативной (автономной) системы, а также гуморально-метаболической средой. Симпатический и парасимпатический отделы автономной системы обеспечивают быстрое изменение частоты сокращений сердца за счёт изменений временных систолических интервалов. Они, в свою очередь, сочетаются с автоматическими возбуждениями пейсмекерных клеток СУ под регулирующим влиянием автономной системы с её двумя отделами - симпатическим и парасимпатическим. В организме человека есть филогенетически более древний регулирующий фактор, медленный, недостаточный, иногда неадекватный – гуморально-метаболическая среда в крови, лимфе, внеклеточном гуморе. Она воздействует на пейсмекеры СУ, участвуя в формировании медленных потенциалов действия в них, но в норме преобладает быстрая автономная регуляция [1-4]. При ССЗ с автономной дизрегуляцией гуморальная среда может стать ведущей вплоть до образования автономной кардионейропатии (АКН) с предельно выраженным угнетением симпато-парасимпатического воздействия и соответственно повышением гуморально-метаболического. Зарубежные коллеги, изучающие ВСР, этот фактор регуляции не учитывают [5-9], хотя в классической физиологии его роль считается обоснованной и хорошо изученной в лаборатории нейрогуморальной регуляции при медицинском университете им И.М. Сеченова. В результате неучёт гуморального влияния на пейсмекеры СУ приводит к ошибочным суждениям, что в клинической диагностике неприемлемо.
Материалы и методы. До интервенционной реваскуляризации миокарда методом аортокоронарного и маммарокоронарного шунтирования были обследованы 256 пациентов со стабильной стенокардией. Помимо стандартных методов обследования (ЭКГ, ЭКГ с субмаксимальной нагрузкой, ХМ, ЭхоКГ, КАГ, лабораторное определение тропонина и КФК), несколько раз в процессе наблюдения применялась РКГ со статистическим временным и спектральным анализом ВСР с возможными для пациента нагрузочными вегетативными пробами. Данные до операции сопоставлялись с контролем из 47 здоровых лиц, гендерно и по возрасту совместимых с основной группой исследования. РКГ здорового человека представлена на рис. 1.
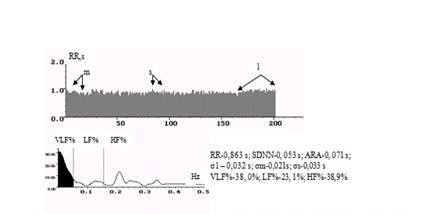
Рис. 1. Ритмокардиограмма, спектрограмма и цифровые значения показателей ВСР у здорового мужчины группы контроля. Показаны симпатические (m), парасимпатические (s) и гуморально-метаболические (l) волны ВСР. Автономные колебания (σm+σs) преобладают по амплитуде над амплитудой гуморально-метаболических флуктуаций –σl. В спектральном соотношении факторов регуляции в СУ доля автономного воздействия наибольшая - LF%+ HF% (52%) - белая часть спектра. Установлено наименьшее гуморальное влияние (VLF%-38%) на пейсмекеры СУ, судя по спектрограмме (LF%+HF%> VLF%)
Из 256 пациентов со стабильной стенокардией (СтСт) на шунтирование направлены 123. РКГ-данные прооперированных больных сопоставлялись с исходными до операции, во время и после неё. Инновационному применению в практике РКГ предшествовала разработка специализированного аппаратно-программного компьютерного комплекса (АПК) для РКГ с анализом ВСР, а также сопоставление РКГ-результатов с данными стандартных обследований больных. Результаты применения РКГ убеждают в неотвратимости ВСР-диагностики, её информативности и перспективах для выявления начала и фона дизрегуляторных нарушений, интранозологической диагностики клинических вариантов ССЗ на основе отклонений ВСР от нормы.
Методологическая основа анализа ВСР и его математическое обеспечение фрагментированно создавались результатами отечественных и зарубежных физиологических исследований Д. Жемайтите (1989), M. Malik (1995), A.J. Camm (1995), A. Malliani (1996, 1998) и многих других. Метод же с клинической интерпретацией ВСР-данных удалось приоритетно разработать и апробировать с положительным результатом в лечебных учреждениях Урала [1-3; 5; 6]. РКГ позволяет осуществлять неэтиологическую, интранозологическую диагностику кардиоваскулярной патологии, поскольку большинство ССЗ начинается с нарушений регуляции функций. Но по совокупности достаточно точных данных ВСР-анализ определяет направление этиологического поиска.
Сокращения сердца потенцируются автоматически возбудимыми пейсмекерными Р-клетками СУ, которые регулируются двумя отделами автономной системы по закону акцентированного антагонизма, а также гуморально-метаболической внеклеточной средой [1; 2]. Необходимым условием для корректной клинической интерпретации является точность съёма электрокардиосигнала (ЭКС) с дискретизацией в 1000±3 Гц, с такой же точностью данные хранятся в оперативной памяти компьютера, анализ также ей соответствует. Извлечение интервалов из Холтеровского мониторирования такой точности не предоставляет, поскольку дискретизация для технологии записи ЭКГ в течение суток ниже требуемой для РКГ. База данных за 24 года более чем в 70 тысяч обследований свидетельствует о необходимости соблюдения названной точности. Хотя и она не предел. Исходно обследование проводилось в лаборатории нейрокардиологии с помощью специализированного аппаратно-программного комплекса компьютерной ритмокардиографии КАП-РК-01-«Микор», который создавался авторами метода в течение 8 лет для 300-интервальных записей. АПК является базовой моделью для линейки приборов для РКГ и рекомендован МЗ РФ и Федеральным агентством по надзору в сфере здравоохранения (Рег. удостоверение № ФС 022б2005/2447-06,ТУ-9441-002-21569106-2005). Комплекс состоит из портативного внешнего прибора – преобразователя ЭКС- ПРКГ-01 со схемно-техническими фильтрами разночастотных помех и усилителями ЭКС перед подачей в компьютер, оснащённый специальной программой «Микор» для математического анализа ВСР. ПРКГ-01 и корректная программа обеспечивают точность регистрации ЭКС и анализ в 1 миллисекунду. Запись из-за высокой чувствительности осуществлялась в строго стационарных контролируемых условиях и производилась с применением клинико-экспериментального метода в фоне и в различно направленных 4 стимулирующих пробах. Программа содержит приемы автоматизированной обработки на 5 стационарных постстимульных ритмокардиограммах (РКГ) по 260-300 интервалов в покое и в пробах, итого 1500-1800 интервалов при 20-25-минутной регистрации (Миронова Т.Ф., Миронов В.А., 1998).
Физиологической основой РКГ является оценка 3 выше названных факторов регуляции волновой структуры межсистолических RR-интервалов ВСР по математической характеристике трех видов флуктуаций определенных частоты и периодичности [10; 11]. В отдельных случаях помогает визуально – логическая оценка, например при АКН. Волны формируются в соответствии с различиями скорости проведения импульсов по вегетативным волокнам (Warner H, 1962), а также в зависимости от колебаний концентраций полувыведения активных веществ в тканевых биосредах, влияющих на медленные потенциалы действия в пейсмекерных клетках СУ [1]. Программное обеспечение учитывает особенности периферической автономной неравномерной и асимметричной иннервации СУ и сердца, особенно в клинической интерпретации данных.
РКГ – это графическое изображение последовательного временного ряда RR-интервалов в виде отрезков прямой линии, эквивалентных по длине продолжительности пауз между сокращениями сердца. Каждый отрезок начинается на горизонтальной оси абсцисс с числом интервалов и продолжается вверх параллельно оси ординат со шкалой времени в секундах (с). В представляемой математической обработке РКГ временной (Time Domain) анализ сочетается со спектральным (Frequency- Domain) для оценки соотношения влияния на пейсмекеры СУ каждого из 3 факторов, участвующих в регуляции их активности [1-4]. Выделялись временные статистические средние значения: средний RR(NN)-интервал, среднеквадратические отклонения всех волн ВСР - SDNN, а также отдельно гуморальных, симпатических и парасимпатических волн - sl, sm, ss. Названия «l, m, s волны» определены продолжительностью периодов этих волн (long, middle, short). ARA - амплитуда дыхательной аритмии - средняя величина всех высокочастотных удлинений интервалов. В спектральном анализе применялось быстрое преобразование Фурье и спектральные окна Хамминга и Парсена. Спектральный анализ после разложения на частотные гармоники и определения спектральной мощности 3 диапазонов характеризовал соотношение трёх факторов регуляции по процентному соотношению относительно тотального спектра (100%), а также степень влияния в СУ каждого из названных факторов. Оценивались доли спектральной энергетической мощности трех диапазонов в тотальном спектре ВСР - VLF%, LF%, HF%, характеризующих степени влияний гуморально-метаболического, симпатического и парасимпатического на пейсмекерную активность в СУ. Периоды стимуляции в исходном РКГ-обследовании в покое и 4 пробах оценивались по значениям показателей: DRR - величина максимальной реакции на стимул, выраженная в процентах относительно исхода, tAB и tr – абсолютное время достижения максимальной реакции на стимул и восстановления после него до 95% величины исходного среднего интервала (в активной ортопробе - до 75%); DRR’ - величина минимального интервала при нагрузке в пробе PWC120 в секундах.
При исследовании РКГ в клинико-экспериментальном методе после исходной записи в покое (Ph) подобраны пробы со стимулирующим преимущественным воздействием на один из регулирующих факторов. манёвр Вальсальвы-Бюркера (Vm) с задержкой дыхания на глубоком вдохе в норме действует на парасимпатическую регуляцию, замедляющую и урежающую выход автоматических импульсов из Р-клеток СУ. Проба Ашнера (рА) с прессорным воздействием на глазные яблоки в наших исследованиях вызывала увеличение частоты и амплитуды гуморальных волн ВСР, что имеет физиологическое объяснение (Миронова Т.Ф., Миронов В.А., 1998). Активная ортостатическая проба (Aop) с постуральным переходом из позы лёжа в активный ортостаз действует на увеличение симпатического влияния в СУ, но не исключительно и имеет фазовые изменения. PWC, приближена к субмаксимальной нагрузке на велоэргометре или тредмиле у кардиологических пациентов, но дозируется по ЧСС120 для сравнения результатов РКГ. РКГ стационарной части в пробах сопоставлялись с РКГ в покое лежа (Ph).
При разработке каждого тематического фрагмента исследований РКГ-данные сопоставлялись со здоровым, сопоставимым контролем (47 чел.) - рисунок 1, а также с результатами стандартных референсных обследований (ЭКГ с нагрузкой, суточным мониторированием ЭКГ и АД, ЭхоКГ, КАГ перед операцией). При оценке по методике В.В. Власова диагностической ценности РКГ-симптомов дизрегуляции СУ вычисления проводились для каждого пациента.
Результаты и их обсуждение. ВСР-данные сопоставлялись с клиникой и параклиникой заболевания и с достаточной достоверностью (p<0,01-0,001) позволили определить РКГ-комплексы, характерные для ишемической патологии. При хронической ИБС перед шунтированием выделены РКГ-симптомы, которые патогенетически можно связать с хроническим нарушением перфузии тканей сердца, в том числе и узловой, из-за окклюзии венечных артерий. Дизрегуляции в СУ при ИБС любой клинической формы в РКГ-исследовании сопровождались снижением в СУ автономного симпато-парасимпатического влияния – снижение значений sm, ss, LF%, HF% и переход руководства ВСР на филогенетически низкий гуморально-метаболический уровень. Увеличивалась мощность очень низкочастотной периодики – VLF% за счёт снижения спектральных вкладов автономной – LF%, HF%, снижалась и стабилизировалась ВСР, снижалось реагирование на стимулы -DRR, увеличивались tAB, tr.
В 2003 г. найден РКГ-симптом ишемического эпизода при СтСт, что в клинике ИБС на РКГ сопровождалось выраженной стабилизацией ВСР во время пароксизмов, часто сразу после физической нагрузки. Во время ишемического эпизода RR-интервалы становятся почти одинаковыми, с разницей в пределах 3,55±1,02 миллисекунды, из-за гибернации, снижения возбудимости пейсмекерных клеток СУ в период резкого нарушения кровоснабжения в СУ вследствие возросшей окклюзии коронарных артерий. Особенно при окклюзии артерии СУ, отходящей от правой коронарной артерии [3; 4]. Вероятно, в результате активации эндотелина-1 над атеросклеротической бляшкой и увеличения окклюзии в венечном сосуде до критического 70-80% уровня, что предполагает не столь локальный характер этой ситуации. Такие эпизоды были у 95 (77,23%) пациентов с суммарной продолжительностью 2,045± 0,871 минуты (рис. 2).
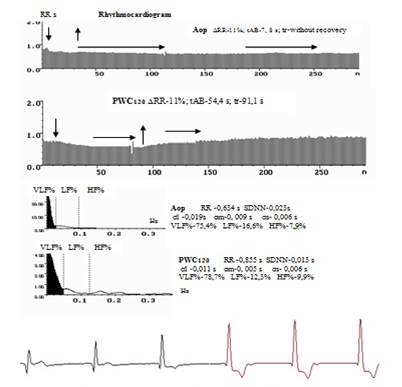
Рис. 2. Ритмокардиограммы, спектрограммы и средние значения показателей ВСР пациента со стабильной стенокардией 2 ФК в Аор и PWC. Амплитуда волн ВСР снижена. На спектрограмме патологическое соотношение влияния регулирующих факторов с преобладанием очень низкочастотной гуморально-метаболической периодики – VLF%. Горизонтальные стрелки показывают эпизоды стабилизации на РКГ, синхронные с эпизодами ишемии. На ЭКГ им соответствует депрессия ST
В 44 (35,77%) случаях стабилизация совпадала с депрессией ST. С 2003 г. в кардиологической практике используется этот РКГ-симптом. При вариабельном пороге ишемии в стационарной части РКГ всех проб появляются участки стабилизации ВСР при СтСт 2 и 3 ФК. При СтСт 4 ФК у пациентов с АКН, то есть при стабилизации и отсутствии реагирования на любые стимулы в пробах, такие ишемические эпизоды трудно различить из-за общей стабилизации ВСР при существующей недостаточной чувствительности экранов компьютерных мониторов.
При мониторной РКГ-записи во время операции оказалось, что каждому этапу соответствуют определённые изменения ВСР [4-7; 9; 11; 12]. При премедикации, к примеру, за 30 минут до начала операции в ответ на введение диазепама, атропина, промедола значительно и достоверно снизились статистические временные ВСР-показатели симпатической и парасимпатической регуляции-σm, σs. Амплитуда гуморальных колебаний тоже снизилась, без достоверности (табл. 1).
Таблица 1
ВСР-показатели до (n-123) и после (n-123) премедикации при шунтировании
|
ВСР показатели (M ± s) в сек. (с) и % |
RR с среднее з значение всехRR |
SDNN с среднеква- дратичная девиация всех волн |
σl, с среднеква- дратичное отклонение гуморальн. волн |
σm, с среднеква- дратичное отклонение симпатическ. волн |
σs, s среднекв. откл-е парасим- патич. волн |
VLF% спектра- льная доля гу-моральн. волн |
LF% спектр. доля симпа-тическ. волн |
HF% спектр. доля парасим- патич. волн |
|
HRV –in-dices before CABGS |
0,984± 0,144 |
0,024± 0,009 |
0,018± 0,008 |
0,011±0,005 |
0,011± 0,008 |
56,39± 14,9 |
17,84± 10,83 |
25,76± 12,53 |
|
HRV –in- dices after pre-medication |
0,522± 0,031 |
0,011± 0,002 |
0,002± 0,001 |
0,001± 0,0012 |
0,002± 0,001 |
68,8± 8,42 |
15,23± 6,11 |
15,7± 4,78 |
|
Z* p |
34,7 p<0,0001 |
6,5 p<0,01 |
1,45 p>0,05 |
4,01 p<0,05 |
12,8 p<0,001 |
7,892 p<0,01 |
2,1 p<0,05 |
6,89 p<0,01 |
*Здесь использован критерий Z для непараметрических выборок большого объёма (разница достоверна при z>1,9).
За счёт снижения m- и s-колебаний уменьшился общий показатель всех волн ВСР (SDNN= 0,024±0,009 с до премедикации vs 0,011±0,002 c после неё (p<0,01)). При этом гуморально-метаболические флуктуации, по-видимому, участились, и в результате гуморальная доля воздействия на пейсмекеры возросла с высокой достоверностью (p<0,01). После премедикации ВСР волны исчезли, РКГ стабилизировалась. Изменения ВСР данных начинались с премедикации и продолжались до конца операции, а также в раннем периоде после неё (рис. 3).
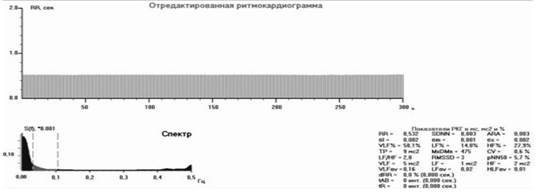
Рис. 3. Ритмокардиограмма и спектрограмма после премедикации и интубационного наркоза. На фоне тахикардии выраженная стабилизация ВСР. Волновая структура представлена очень низкочастотной гуморально-метаболической периодикой VLF. На спектрограмме её спектральная площадь выделена чёрным цветом - 58,1%.
Симпатические и парасимпатические волны в низко- и высокочастотном спектрах ниже нормы - 14% и 27,9%
Канюляция полых вен и аорты и инсталляция зажимов выполнялись для перевода кровообращения на аппарат искусственного кровообращения (АИК). В вену вводился кардиоплегический раствор с высокой концентрацией калия для остановки сердца. Установка канюль и зажимов сопровождалась манипуляциями хирурга, чему на РКГ соответствовали аритмические эпизоды желудочковой тахикардии (VT), экстрасистолии (VE) и асистолии (AS) (рис. 4).
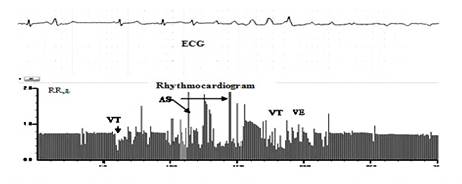
Рис. 4. Ритмокардиограмма и ЭКГ при установке зажимов в аорте и введении кардиоплегического раствора. Манипуляции хирурга вызвали нарушения ритма в виде желудочковой тахикардии (VT), полифокусной экстрасистолии и асистолии. Судя по ЭКГ, началась последовательная постепенная остановка сердца, после чего кровообращение переходит на аппаратное кровоснабжение, на АИК
После остановки сердечных сокращений и перевода кровообращения на АИК РКГ-запись приостанавливалась, хирургами выполнялось шунтирование, снимались зажимы, отключался АИК и сердечные сокращения запускались вновь. Запуск систол сопровождался манипуляциями хирургов, прямым массажем сердца, электрической дефибрилляцией. Процедура восстановления самостоятельной работы сердца во время хирургических манипуляций и дефибрилляции также сопровождалась жизнеопасными нарушениями ритма вплоть до асистолии (рис. 5).

Рис. 5. РКГ и ЭКГ пациента после отключения АИК при запуске самостоятельных сокращений сердца. На фоне тахикардии в начале записи РКГ выраженные аритмии, асистолия (As), дефибрилляция (ED), множественные полифокусные желудочковые экстрасистолы (VE) во время прямого массажа сердца.
На ЭКГ медленное восстановление кардиокомплексов
При этом нарушения по РКГ-представленности совпадали с локализацией манипуляций хирургов, что предполагает связь нарушений с работой хирургов руками – наджелудочковые нарушения и трепетание предсердий возникали при работе с предсердиями, желудочковые зарегистрированы при прямом массаже желудочков сердца (рис. 4, 5). РКГ-данные предполагают, что жизнеопасные нарушения ритма сердца при интервенционной реваскуляризации миокарда связаны с манипуляциями хирургов при проведении операции.
В таблице 2 приводятся РКГ-показатели по этапам шунтирования.
Таблица 2
Показатели РКГ-исследования по этапам хирургической реваскуляризации миокарда (n-123)
|
ВСР-показатели (M±õ) в секундах (с) и % |
RR с средний RR-интервал |
SDNN с стандарт-ная дисперсия всех волн |
σl, с среднеква-дратичная дисперсия гумораль-ных волн |
σm,с среднеква-дратичная дисперсия симпатии-ческих волн |
σs, с среднеква-дратичная дисперсия парасим-патических волн |
VLF% спектра- льная доля гуморальных волн ВСР |
LF% спектра- льная доля сим патическ. волн ВСР |
HF% спектра- льная доля пара симпатич. волн ВСР |
|
Премедикация и интубац. наркоз |
0,783± 0,030 |
0,003± 0,001 |
0,003± 0,001 |
0,001± 0,001 |
0,001± 0,001 |
72,2± 18,4% |
12,8± 4,23% |
15,0± 3,5% |
|
Каннюляция вен и аорты |
0,653± 0,024 |
0,003± 0,001 |
0,003± 0,001 |
0,001± 0,001 |
0,001± 0,001 |
84,2± 11,2% |
7,4± 3,4% |
8,4± 2,82% |
|
Введение кардиоплегической смеси |
0,610± 0,033 |
0,004± 0,001 |
0,002± 0,002 |
0,004± 0,001 |
0,001± 0,001 |
91,2± 7,2% |
6,4± 2,33% |
2,4± 1,87% |
|
Подключение к АИК |
0,580± 0,087 |
0,002± 0,001 |
0,002± 0,002 |
0,002± 0,001 |
0,001± 0,001 |
90,2± 10,8% |
6,8± 3,2% |
3,0± 1,9% |
|
Удаление зажимов |
0,564± 0,034 |
0,003± 0,001 |
0,003± 0,001 |
0,002± 0,001 |
0,001± 0,001 |
88,6± 12,4% |
5,4± 1,9% |
5,0± 2,1% |
|
Восстановление работы сердца |
0,680± 0,110 |
0,006± 0,002 |
0,006± 0,002 |
0,002± 0,001 |
0,002± 0,001 |
87,2± 7,12% |
5,0± 2,1% |
7,8± 3,4% |
В таблице 2 представлены данные временного статистического и спектрального анализа ВСР при различных этапах выполнения аорто- и маммарокоронарного шунтирования. После премедикации и интубационного наркоза значения ВСР-показателей существенно снизились. Исходно низкие до операции ВСР-показатели стали ещё ниже после наркоза и выражались единицами миллисекунд. В последовательности этапов заметно, что амплитуда всех флуктуаций становилась всё ниже и ниже. Изменилось соотношение влияния регулирующих факторов в сторону значительного увеличения воздействия в СУ гуморально-метаболического, филогенетически неэффективного, за счёт снижения влияния автономной регуляции. Это видно по предельному увеличению доли VLF% и столь же низким значениям симпатического и парасимпатического влияний - HF%, LF%. И лишь в периоде восстановления работы сердца началось небольшое изменение спектрального соотношения факторов регуляции в направлении увеличения автономных показателей.
Среди пациентов, перенёсших операцию, был случай с летальным исходом на 4-й день после операции. Исходно у этого больного были наиболее неблагоприятные ВСР-показатели, соответствующие автономной кардионейропатии: предельно выраженная стабилизация ВСР, полное отсутствие реакций на допустимые стимулирующие пробы. На этом фоне периодически возникали заместительные ритмы. При жизни у больного до шунтирования была АКН. РКГ пациента представлена на рис. 6.
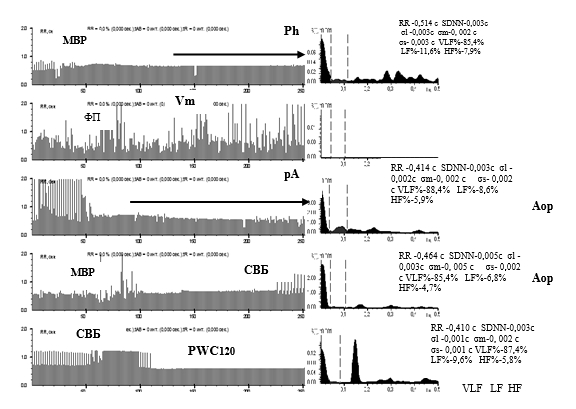
Рис. 6. Исходные ритмокардиограммы, спектрограммы и средние значения ВСР-показателей больного Д. до проведения коронарного шунтирования. В Ph (РКГ 1) и PWC120 (РКГ 4) значительно сниженная ВСР во время продолжительных эпизодов стенокардии. Между 1 и 40 интервалами - миграция водителя ритма (МВР). На фоне АКН между 130 и 240 интервалами длительный эпизод ишемии (указан горизонтальной стрелкой) с типичными клиническими проявлениями стенокардии. В Vm - фибрилляция предсердий. Среднеквадратичные отклонения амплитуды волн ВСР-SDNN, σl, σm, σs исчисляются единицами миллисекунд. В спектральном соотношении регулирующих факторов в СУ значительное преобладание гуморально-метаболического влияния (VLF%) над автономным симпато-парасимпатическим (LF%, HF%). В рА в начале записи между 1 и 43 интервалами синоатриальная блокада 2-3 степени на фоне АКН и МВР. В Аор между 60 и 100 интервалами фибрилляция предсердий (ФП), затем ишемический эпизод со стабилизацией ВСР (разница между соседними RR-интервалами в пределах 3.55±1.02 миллисекунды) и в конце ортостаза суправентрикулярная бигеминия - СВБ (относительно одинаковые преэктопические интервалы), которая продолжилась во время ходьбы на тредмиле в PWC120, после чего вновь эпизод ишемии на фоне значительно сниженной ВСР, соответствующей АКН. Все аритмии возникали на фоне выраженного угнетения автономного влияния в СУ, что свидетельствует о протектирующем значении симпато-парасимпатической регуляции в СУ и повышении риска смерти при её отсутствии. Больной умер на 4-й день после операции, что подтверждает значение АКН для прогноза летального исхода [8]
Наиболее клинически тяжёлые пациенты имели стабилизированную или значительно сниженную ВСР (рис. 5), а также отсутствие реакций на стимулы в пробах ещё до операции при отборе больных на хирургическую реваскуляризацию миокарда. У всех 67 таких пациентов до операции и во время манипуляций хирургов возникали аритмические осложнения, в том числе трепетание предсердий при манипуляциях на предсердиях. Поэтому были основания предполагать, что АКН, то есть отсутствие автономного контроля, является предиктором аритмических осложнений во время операции и тяжести состояния до и после шунтирования. То есть утрата протективного вегетативного контроля в СУ является маркёром и предвестником осложнений и повышением риска летального исхода. Представлены результаты ВСР-исследования наиболее клинически тяжёлых больных с АКН до операции. Вегетативная регуляция СУ у них отличается с высокой достоверностью от показателей ВСР с более сохранной вариабельностью ритма (таблица 3).
Таблица 3
Результаты сравнения ВСР-показателей у больных с автономной кардионейропатией (АКН) n-56, верхняя строка) и у больных без АКН (n-67, вторая строка) до шунтирования
|
HRVпоказатели (M ±s) в сек. (с) и % |
Ph, Исходная поза лёжа |
Vm, Проба Вальсальвы-Бюркера |
рА, Проба Ашнера |
Aор, Активная ортостатическая проба |
PWC120 Проба с физической нагрузкой |
|
RR с, Средний интервал |
0,522±0,081 0,768±0,114 t= 14.05 *** |
0, 542±0,072 0,770±0, 102 T= 14.61*** |
0,546±0,082 0,777±0,107 t=13.83** |
0,698±0,095 0,810±0, 087 t= 7.25** |
0,783±0,124 0, 730±0,074 t=2.83* |
|
SDNN с, стандартная девиация всех волн |
0,011±0,002 0,017±0,006 t=2.0* |
0,011±0,005 0,016±0,005 t= 5.98** |
0,011±0,006 0,017±0,004 t= 7.79** |
0,009±0,004 0,017±0,006 t=8.88*** |
0,010±0,005 0,018±0,004 t= 10.3*** |
|
σl, с среднеква-дратичная деви -ация гумораль -ных волн ВСР |
0,002±0,001 0,008±0,004 t= 10,0*** |
0,008±0,004 0,011±0,005 t= 4.28* |
0,008±0,004 0,012±0,005 t= 5.19** |
0,007±0,003 0,012±0,004 t= 8.33*** |
0,008±0,003 0,015±0,004 t= 11.6*** |
|
σm, с среднеквадратичная девиация симпатич.волн ВСР |
0,001±0,001 0,006±0,002 t= 6.02** |
0,004±0,002 0,008±0,002 t=4.0** |
0,004±0,002 0,009±0,003 t= 3.57* |
0,003±0,002 0,009±0,002 t= 5.45** |
0,005±0,003 0,012±0,002 t= 8.49*** |
|
σs, среднеквадратичная дисперсия пара симпатич.волн ВСР |
0,002±0,001 0,007±0,004 t= 7.93** |
0,006±0,003 0,011±0,003 t= 4.54** |
0,006±0,004 0,010±0,001 t= 6.34** |
0,004±0,003 0,012±0,001 t= 16.0*** |
0,007±0,005 0,014±0,003 t= 5.38** |
|
VLF% спектра- льная доля гуморальных волн ВСР |
78,8±8,42 56,39±14,89 T= 10.47*** |
74,64±8,34 60,26±16,30 t=6.3** |
76,19±9,98 55,31±16,42 t=8.66*** |
77,20±19,64 59,36±16,23 t=5.42** |
78,46±24,39 57,87±19,35 t= 5.11* |
|
LF% спектра- льная доля симпатических волн ВСР |
12,33±7,03 17,84±10,83 t=3.39* |
13,77±8,99 16,60±5,82 t=2.02* |
13,98±8,88 17,75± 10,0 t=2.21* |
12,89±7,32 18,91±14,22 t= 3.02* |
14,87±6,98 16,64±7,79 t=1.33 |
|
HF% спектра- льная доля парасимпатических волн ВСР |
15,7±4,78 25,76±12,53 t=6.03** |
16,58±7,84 21,12±16,18 t=2.028* |
16,88±7,61 20,93±12,7 t=2.19* |
17,9±6,31 22,72±11,24 t=2.88* |
22,66±7,11 37,48±19,12 t= 5.87** |
|
Δ RR % максимальн. реакции в пробах |
6,48±6,13 11,59± 9,96 t= 3.48* |
4,12±3,60 7,95± 6,87 t= 3.95* |
12,31±6,78 21,69±8,07 t = 6.91** |
9,62±7,21 19,23±11,26 t = 5.72** |
|
|
tAB, с время макс. реакций в пробах |
9,92 ± 2,56 7,78±2,58 t =4.6** |
9,38±2,47 5, 55±2,38 t = 8.71*** |
18,61± 6,39 11,99±3,82 t =6.8** |
43,85 ±12,96 20,0±12,16 t =10.45*** |
|
|
tr, время восстановления после проб |
12,73± 8,61 7,48±4,71 t =4.07* |
24,61±7,85 14,47±4,98 t = 8.36*** |
20,03±6,26 15,05±5,74 t = 4.56** |
102,06±32,21 75,06±27,71 t = 4.92** |
- *p<0,05; ** p<0,01; ***p<0,001.
В таблице 3 представлены в сравнении ВСР-данные до шунтирования у пациентов с АКН (верхняя строка) и без АКН (нижняя строка). По всем показателям различия между группами достоверны. Показано, что у пациентов с АКН ниже показатели ВСР, ниже реакции на стимулы в пробах, медленнее их достижение и восстановление после действия стимулов. Спектральное соотношение регулирующих факторов в СУ при АКН неблагоприятное и показывает ведущую роль в пейсмекерной функции СУ гуморально-метаболического воздействия за счёт угнетения протективного автономного симпато-парасимпатического руководства ритмом. Частота кардиоаритмий у больных с АКН средне значимо отрицательно коррелировала с выраженностью ВСР-показателей (=0,584-0,638).
Нам удалось получить контрольный аутопсийный материал синоатриального узла мужчины, погибшего от несердечной причины, а также материал умершего больного с АКН при жизни [10]. Результаты электронной микроскопии показаны для сравнения (рис. 7 и 8).

Рис. 7. Электронная микроскопия нормального состояния пейсмекерных клеток синоатриального узла сердца. Гистологический препарат клеток переходного типа проводящей системы сердца в области синусового узла погибшего от внесердечной причины мужчины из группы контроля. Ультратонкий срез, контрастированный уранилацетатом свинца и цитратом свинца (увеличение в 1260 и 1984 раза). Видны митохондрии с сохранными кристами внутри митохондрий пейсмекерной клетки [10]
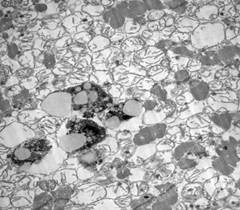
Рис. 8. Гистологический препарат клетки переходного типа проводящей системы сердца в области синусового узла у погибшего больного ИБС и с автономной кардионейропатией. Ультратонкий срез, контрастированный уранилацетатом свинца и цитратом свинца (увеличение в 1984 раза). Набухание множественных митохондрий и разрушение митохондриальных крист, кальцинаты в митохондриях, внутриклеточные включения липидных капель и липофусцина, что соответствует дистрофии пейсмекерных клеток синоатриального узла сердца
Таким образом, РКГ является информативным методом интранозологической диагностики дизрегуляторных нарушений кардиоваскулярной системы в главном пейсмекере – синоатриальном узле. Высокое разрешение специализированного аппаратно-программного комплекса при измерении и анализе волновой структуры межсистолических временных интервалов, разработка временного и спектрального математического компьютерного анализа ВСР могут оцениваться клинически адекватными из-за достоверного соответствия, воспроизводимости и сопоставимости результатов с данными других исследований и клиникой заболеваний. Метод РКГ предоставляет возможность анализа многовариантных периферических вегетативных дизрегуляторных нарушений пейсмекерной активности СУ сердца, являющихся облигатным, патогенетически обусловленным и ранним проявлением, а в последующем и фоном, сердечно-сосудистой патологии при многих заболеваниях. Исследование РКГ может быть полезным для создания системы анестезиологического ведения оперативных вмешательств. РКГ является также адекватным методом неспецифической диагностики болезней на основе выявления дизрегуляций вариабельности сердечного ритма, поскольку с нарушений регуляций начинаются многие заболевания и на фоне дизрегуляций формируются в дальнейшем. В этом отношении альтернативы у этого метода пока нет.
Библиографическая ссылка
Миронова Т.Ф., Миронов В.А., Куватова Е.В., Куватов В.А. ВЫСОКОРАЗРЕШАЮЩИЙ АНАЛИЗ ВАРИАБЕЛЬНОСТИ СЕРДЕЧНОГО РИТМА У БОЛЬНЫХ СТЕНОКАРДИЕЙ НАПРЯЖЕНИЯ ВО ВРЕМЯ КОРОНАРНОГО ШУНТИРОВАНИЯ // Современные проблемы науки и образования. – 2017. – № 6. ;URL: https://science-education.ru/ru/article/view?id=27059 (дата обращения: 19.04.2024).



