Возможность осуществления функции кровообращения кооперацией деятельности двух органов – сердца и сосудов – объясняет объединение их с незапамятных времен в единую сердечно-сосудистую систему. Интегральная характеристика степени участия сердечного и сосудистого компонентов в величине артериального давления (АД) крови и типов гемодинамики [1], предложенная в 1974 г., таковой и осталась, несмотря на уже многолетние определения функциональных и морфологических параметров гемодинамики ультразвуковым исследованием (УЗИ). Была предложена лишь стандартизация минутного объёма крови [2], а составляющие сосудистого компонента были дополнены феноменом амплификации пульсовой волны [3], связанным с морфологической гетерогенностью сосудистых бассейнов, модифицирующейся, естественно, в условиях патологии. При гипертонической болезни (ГБ) этот феномен негативно сказывается на показателях центральной гемодинамики, а природа его возникновения не позволяет считать ремоделирование сосудистой стенки при ГБ прерогативной какой-то одной сосудистой зоны [4; 5].
В то же время клиническая литература наводнена публикациями об ассоциациях показателей центральной гемодинамики с фрагментарными морфологическими или функциональными показателями периферической гемодинамики того или иного бассейна, в которых отсутствует аргументация выбора исследуемого бассейна, не объяснятся, чем была определена односторонность или двусторонность исследования его сосудов, почему при одностороннем исследовании авторы отдали преимущество одной из сторон. К примеру, изучая ремоделирование артерий разных бассейнов при ГБ – общей сонной артерии (ОСА) [6; 7]; ОСА, плечевой артерии (ПА) и лучевой артерии (ЛА) [8]; ОСА, общей бедренной артерии (ОБА) и поверхностной бедренной (ПБА) [9]; ОСА, ОБА, ПА и ЛА [10]; ОСА, ОБА и подколенной артерии (ПКА) [11], исследователи использовали различные показатели без обоснования выбора изучаемого бассейна, односторонности исследования, не всегда указывая даже выбранную сторону тела.
Проведя двухстороннее исследование одноименных сосудов и обнаружив морфологические и функциональные различия в разных сосудистых бассейнах [12], предложили использовать васкулярный индекс CARFEM, определяемый как среднеарифметическое значение суммы четырех величин – толщины интимы-медиа (ТИМ) ОСА и толщины стенки (ТС) ПБА с обеих сторон или двух – для правой и левой стороны соответственно. Кроме того, существует разночтение понятий эластических и мышечных сосудов, сосудов крупного, среднего и мелкого калибров [11; 13-16].
Приведенные публикации, указывая на многоуровневое и неоднородное поражение сосудов при ГБ, свидетельствуют об отсутствии единого подхода к выбору сосудистого бассейна и показателей оценки его состояния для изучения закономерностей сердечно-сосудистой кооперации как в норме, так и в патологии.
Цель исследования: обосновать выбор приоритетных сосудистых бассейнов, а также ультразвуковых показателей, отражающих морфологическое и функциональное состояние их сосудов, при обследовании пациентов с гипертонической болезнью.
Материал и методы. Проведено дуплексное сканирование (ДС) периферических артерий разного калибра и разной локализации с обеих сторон у 154 человек в возрасте от 21 до 75 лет (в среднем 51,82±10,01): 23 – контрольная группа (КГ), представленная практически здоровыми лицами в возрасте 34-70 лет (в среднем 47±8,41), и 131 – лица с гипертонической болезнью (ГБ) I-III стадий в возрасте 21-75 лет (в среднем 52,65±10,07) на УЗ-сканере «Medison 8000». Исследованы артерии крупного (ОСА – все лица КГ и пациенты с ГБ; ОБА – 21 лицо КГ и 110 пациентов с ГБ); малого (задняя большеберцовая артерия (ЗББА) – 21 и 105; передняя большеберцовая (ПББА) – 7 и 51 соответственно), а также среднего калибра (правой ПА – 21 лицо КГ и 110 пациентов с АГ).
Из структурных показателей состояния артерий определяли толщину стенки (ТС) артерии, в том числе и относительную, ТИМ, диаметры артерий, массу артериальной стенки (АМ) рассчитывали по формуле АМ=ρ×L×(π×Re2- π×Ri2), где ρ – плотность артериальной стенки, L – референтная длина артериального сегмента, равная 1 см, Re – наружный радиус сосуда, Ri – внутренний радиус сосуда. Кроме того, были рассчитаны параметры, характеризующие функциональные свойства артериальной стенки: коэффициент диаметрального расширения (DC=((2×(Ds-Dd)/Dd)×103)/(ПАД/5,5187)), индекс жесткости (β=In (САД/ДАД)×Dd/(Ds-Dd)), циркумферентное напряжение (ЦН=АДср/(ТС/Dпр), мм рт.ст.), эластический модуль Петерсона (Ep=ПАД×(Dd/(Ds-Dd)) мм рт.ст. на единицу относительной деформации), статический эластический модуль Юнга (Es=Ep×Dd/(2×ТС), мм рт. ст. на единицу относительной деформации), скорость распространения пульсовой волны (PWV=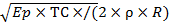 , где R – радиус сосуда) [12; 13].
, где R – радиус сосуда) [12; 13].
Статистический анализ. Нормальность распределения изучаемых показателей оценивали по критерию Колмогорова-Смирнова. Большая часть параметров не имела нормального распределения, и достоверность их различий между лицами КГ и пациентами с ГБ определяли непараметрическим критерием U Манна-Уитни. Корреляционный анализ использовали для оценки симметричности строения одноименных сосудов. Дискриминантным анализом определялась предикторность структурных и функциональных сосудистых параметров у лиц с ГБ. За достоверное значение коэффициента результативности (КФР) принимали значение, превышающее 75%, при р<0,05. Данные представлены в виде M±SD, где SD – среднеквадратичное отклонение. Статистическая обработка результатов проводилась программой SPSS, Versia 19 (лицензия № 20101223-1).
Результаты и обсуждение. Дискриминантным анализом было исключено (КФР=71%) влияние конституциональных факторов, таких как рост, вес, пол, ИМТ и возраст на сосудистые параметры.
Непараметрический анализ выявил значимые различия как по структурным, так и по функциональным признакам между группой контроля и лицами ГБ в каждом изучаемом бассейне с обеих сторон (p<0,05). В большей степени эти различия были выражены при сравнении крупных периферических сосудов, ЗББА и ПА, в меньшей – по ПББА.
Корреляционным анализом оценена симметричность строения одноименных сосудов (справа и слева) у лиц КГ и ГБ. В группе контроля обнаружена высокая корреляция между диаметрами на всех уровнях, а также ТИМ в ОСА и ПББА. У пациентов с ГБ корреляционные связи между этими показателями справа и слева указывают на склонность к асимметрии ремоделирования (табл. 1).
Таблица 1
Значения коэффициента корреляции (r) между правыми и левыми одноименными артериями по ТИМ, диаметрами сосудов в систолу, диастолу и диаметрами просвета
|
Показатель |
ОСА |
ОБА |
ЗББА |
ПББА |
||||
|
r |
p |
r |
p |
r |
p |
r |
p |
|
|
Контрольная группа |
||||||||
|
ТИМ |
0,797 |
0,0001 |
0,642 |
0,0001 |
0,393 |
0,078 |
0,778 |
0,039 |
|
Ds |
0,844 |
0,0001 |
0,891 |
0,0001 |
0,95 |
0,0001 |
0,903 |
0,005 |
|
Dd |
0,829 |
0,0001 |
0,812 |
0,0001 |
0,906 |
0,0001 |
0,923 |
0,002 |
|
Dпр |
0,84 |
0,0001 |
0,79 |
0,0001 |
0,824 |
0,0001 |
0,956 |
0,001 |
|
Группа лиц с гипертонической болезнью |
||||||||
|
ТИМ |
0,783 |
0,0001 |
0,72 |
0,0001 |
0,515 |
0,0001 |
0,556 |
0,0001 |
|
Ds |
0,84 |
0,0001 |
0,594 |
0,0001 |
0,827 |
0,0001 |
0,411 |
0,003 |
|
Dd |
0,818 |
0,0001 |
0,778 |
0,0001 |
0,794 |
0,0001 |
0,45 |
0,001 |
|
Dпр |
0,728 |
0,0001 |
0,772 |
0,0001 |
0,653 |
0,0001 |
0,365 |
0,008 |
Примечание: ОСА – общие сонные артерии, ОБА – общие бедренные артерии, ЗББА - задние большеберцовые артерии, ПББА – передние большеберцовые артерии, ТИМ - толщина интимы-медиа, Ds – диаметр в систолу, Dd – диаметр в диастолу, Dпр – диаметр просвета, r – коэффициент корреляции, p – уровень значимости.
Поиск наиболее адекватных показателей, характеризующих поражение сосудов как единого «органа-мишени» при ГБ, предикторности структурных и функциональных параметров по каждому изучаемому сосудистому бассейну раздельно справа и слева, а также при их сочетании с обеих сторон одного бассейна и разных бассейнов, осуществлен дискриминантным анализом. Полученные значения КФР представлены в таблице 2.
Таблица 2
Значения КФР (%) предикторности функциональных характеристик и структурных параметров между лицами КГ и пациентами с ГБ (p=0,0001)
|
Сосуд |
Функциональные характеристики |
Структурные показатели |
||||
|
D |
S |
D+S |
D |
S |
D+S |
|
|
ОСА |
87,0 |
90,3 |
87,0 |
82,5 |
76,6 |
81,2 |
|
ОБА |
84,0 |
89,3 |
92,4 |
81,7 |
87,0 |
84,0 |
|
ЗББА |
81,0 |
74,6 |
80,2 |
81,7 |
79,4 |
86,5 |
|
ПББА |
87,9 |
84,5 |
93,1 |
– |
– |
– |
|
ПА |
84,7 |
– |
||||
|
ОСА+ОБА |
89,3 |
90,1 |
90,8 |
82,4 |
84,7 |
87,0 |
|
ЗББА+ПББА |
72,2 |
89,7 |
91,8 |
75,4 |
91,4 |
91,4 |
|
Все сосуды |
94,8 |
90,8 |
100,0 |
81,0 |
100,0 |
100,0 |
Примечание: D – справа, S – слева, D+S – с обеих сторон, ОСА – общие сонные артерии, ОБА – общие бедренные артерии, ЗББА - задние большеберцовые артерии, ПББА – передние большеберцовые артерии, ПА – плечевая артерия справа, ОСА+ОБА – общая сонная и общая бедренная артерии; ЗББА+ПББА – задняя и передняя большеберцовые артерии.
Преобладание функциональных расстройств сосудистой стенки над их структурной перестройкой доказано большей выраженностью изменений функциональных характеристик между сравниваемыми группами, в том числе и в сосудах с отсутствием структурной перестройки (ПББА и правая ПА). Время же возникновения ремоделирования сосудов у пациентов ГБ требует дальнейшего его изучения по стадиям ГБ. Объединение изучаемых функциональных показателей с двух сторон одного бассейна повысило предикторность со стороны ОБА и берцовых артерий, а разных бассейнов – и для крупных, и для мелких артерий.
Выявленные нами в ходе анализа различия структурных показателей согласуются с данными [9; 11], которые касаются обнаруженных изменений крупных артерий и ЗББА при отсутствии таковых в ПА и ПББА. Boutouyrie P., Benetos A. et al. [10] получили большую жесткость сонных артерий, чем бедренных или лучевых, у пожилых людей с АГ или сахарным диабетом. Возможно, полученные результаты обусловлены более сильным механическим воздействием пульсовой волны на стенки ОСА из-за близости к аорте, большим объемом зоны кровоснабжения ОБА и ЗББА в сравнении с ПА и ПББА.
Отсутствие публикаций с одномоментным изучением показателей разных сосудистых бассейнов как предикторов ГБ, полученные некоторыми авторами доказательства асимметрии структурных характеристик одного бассейна [8], а тем более разных бассейнов [12], и использование среднеарифметических величин некоторых показателей побудило нас провести дискриминантный анализ при объединении структурных характеристик сосудов одного бассейна с двух сторон, что дало прирост КФР по ЗББА и усреднило его по крупным артериям.
Объединение же структурных параметров сосудов крупного или мелкого калибра усилило различия между сравниваемыми группами как при одностороннем, так и при двустороннем объединении для крупных артерий. Для берцовых же артерий аналогичный анализ показал прирост КФР слева и с двух сторон. Объединение параметров сосудов всех изучаемых калибров с обеих сторон повысило КФР до 100% как по структурным, так и по функциональным характеристикам.
Изучение среднеарифметических значений между правой и левой сторонами одного бассейна показало больший КФР только по функциональным характеристикам сосудистой стенки ЗББА (при включении в независимые переменные одномоментно показателей справа и слева получено значение КФР=80,2%, а по среднеарифметическим значениям этих же параметров КФР=83,3%) и объединения крупных артерий (84% и 89,3% соответственно), не имея преимуществ по структурным параметрам ни в одном из изучаемых сосудов.
Выявлены различия параметров сосудов не только разной локализации, но и разных сторон между контролем и больными, что делает обоснованным проведение как двустороннего, так и разноуровневого ДС периферических сосудов, хотя бы при научных исследованиях.
Параллельно дискриминантный анализ позволил выявить и сосудистые маркеры ГБ (табл. 3).
Таблица 3
Значения функциональных и структурных параметров периферических сосудов в контрольной группе и у больных ГБ (значимо отличающиеся)
|
Показатель |
КГ (M±SD) |
ГБ (M±SD) |
|
Функциональные показатели |
||
|
DCоса справа |
26,52±9,84 |
16,84±8,42 |
|
ЦНоса справа |
466,99±108,42 |
484,8±111,03 |
|
Ep оса слева |
681,07±276,05 |
1193,86±729,03 |
|
Es оса слева |
1937,34+921,8 |
3199,54±2125,03 |
|
ЦНоса слева |
439,45±91,55 |
464,64+105,03 |
|
PWVоса слева, см/сек |
9,36±1,92 |
13,03±3,7 |
|
ЦНоба справа |
542,45±95,14 |
546,45±124,08 |
|
PWVоба справа |
8,13±1,6 |
12,84±4,06 |
|
β оба справа, мм рт. ст. |
6,31±3,21 |
10,77±6,61 |
|
Ep оба справа |
1067±250,01 |
1318,63±826,63 |
|
Es оба справа |
2249,49±968,05 |
3980,5±2599,8 |
|
DCоба слева |
25,45±10,61 |
15,35±7,77 |
|
β збба справа, мм рт. ст. |
4,54±2,18 |
8,53±5,3 |
|
PWVзбба справа, см/сек |
9,13±1,49 |
14,79±4,34 |
|
PWVзбба слева, см/сек |
9,51±1,49 |
14,4±4,01 |
|
PWVпа, см/сек |
10,69±2,24 |
13,95±4,23 |
|
ЦНпа |
373,22±70,9 |
513,66±136,56 |
|
DCпбба справа |
43,48±42,83 |
15,47±10,24 |
|
DCпбба слева |
30,46±20,57 |
18,84±13,27 |
|
ЦНпбба слева |
246,36±35,16 |
233,16±73,21 |
|
Структурные показатели |
||
|
ТИМоса справа, см |
0,61±0,2 |
0,86±0,17 |
|
RWTоса справа |
0,4±0,08 |
0,49±0,09 |
|
Dd оса справа, см |
6,67±0,83 |
7,2±1,04 |
|
ТИМоса слева, см |
0,62±0,12 |
0,86±0,17 |
|
ТСоса слева, см |
1,05±0,17 |
1,35±0,21 |
|
ТИМоба справа, см |
0,67±0,07 |
0,91±0,16 |
|
RWTоба справа |
0,33±0,05 |
0,43±0,09 |
|
ТИМоба слева, см |
0,62±0,06 |
0,93±0,19 |
|
Ds оба справа, см |
9,02±1,18 |
9,16±1,27 |
|
ТСоба слева, см |
1,11±0,08 |
1,48±0,23 |
|
ТИМзбба справа, см |
0,25±0,05 |
0,44±0,12 |
|
АМзбба справа, гр |
0,04±0,02 |
0,06±0,03 |
|
ТИМзбба слева, см |
0,29±0,05 |
0,45±0,1 |
Примечание: p<0,0001; ТИМоса, ТИМоба, ТИМзбба – толщина интимы-медиа общей сонной, общей бедренной, задней большеберцовой артерий соответственно; ТСоса, ТСоба – толщина стенки ОСА и ОБА; Dd – диаметр в диастолу; Ds – диаметр в систолу; RWTоса, оба – относительная толщина стенки ОСА и ОБА; АМ – масса артериальной стенки; DCоса, оба, пбба – коэффициент диаметрального расширения ОСА, ОБА и ПББА соответственно; ЦНоса, оба, па, пбба – циркумферентное напряжение ОСА, ОБА, ПА и ПББА соответственно; Ep оса, оба – эластический модуль Петерсона ОСА и ОБА соответственно; Es оса, оба – статический эластический модуль Юнга ОСА и ОБА; PWVоса, оба, збба – скорость распространения пульсовой волны ОСА, ОБА и ЗББА; β оба, збба – индекс жесткости ОБА и ЗББА.
Более выраженные изменения при ГБ выявлены в артериях крупного калибра в виде двухстороннего утолщения сосудистой стенки и её компонентов при одностороннем увеличении диаметров. В мелких артериях ремоделирование имеет несколько иной характер: в ЗББА только двустороннее увеличение толщины стенки без дилатации просвета; в ПА и ПББА определены лишь функциональные изменения. ГБ ассоциирована с повышением жесткости сосудистой стенки артерий ног (ОБА и ЗББА), PWV во всех исследуемых бассейнах (кроме ПББА) при закономерном снижении диаметрального расширения и возросшем напряжении на стенку всех сосудистых бассейнов (даже ПББА).
Таким образом, ремоделирование артерий разного калибра при ГБ имеет некоторые особенности: утолщение стенки на разных уровнях, одностороннее увеличение диаметра крупных артерий, что может быть объяснено исходными морфометрическими и гистологическими отличиями в виде большей представленности в более мелких периферических артериях гладкомышечных клеток.
Выводы
1. Причина асимметричности ремоделирования сосудов при ГБ изначально заложена в асимметричности их морфологического строения у лиц контрольной группы.
2. Выраженность функциональных изменений у лиц ГБ бóльшая, чем структурных, причем в ПББА и ПА первые из них развивались изолированно.
3. Объединение параметров, либо структурных, либо функциональных одноименных сосудов одного бассейна, а также у сосудов разных бассейнов чаще повышает КФР вплоть до 100% при суммации параметров сосудов всех изучаемых бассейнов с обеих сторон. Объединение для анализа всех структурных и функциональных параметров как одного бассейна, так и их совокупностей обнаруживает ещё бóльшую предикторность в отношении ГБ.
4. Использование среднеарифметических показателей одноименных сосудов одного бассейна не обнаруживает преимуществ перед использованием в качестве независимых переменных каждого из слагаемых.
5. При ГБ выявлено достоверное утолщение сосудистой стенки разных бассейнов (кроме ПББА), а расширение диаметра – только у крупных артерий, и то одностороннее. Утолщение сосудистой стенки ассоциировано с повышением PWV, снижением диаметрального расширения и возрастанием напряжения.
6. Поиск при ГБ наиболее информативного сосудистого бассейна и его структурных и функциональных параметров не выявил приоритетности какого-либо из них, а обнаружил многоуровневое и неоднородное поражение сосудов при данной нозологии, диктующее необходимость в научных изысканиях состояния сосудов исследовать как можно большее их количество.
Библиографическая ссылка
Задорожная М.П., Разумов В.В. О «РЕПРЕЗЕНТАТИВНОМ» СОСУДЕ ИЛИ СОСУДИСТОМ БАССЕЙНЕ ПРИ ГИПЕРТОНИЧЕСКОЙ БОЛЕЗНИ // Современные проблемы науки и образования. – 2017. – № 4. ;URL: https://science-education.ru/ru/article/view?id=26696 (дата обращения: 19.04.2024).



