Введение
Одним из видов техногенных отходов, утилизация которых служит необходимым условием сбережения природных ресурсов, являются шлаки плавки цветных металлов. Их масса имеет порядок 107 т/год. Цинк из шлаков из-за его экономической ценности и для предотвращения разрушения футеровки аппаратуры, используемой на дальнейших этапах утилизации шлаков, следует извлекать на первой стадии переработки [3]. Для этой цели достаточно эффективна обработка шлака совместным раствором аммиака и NH4Cl в воде.
Цель исследования
Исследовать влияние на степень извлечения цинка из шлаков медной плавки состава аммиачно-аммонийного раствора, определив условия максимального извлечения цинка.
Метод исследования
Высокая эффективность совместных водных растворов аммиака и NH4Cl в воде для селективного выщелачивания цинка и меди из твёрдых материалов установлена ранее [7]. В эксперименте выщелачивание вели в мельнице мокрого помола аммиачно-аммонийным раствором при содержании аммиака в аммиачной воде 5, 10, 15, 20, 25% масс., NH4Cl − от 50 до 180 г/л. В отдельных сериях опытов при 298 К изучено влияние концентраций аммиака и NH4Cl, отношения Т : Ж, времени выщелачивания на степень извлечения цинка из шлака. Навеску шлака массой 20 г загружали в барабан мельницы с залитой аммиачной водой известной концентрации, объём которой соответствовал планируемому для данного опыта значению Т : Ж; в отдельных опытах в тот же барабан загружали расчётное количество NH4Cl.. После выщелачивания в течение намеченного времени опыта расфильтровывали суспензию и в фильтрате определяли концентрацию цинка методом трилонометрии [5].
![]() (1)
(1)
![]() , (2)
, (2)
СZn − содержание цинка в фильтрате, г/л; T − титр раствора трилона Б, равный 0,00327 г; а − объём раствора трилона Б, пошедшего на титрование, мл; 20 − объём пробы, взятой на титрование, мл; V − объём жидкой фазы в барабане мельницы, л; m − масса навески шлака, г; C − содержание цинка в шлаке, % масс. по данным заводских анализов.
Результаты исследований
В серии опытов получены данные, характеризующие скорость извлечения цинка от времени извлечения и концентрации аммиака в растворе (рис. 1). Показанные на рис. 1 кинетические кривые позволяют вычислить путём графического дифференцирования скорость выщелачивания в данный момент времени и среднюю скорость выщелачивания − V за время Δt при приращении концентрации цинка в растворе на величину ΔСZn [1].
![]() (3)
(3)
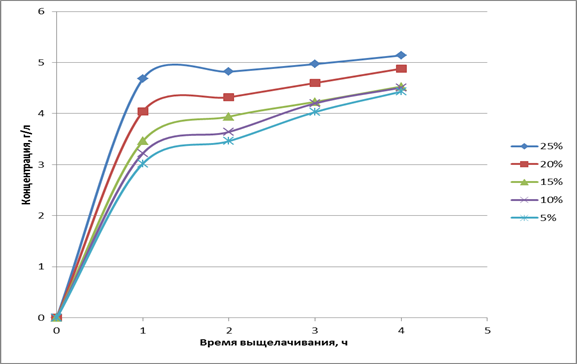
Рисунок 1 - Кинетические кривые
Из рисунка 1 видно, что за первый час выщелачивания происходит основной прирост концентрации цинка в растворе, далее значительный рост СZn в жидкой фазе при концентрации NH3 выше 10% масс. не имеет места. Из таблицы 1, в которой приведены величина порядка реакции и константы скорости образования аммиакатов цинка при его извлечении из шлака, видно практическое постоянство константы скорости извлечения цинка из шлака аммиачной водой в области концентраций аммиака в жидкой фазе 5-10%.
Таблица 1. Кинетические данные процесса извлечения цинка из шлака
|
Концентрация аммиака, % масс |
5 |
10 |
15 |
20 |
25 |
|
Порядок реакции |
1 |
1 |
1 |
1 |
1 |
|
Константа скорости, моль/сек |
0,74 |
0,75 |
0,74 |
0,75 |
0,75 |
Основные результаты эксперимента по определению степени извлечения цинка при различном составе экстрагирующего раствора и значениях Т : Ж представлены на рис. 2−4.
Из графиков рисунка 2 видно, что степени извлечения цинка возрастают с ростом концентрации аммиака в растворе, по крайней мере, для концентраций NH3 5−20% масс. Максимальное значение степени выщелачивания цинка 25%-ной аммиачной водой за 30 минут составило 63,2%, минимальное значение для 5%-ной аммиачной воды равно 40,8%. Те же величины для раствора, содержащего 20 и 25% масс. аммиака, незначительно отличаются, почти совпадая при времени извлечения более 3 часов. Опытные данные по зависимости степени извлечения цинка от содержания NH3 в экстрагенте показывают, что содержание NH3 около 20% близко к оптимуму. Ранее [2] показан заметный рост давления паров NH3 над экстрагентом и его потерь при содержании NH3 в воде выше 20% масс.
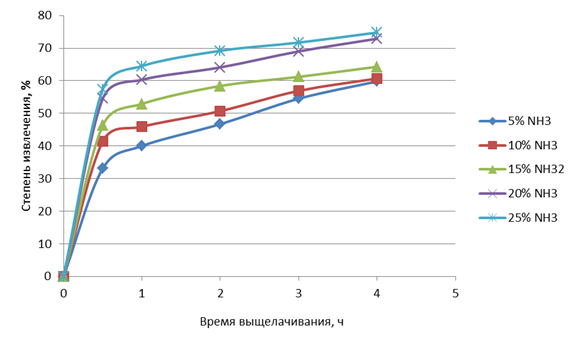
Рисунок 2 - Зависимость степени выщелачивания цинка от концентрации NH3
Известно, что в присутствии хлорид-иона возрастает растворимость аммиакатов цинка в аммиачной воде [4; 6], что, вероятно, связано с различным значением произведений растворимости соединений [Zn(NH3)4] (OH)2 и [Zn(NH3)4] Сl2. Из рисунка 3 видно, что влияние концентрации NH4Сl на достигаемую степень извлечения достаточно велико для практического использования, особенно для времени выщелачивания менее часа и при изменении концентрации NH4Сl с 50 до 150 г/л. Небольшая, порядка 5%, разница в значениях степени извлечения цинка при концентрациях хлорида аммония 180 и 150 г/л доказывает, что применять растворы, содержащие более 150 г/л NH4Сl, нецелесообразно.
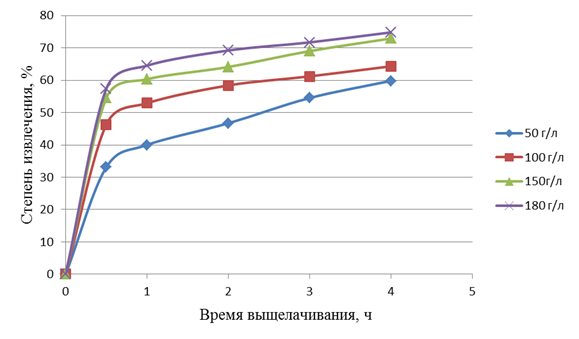
Рисунок 3 - Зависимость степени выщелачивания цинка от времени для 5% NH3
В отдельной серии опытов изучено влияние на степень извлечения цинка величины Т:Ж в интервале 1:10 − 1:25. Результаты эксперимента представлены графиками рисунка 4. Цинк извлекали раствором, содержащим 20% масс. аммиака и 150 г/л хлорида аммония. Как показано выше, указанные концентрации компонентов близки к оптимальным.
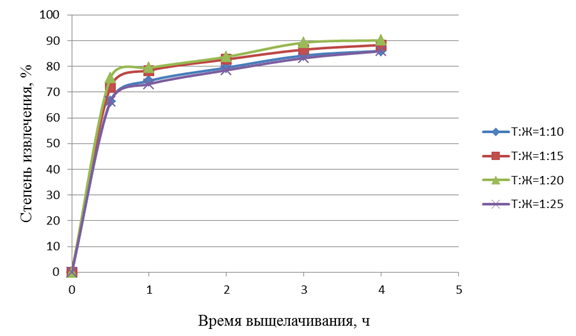
Рисунок 4 - Зависимость степени выщелачивания цинка от времени для 25% NH3 + 180г/л ![]()
Из рисунка 4 видно, что в принятом интервале изменения Т : Ж эта величина в общем оказывает относительно небольшое влияние на степень перехода цинка в раствор. Всё же следует отметить, что наибольшая степень извлечения цинка (90%) достигнута в условиях опытов при Т : Ж равном 1: 20, рекомендуемом и для промышленных условий.
Выводы
1. Изучено влияние концентрации аммиака в экстрагирующем растворе на степень извлечения цинка. Установлено, что увеличение степени извлечения соединений цинка в раствор с ростом содержания в нём аммиака наиболее существенное в интервале изменения концентраций аммиака 5 − 20% масс.
2. Степень извлечения цинка из шлака растёт с увеличением концентрации в экстрагенте хлорида аммония в интервале концентраций NH4Сl до 150 г/л. Дальнейшее увеличение содержания NH4Сl не оказывает существенного влияния на извлечение цинка.
3. Для значений Т:Ж 1:10 ─ 1:25 изучено влияние Т:Ж на извлечение цинка. При всех изученных концентрациях аммиака и NH4Сl оптимальное значение Т:Ж равно 1:20.
4. Исследована зависимость степени извлечения цинка из шлака от времени проведения процесса. Установлено, что в условиях опыта основная масса цинка переходит в раствор в первый час, далее извлечение цинка происходит менее активно. Сделан вывод о нецелесообразности длительности процесса более двух часов. Графическим дифференцированием кинетических кривых определена константа скорости процесса извлечения цинка из шлака медной плавки.
Рецензенты:
Когтев С.Е., д.т.н., профессор, директор по развитию производства, ООО «Синтез ПКЖ» г. Дзержинск.
Казанцев О.А., д.х.н., профессор, профессор кафедры «Технология органических веществ», Дзержинский политехнический институт (филиал) Нижегородского государственного технического университета им. Р.Е. Алексеева, г. Нижний Новгород.



