Введение
Адсорбция микробиологических объектов, имеющих в водных средах отрицательный заряд, наиболее эффективно происходит на поверхностях, обладающих электроположительным зарядом. Однако ряд таких адсорбентов весьма ограничен, и еще более сузился после отказа от использования хризотилового асбеста. В связи с этим постоянно ведется поиск и разработка новых сорбентов с электроположительным зарядом, эффективных для адсорбции микроорганизмов. Развитие нанотехнологий в последние годы сделало возможным получение в достаточных количествах нового электроположительного адсорбента – оксигидроксида алюминия со структурой псевдобемита в виде пористых практически сферических агломератов. Закрепление агломератов на полимерных микроволокнах позволяет получить волокнистый материал с максимально доступной для микроорганизмов положительно заряженной развитой поверхностью, что позволяет с высокой эффективностью адсорбировать бактерии и вирусы из водных сред и биологических жидкостей [6]. Такой материал может использоваться для создания ранозаживляющих повязок, действие которых основано на адсорбции и инактивации патогенных микроорганизмов.
Целью настоящей работы является изучение закономерностей адсорбции микроорганизмов волокнистым сорбционным материалом на основе ацетатцеллюлозных микроволокон, модифицированных частицами псевдобемита, и его применение в качестве адсорбента с широким антимикробным спектром.
Экспериментальная часть
Волокнистый сорбционный материал получали по патенту [4]. Предварительно агрегаты нанопорошков алюмонитридной композиции, служащих прекурсором для синтеза оксигидроксида алюминия, деагрегировали с помощью струйного насоса по патенту [10]. Дзета-потенциал частиц псевдобемита определяли по их электрофоретической подвижности (Zeta Sizer Nano ZS). Морфологию сорбционного материала изучали методом электронной микроскопии (JEM 2100, Quanta 200 3D). Сорбционные свойства полученных образцов исследовали в статических и динамических условиях. В качестве модельных адсорбатов были выбраны анионный краситель эозин (С20Н6О5Br4K2), монодисперсные латексные сферы диаметром 0,33 нм, бактериофаг MS2 и бактерии различной морфологии [3; 5; 7]. Концентрацию эозина в растворе определяли фотоколориметрическим методом (Specol 1300). Количество латексных сфер определяли нефелометрически (Hanna HI 93703). Пробы на наличие бактериофагов MS2 исследовали методом Грациа с индикаторной культурой E.coli [5; 7]. Концентрацию жизнеспособных бактерий определяли высевом на чашки Петри с плотной питательной средой [3].
Обсуждение результатов
Волокнистый сорбционный материал представляет собой полимерную волокнистую матрицу с адгезионно закрепленными частицами псевдобемита и в виде отдельных пористых частиц или сплошного пористого покрытия (рис. 2). Содержание псевдобемита составляет 30−33% масс, удельная поверхность волокнистого сорбционного материала − 100–120 м2/г [5].
а)  б)
б) 
Рисунок 2. СЭМ–изображения полимерного волокна с частицами псевдобемита (а) и сплошным пористым покрытием псевдобемитом (б)
Изотерма адсорбции эозина волокнистым сорбционным материалом имеет выпуклую форму и описывается уравнением Лэнгмюра (рис. 3а). Резко восходящий начальный участок на изотерме обусловлен сильным взаимодействием адсорбата с адсорбентом, что подтверждается наличием участка нулевых концентраций на динамических кривых адсорбции (рис. 3б). Емкость материала на этом участке (до проскока) составляла 3,6 мг/г. Сорбционная емкость волокнистого сорбционного материала по эозину составляет 17,9 мг/г и определяется практически полностью емкостью псевдобемита, вклад ацетатцеллюлозных волокон в адсорбцию не превышал 0,07 мг/л. Полученные результаты говорят о высокой скорости адсорбции эозина в первоначальный момент времени.
а) 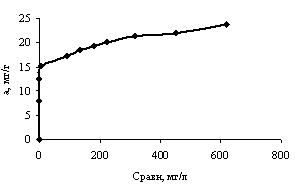 б)
б) 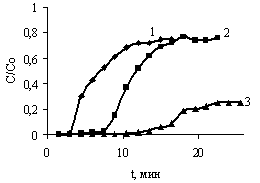
Рисунок 3. Изотерма адсорбции эозина (а) и динамические кривые адсорбции эозина волокнистым сорбционным материалом (б) при различных исходных концентрациях эозина: 1 –100 мг/л, 2 – 50 мг/л, 3 –25 мг/л
На динамических кривых адсорбции латексных наносфер, имитирующих вирусы, также имеется участок нулевых концентраций t0, который позволяет определить емкость сорбционного материала до проскока (рис. 4). Сорбционная емкость материала до времени t0 составила 4·1012 см-2. При этом латексные наносферы адсорбируются на агломератах нанолистов псевдобемита, в том числе в пространстве между нанолистами (рис. 5).
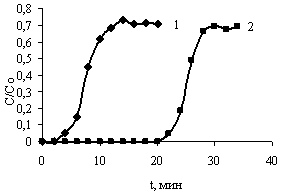
Рисунок 4. Динамические кривые адсорбции латексных сфер (1) – С0=1012 см-3; (2) –С0=1011 см-3

Рисунок 5. ПЭМ-изображение латексных сфер, адсорбированных на поверхности агломерата нанолистов псевдобемита
Исследование эффективности адсорбции живых культур микроорганизмов различной морфологии проводили на непатогенных культурах E. coli, St. aureus, P. aeruginosa (табл. 1). Проведенные исследования показали, что эффективность удержания микроорганизмов, имеющих близкие размеры, достигает 97-99% и не зависит от их морфологии, что позволяет прогнозировать эффективное улавливание микроорганизмов других видов [9].
Таблица. Адсорбция микроорганизмов волокнистым сорбентом
|
№ |
Наименование культуры |
Морфология микроорганизмов |
Эффективность адсорбции, % |
|
1 |
E. coli |
палочки, 1,5–3 мкм |
98,90±0,05 |
|
2 |
St. aureus |
кокковидные, 1,0–1,5 мкм |
97,17±0,18 |
|
3 |
P. aeruginosa |
палочки, 1,0–3,0 мкм |
98,25±0,11 |
Основной вклад в высокую эффективность удерживания бактерий вносит электростатическое взаимодействие между клеткой и электроположительным адсорбентом, обусловленное присутствием на взаимодействующих поверхностях разноименно заряженных и неполярных функциональных групп [7]. Также нельзя не учитывать тот факт, что бактериальные клетки могут формировать скопления микроорганизмов за счет сил взаимного притяжения и отталкивания [1], агрегироваться и удерживаться друг относительно друга с помощью дополнительных механизмов фиксации (тейхоевые кислоты, фимбрии, белки наружной мембраны и др.) [2; 8]. Возможно, в удерживании микроорганизмов на частицах псевдобемита принимает участие гликокаликс, представляющий собой полисахаридные волокна клеточной стенки бактерии, основная функция которого – адгезия к различным субстратам. Комплекс адсорбирующих приспособлений позволяет микроорганизмам достаточно прочно фиксироваться на частицах.
Еще одним подтверждением существенного вклада электростатических взаимодействий в адсорбцию микроорганизмов является различие эффективности адсорбции в дистиллированной воде и растворах электролитов. Так, максимальная сорбционная емкость волокнистого сорбционного материала по бактериям E. coli из дистиллированной воды составила 1011 КОЕ/см2, в то время как из водопроводной воды только 109 КОЕ/см2. Участок нулевых концентраций при адсорбции в динамических условиях бактерий E. coli из водопроводной воды также значительно меньше, чем из дистиллированной, для которой проскок в условиях эксперимента достигнут не был (рис. 6а). Ацетатцеллюлозная основа той же плотности и толщины, что и испытанные образцы, практически не сорбирует E. сoli, следовательно, удерживание бактерий за счет механической фильтрации микроволокнистым слоем пренебрежимо мало.
Эффективность извлечения бактериофага MS2 в сравнимых условиях ниже (107– 109 БОЕ/см3), чем бактерий (рис. 6б).
а)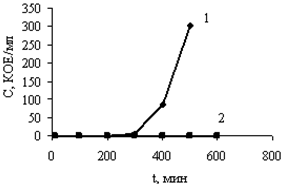 б)
б)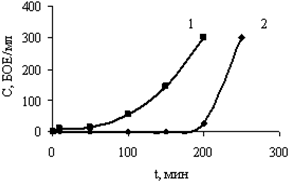
Рисунок 6. Динамические кривые адсорбции бактерий E. сoli (С0=105 КОЕ/см3): (а) и бактериофага MS2 (С0=105 БОЕ/см3) (б): 1 − из водопроводной воды; 2 – из дистиллированной воды
При этом наблюдается характерная для всех адсорбционных процессов обратная зависимость эффективности улавливания вирусов от начальной концентрации и скорости пропускания растворов через волокнистый сорбент. Увеличение эффективности улавливания с увеличением размера микроорганизма, при переходе от MS2 к E. сoli, связано, по-видимому, с увеличением вклада в результирующий процесс адсорбции инерционных сил и эффекта касания [5] наряду с зарядовыми взаимодействиями.
Для определения влияния поверхностного заряда адсорбента на его сорбционные свойства были измерены величины дзета-потенциала псевдобемита, бактериофага MS2 и псевдобемита с различным количеством адсорбированных вирусов. Измерения проводили в дистиллированной воде и в растворах KCl. По мере накопления бактериофага MS2 на поверхности псевдобемита наблюдалось уменьшение дзета-потенциала от исходного +39 мВ сначала до 0 мВ, а затем и до −41,0 мВ, что близко к заряду вирусов (рис. 7а) [5]. При этом адсорбция бактериофага продолжалась и после компенсации заряда поверхности псевдобемита (рис 7а).

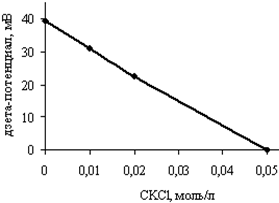
Рисунок 7. Зависимость дзета-потенциала оксигидроксида алюминия от количества адсорбированного бактериофага MS2 (С, БОЕ) (а) и концентрации KCl в растворе (б)
Зависимость дзета-потенциала от концентрации индифферентного электролита (KСl) в концентрационном интервале до 0,05 М носит убывающий характер с увеличением концентрации KCl (рис. 7б) и аппроксимируется прямой, что согласуется с уравнением Гельмгольца – Смолуховского и объясняет снижение адсорбционной способности материала с уменьшением дзета-потенциала в растворах электролитов (рис. 6).
Таким образом, адсорбция микроорганизмов обусловлена не только высокой удельной поверхностью и структурой материала, но и электростатическим притяжением адсорбатов к поверхности материала, а также адгезионными свойствами самих микроорганизмов, что значительно увеличивает скорость адсорбции и предотвращает десорбцию.
Заключение
На основании экспериментальных данных можно предположить, что адсорбция микроорганизмов волокнистым сорбентом, модифицированным частицами псевдобемита, обусловлена совокупным действием нескольких механизмов. В начальный период микроорганизмы приближаются и удерживаются на поверхности адсорбента за счет кулоновских сил, и процесс адсорбции можно рассматривать как электростатическое взаимодействие одиночных зарядов, которые компенсируют друг друга. При этом электрокинетический потенциал системы - сорбент-микроорганизм в целом приближается к нулю. По мере компенсации заряда электростатическое взаимодействие ослабевает и возрастает вклад в результирующий процесс адсорбции эффекта касания и адгезионных свойств самих микроорганизмов.
Совокупность характеристик разработанного материала (высокая удельная поверхность, доступность поверхности для адсорбатов, положительный заряд) показывает возможность применения его в качестве сорбента для удаления микроорганизмов из различных жидких и воздушных сред.
Работа выполнена при финансовой поддержке ГК 14.527.12.0001 и Программы фундаментальных исследований III.23.2.5.
Рецензенты:
Мамаева Вера Александровна, доктор технических наук, научный руководитель технологической группы ООО «Сибспарк» (резидента особой экономической зоны г. Томска), г. Томск.
Коботаева Наталья Станиславовна, доктор химических наук, старший научный сотрудник Учреждения Российской академии наук Институт химии нефти Сибирского отделения РАН, г. Томск.



