Введение
Аминокислоты относятся к классу органических амфолитов, их молекулы содержат одновременно карбоксильные и аминогруппы. Специфичность каждой аминокислоты определяется строением углеводородного радикала. Доказано, что глицин, подобно гамма-аминомасляной кислоте, является медиатором торможения в центральной нервной системы. Подтверждено его участие в патогенезе перинатальной ишемии. Примечательно, что β-аланин также является тормозным медиатором, действуя на те же рецепторы, что и глицин [9], при этом он является важным источником энергии для мышц, головного мозга и центральной нервной системы. Другими словами, аминокислоты влияют на функциональную активность клетки, свойства биологических мембран отдельных органов и их систем, или могут вызвать соответствующие изменения структурного состояния водного компонента биологической системы.
Существуют литературные данные, посвященные изучению влияния аминокислот на структуру воды [10]. Авторы работы [10] используют произведение Уальдена (произведение величины вязкости и проводимости при бесконечном разбавлении раствора) для оценки влияния аминокислот на структуру водной среды. В них показано, что большинство аминокислот обладают умеренной способностью разрушать структуру водных сред. С нашей точки зрения представляло определенный интерес изучить изменения структурного состояния воды в водных растворах глицина и аланина с использованием ИК- спектроскопии.
Цель работы
Установить влияние глицина, аланина и их смеси на водный компонент модельных растворов методом ИК-спектрометрии.
Материалы и методы исследования
В качестве исследуемых жидкостей использовали дважды перегнанную деионизованную воду, 1N растворы глицина (Гли) (50046 Sigma, SID 24873323), аланина (Ала) (05129 Sigma, SID 24845820).
Для исследования нами применялись аппаратно-программый комплекс «Икар» и ИК- спектрометр с Фурье-преобразованием Nicolet IS10.
Анализируемые образцы готовили непосредственно перед снятием спектра в кварцевой посуде быстрым последовательным десятикратным разбавлением исходных растворов от 101 до 1016 раз. Для проведения спектрометрии использовался аппаратно-программный комплекс «ИКАР», разработанный сотрудниками ТГМА совместно с НИИ-2 МО РФ, представляющий собой девятизональный спектроанализатор. Спектрометр сертифицирован как новый тип измерителя (сертификат № 5745 от 20.11.98 г.), который позволяет регистрировать показатели пропускания ИК-излучения после их многократного определения в девяти широких диапазонах в слоях жидкости толщиной 15 мк в кюветах из хлористо-бромистого и йодисто-бромистого таллия (KRS). В процессе анализа в кювету аппаратной части системы помещали 20 мкл полученного раствора и проводили многократные измерения коэффициентов пропускания в течение 30 с [3; 4]. За один цикл осуществляли около 300 измерений коэффициентов пропускания и в каждом из девяти диапазонов частот рассчитывали значения дисперсий, характеризующих флуктуацию инфракрасного спектра [9]. Полученные результаты обрабатывались методом линейного дискриминантного анализа в вычислительной среде интегрированной системы расчетов MATLAB (лицензия № 1462295). Предварительно было отмечено, что в каждом интервале длин волн наблюдалось нормальное распределение величин флуктуаций. Это дало возможность по девяти значениям дисперсий, определенных на исследуемых частотах спектра, количественно охарактеризовать состояния воды в присутствии сверхмалых количеств исследуемых веществ по сравнению с эталоном (бидистиллированная вода) с помощью критерия Махаланобиса, учитывающего корреляционные связи между коэффициентами пропускания и их дисперсиями [8]. В результате по величине отношений критерия «эталон – раствор» определяется близость (принадлежность) спектральной характеристики раствора к эталону.
Преобразование Фурье осуществляли с помощью Nicolet IS10 на компьютере в программной среде OMNIC.
Результаты и их обсуждение
На первом этапе работы нами была проведена ИК-спектрометрия с Фурье-преобразованием водных 1М растворов глицина, аланина, а также их смеси. Результаты спектрографии представлены на рис. 1.
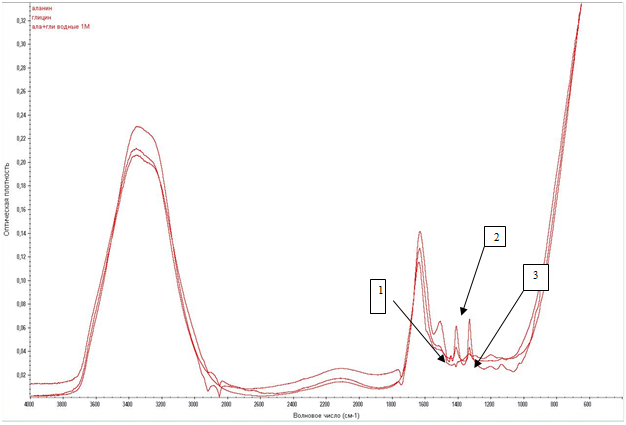
Рис. 1. Огибающие ИК-спектров 1N водных растворов аланина (1), глицина (2) и их смеси (3).
Все изучаемые растворы имеют интенсивную полосу поглощения в области 3000-3600 см-1, характеризующую валентные колебания гидроксильной группы воды [1; 7]. В ИК-спектрах водных растворов глицина и аланина проявляются пики в области около 3100-3150 см-1 ,что свидетельствует об увеличении энергетики водородной связи и структурировании воды. При длине волны 1620 см-1 наблюдаются характерные для деформационных колебаний воды пики, незначительно отличающиеся по интенсивности для исследуемых растворов. Различие в интенсивности максимумов 3100 см-1 - 3500 см-1 и 1620 см-1 для водных растворов глицина, по сравнению с растворами аланина, не значительно, что показывает сходное упорядочивающее действие аминокислот на структуру воды.
На следующем этапе работы было проведено исследование водного раствора глицина и аланина, полученного путем смешивания равных количеств 1N растворов исследуемых аминокислот.
В ИК-спектре этой смеси наблюдается наложение спектральных полос исследуемых аминокислот, при этом в спектре не происходило исчезновения полос поглощения, отвечающих одному из компонентов, как и не образовывалось новых спектральных полос, которые характеризовали бы образование новой связи, что говорит об отсутствии химических реакций взаимодействия данных веществ.
Анализ разведенных образцов аминокислот проводили с использованием АПК «ИКАР». Полученные данные показателей пропускания и их дисперсий обрабатывали методами многомерного анализа с вычислением критерия Махаланобиса.
Установлено (рис. 2), что для глицина анализируемый показатель изменяется волнообразно с достижением максимальных значений при разведении в 1016. Разведения раствора аланина приводят к постепенному снижению критерия Махаланобиса, для которого минимальное значение исследуемой величины определено при максимальном разведении.
Для данных аминокислот установлено, что исходные концентрации, а также одинаковое разведение растворов (105, 1016) вызывают разнонаправленное изменение структурного состояния водной основы растворов, что подтверждается величинами критерия Махаланобиса. Можно предположить, что в этом случае регистрируется неустойчивое состояние водной основы, которое, согласно литературным данным, возникает в тонких слоях жидкостей.
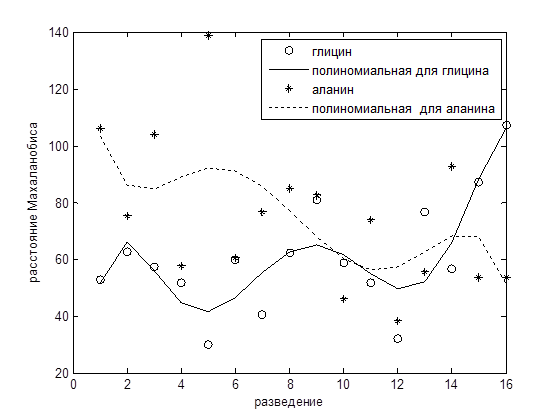
Рис. 2. Графики и их полиномиальная аппроксимация изменения расстояния Махаланобиса водных систем при разведении 1N раствора глицина и аланина.
Выводы
1. Анализ ИК-спектров водных растворов исследуемых аминокислот показывает, что в растворах аланина и глицина происходит упрочнение водородных связей между молекулами воды, за счет увеличения энергии связей ОН-групп.
2. Анализ спектральных линий смешанного водного раствора глицина и аланина подтверждает отсутствие изменения числа частиц за счет взаимодействия исследуемых веществ.
3. Установлено, что водная составляющая модельных растворов аминокислот по-разному изменяется при разведении исследуемых веществ. Вероятно, данное явление связано с процессами образования и распада гигантских кластеров, определяющих жидкокристаллическое состояние водных систем.
Рецензенты:
Лапина Галина Петровна, доктор химических наук, профессор, заведующая кафедрой физико-химической экспертизы биоорганических соединений ФГБОУ ВПО «Тверской государственный университет», г. Тверь.
Слюсарь Николай Николаевич, доктор медицинских наук, профессор, профессор кафедры химии и биохимии ГБОУ ВПО «Тверская ГМА» Минздрава России, г. Тверь.



