Введение. Проблема эндогенной интоксикации (ЭИ) в медицине в настоящее время занимает одно из важнейших мест. ЭИ затрудняет лечение заболеваний, способствует развитию осложнений и возникновению сопутствующих заболеваний. Эндотоксикоз лежит в основе развития тяжелых системных нарушений при различных патологических процессах и заболеваниях [6]. Несмотря на то, что пусковые моменты возникновения эндотоксикоза различны, патогенетические звенья его носят универсальный характер и включают в себя мембранодеструктивные процессы, рецепторные нарушения [2], изменения внутриклеточной деятельности и даже генома. При эндотоксикозе происходит выход в кровь из патологического очага токсических продуктов, их распространение по организму с током крови и воздействие на другие органы и ткани. В результате нарушается клеточно-тканевой обмен веществ и синтетические функции клеток [5].
Крайне тяжелое состояние больных и летальные исходы при остром панкреатите уже в ранние сроки, определяемые порой часами с момента заболевания, обусловлены тяжелым панкреатогенным эндотоксикозом, в связи с протеазной и липазной аутоагрессией [3]. Многочисленными исследованиями установлена и значимая роль в его патогенезе интенсификации перекисного окисления липидов (ПОЛ) [4, 7]. Регуляция интенсивности ПОЛ на различных уровнях осуществляется антиоксидантными системами [1], срыв которых приводит к лавинообразному накоплению токсических промежуточных и конечных продуктов пероксидации.
Поскольку в каскаде патологических процессов, приводящих к эндотоксикозу, существенную роль играют мембранодестабилизирующие явления, обусловленные гиперактивацией ПОЛ [3], то становится очевидный необходимость изучения фармакологической эффективности препаратов метаболического типа действия. В связи с чем, целью работы явилась оценка эффективности препарата метаболического типа действия этоксидола в коррекции эндогенной интоксикации при остром панкреатите.
Материалы и методы исследования. Основой работы явились экспериментальные исследования на 22 взрослых беспородных собаках обоего пола массой от 5,9 до 14,1 кг, разделенных на следующие группы: первая группа (n=11) – контрольная; вторая группа (n=11) – опытная.
Острый панкреатит моделировали по способу В. М. Буянова с соавт. (1989). Взрослым беспородным собакам выполняли срединную лапаротомию, проводили пункцию желчного пузыря с забором желчи и последующим лигированием места пункции. Далее желчь вводили в паренхиму вертикальной части поджелудочной железы по 0,5 мл в 5 точках. Таким образом, воспроизводили отечную форму острого панкреатита. В опытной группе на модели острого панкреатита оценивали ряд фармакодинамических эффектов этоксидола (ежедневные внутривенные введения 10 % раствора (10 мг/кг) в течение 5 суток).
В контрольные сроки исследования (1-е, 3-и и 5-е сутки) животным производили релапаротомию, оценивали состояние поджелудочной железы, определяли характер ее повреждений, а также производили биопсию ее тканей, забирали венозную кровь для дальнейшего исследования.
Для получения данных, принятых за норму, произведены исследования у 10 здоровых животных.
Все опыты проведены под внутривенным наркозом с использованием тиопентал-натрия из расчета 0,04 мг/кг массы тела животного. После проведения исследований животных выводили из эксперимента введением летальной дозы тиопентал-натрия.
В работе применялись следующие методы исследования. Выраженность эндогенной интоксикации оценивали по содержанию молекул средней массы (МСМ) при λ = 254 и 280 нм (Пикуза О. И., Шакирова Л. З., 1994); общую и эффективную концентрацию альбумина (ОКА и ЭКА) в сыворотке крови – флуоресцентным методом на специализированном анализаторе АКЛ-01 «Зонд»; резерв связывания альбумина (РСА) определяли по формуле РСА=ЭКА/ОКА; индекс токсичности (ИТ) плазмы – по формуле ИТ=ОКА/ЭКА – 1 (Грызунов Ю. А., Добрецов Г. Е., 1994).
Липиды из ткани поджелудочной железы экстрагировали хлороформметаноловой смесью (Хиггинс Дж. А., 1990). Липиды фракционировали методом тонкослойной хроматографии (Хиггинс Дж. А., 1990; Vaskovsky V.E. et al., 1975). Молекулярный анализ проводили на денситометре Model GS-670 (BIO-RAD, США) с соответствующим программным обеспечением (Phosphor Analyst/PS Sowtware).
Показатели интенсивности ПОЛ: диеновые конъюгаты (ДК) определяли спектрофотометрическим методом при длине волны 232–233 нм (Ганстон Ф.Д., 1986); уровень малонового диальдегида (МДА) – спектрофотометрическим методом в реакции с тиобарбитуровой кислотой (Sigma), активность супероксиддисмутазы (СОД) – в реакции с нитросиним тетразолием (Гуревич В.С. и др., 1990). Активность фосфолипазы А2 (ФЛА2) исследовали в среде, содержащей 10 ммоль трис-HCL-буфер (рH 8,0), 150 ммоль тритон Х-100, 10 ммоль CaCl2 и 1,2 ммоль субстрата, в качестве которого использовали фосфатидилхолины яичного желтка (Трофимов В. А., 1999).
Статистическую обработку полученных данных производили
общепринятыми методами статистики с определением достоверности различий между
данными в опытной и контрольной группах на основе расчета критерия Стьюдента,
корреляционную связь оценивали по критерию r.
Выявленные закономерности и связи изучаемых параметров между группами и признаками
были значимыми при вероятности безошибочного прогноза
р=95 % и более.
Научно-исследовательская работа проведена в рамках реализации ФЦП «Научные и научно-педагогические кадры инновационной России» на 2009–2013 годы.
Результаты исследования и их обсуждение
Опыты показали, что выбранная модель панкреатита оказалась вполне адекватной для решения цели и задач исследования. Во всех случаях у животных возникал острый панкреатит отечной формы, что подтверждалось макро- и микроскопически.
Полученные в контрольной группе опытных животных данные свидетельствуют о том, что при остром экспериментальном панкреатите развивается выраженная ЭИ. Содержание молекул средней массы (λ=254 нм и 280 нм) в плазме крови было повышено на 59,45–99,70 % (p<0,05) и на 81,43–98,29 % (p<0,05) соответственно. ИТ плазмы был повышен на 103,03–175,76 % (p<0,05) (рис. 1). ЭКА в плазме крови общего кровотока экспериментальных животных была снижена на 33,17–49,41 % (p<0,05), резерв связывающей способности альбумина уменьшался на 20,00–30,67 % (p<0,05).
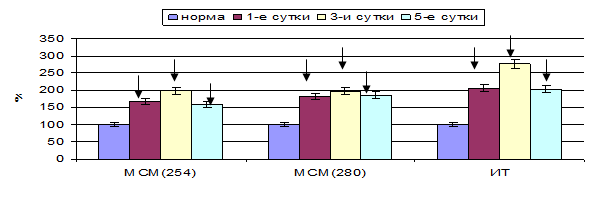
Рис. 1. Показатели эндогенной интоксикации плазмы крови общего кровотока при остром панкреатите отечной формы на фоне стандартной терапии (значения нормы приняты за 100 %)
Примечание: здесь и далее – достоверность отличия от нормы при p<0,05.
Таким образом, при остром панкреатите развивается синдром эндогенной интоксикации, при этом наиболее выраженные проявления эндотоксикоза зафиксированы на третьи сутки динамического наблюдения.
Известно, что одним из ключевых механизмов мембранодеструктивных процессов, ведущих к морфофункциональным расстройствам различных органов и тканей, выступает ПОЛ, достигающее значительной интенсивности при выбранной модели острого панкреатита. Нами установлено, что в тканевых структурах поджелудочной железы содержание ДК было повышено на 122,50–187,50 % (p<0,05), концентрация МДА превышала норму более чем в 1,5–2,5 (p<0,05) раза. Активность фосфолипазы А2 в ткани поджелудочной железы была повышена на 22,97–90,43 % (p<0,05) (рис. 2).
Выявлено, что при остром панкреатите происходит изменение количественного и качественного состава липидов тканей поджелудочной железы. Так, зарегистрировано снижение количества суммарных фосфолипидов – на 22,44–45,52 % (p<0,05), холестерола – на 2,32–53,31 % (р<0,05), фосфатидилсерина – на 11,99–69,60 % (p<0,05), фосфатидилэтаноламина – на 17,62–34,82 % (p<0,05); увеличение содержания эфиров холестерола на 24,97–33,17 % p<0,05), моноацилглицеролов – на 50,53–200,53 % (p<0,05), диацилглицеролов – на 100,00–1276,69 % (p<0,05), лизофосфолипидов – на 463,87–1125,21 % (p<0,05), сфингомиелина – на 84,48–151,40 % (p<0,05), фосфатидилхолина – на 31,89–33,68 % (p<0,05).
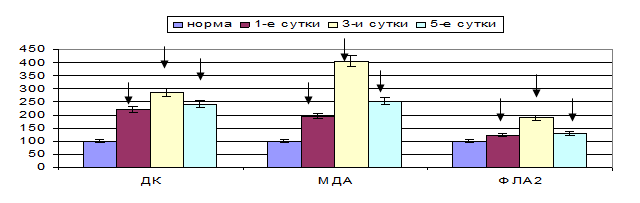
Рис. 2. Показатели перекисного окисления липидов в тканях поджелудочной железы при остром панкреатите (значения нормы приняты за 100 %)
Таким образом, полученные в контрольной группе животных результаты свидетельствуют о том, что при остром экспериментальном панкреатите в тканевых структурах поджелудочной железы происходит существенная модификация липидного метаболизма, свидетельствующая о развитии мембранодеструктивных явлений. Подчеркнем, что при статистической обработке данных определена достоверная корреляционная зависимость интенсификации процессов ПОЛ с развивающейся при остром отечном панкреатите эндогенной интоксикацией (табл. 1).
Принимая во внимание факт важнейшей роли расстройств липидного обмена в патогенезе острого панкреатита, целесообразным представляется исследование фармакодинамики препаратов метаболического типа действия, одним из объектов воздействия которых являются липиды или процессы, регулирующие их обмен. Из их многочисленного количества нами выбран этоксидол – препарат антиоксидантного типа действия.
При использовании препарата в плазме крови по сравнению с данными контрольной группы наблюдалось снижение содержания МСМ на 15,79–35,57 % (λ=254 нм) и 17,17–26,29 % (λ=280 нм) (р<0,05), а ИТ – на 26,37–47,76 % (p<0,05). Причем существенный эффект отмечен после первого введения препарата. ЭКА в плазме крови экспериментальных животных была выше данных группы контроля на 19,33–45,26 % (p<0,05), резерв связывающей способности альбумина – на 13,56–23,33 % (p<0,05) (рис. 3).
Таблица 1
Корреляционная зависимость между изменениями показателей эндогенной интоксикации и перекисного окисления липидов, фосфолипазной активности поджелудочной железы при остром панкреатите
|
|
ДК |
МДА |
ФЛА2 |
СОД |
|
ЭКА |
-1,00* |
-0,94* |
-0,89* |
0,85* |
|
ОКА |
-1,00* |
-0,90* |
-0,85* |
0,87* |
|
РСА |
-0,99* |
-0,86* |
-0,86* |
0,91* |
|
ИТ |
0,98* |
0,88* |
0,91* |
-0,92* |
|
МСМ (λ=254 нм) |
0,98* |
0,84* |
0,88* |
-0,93* |
|
МСМ (λ=280 нм) |
0,92* |
0,85* |
0,74 |
-0,81 |
Примечание: * – достоверная корреляционная зависимость.
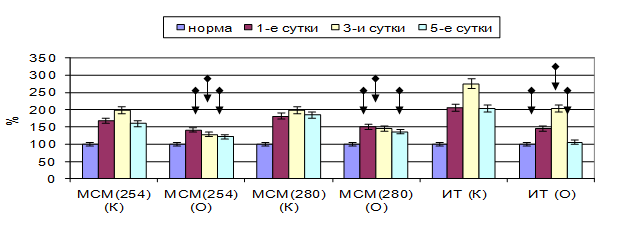
Рис. 3. Показатели эндогенной интоксикации плазмы крови при остром отечном панкреатите на фоне применения этоксидола (K – контрольная группа; О – опытная группа; значения нормы приняты за 100 %)
Опыты показали, что включение в терапию острого панкреатита этоксидола приводило к существенному уменьшению интенсивности процессов ПОЛ. Так, в тканях поджелудочной железы на фоне применения препарата содержание ДК было ниже данных группы контроля на 19,10–38,14 % (p<0,05), концентрация МДА – на 14,85–35,61 % (p<0,05), активность СОД – на 15,45–40,90 % (p<0,05). Интересен тот факт, что активность фосфолипазы А2 существенно снижалась уже после первого приема препарата и в целом уменьшалась по отношению к контролю на 12,84–19,72 % (p<0,05) (рис. 4).
По отношению к данным контрольной группы при применении этоксидола в тканевых структурах поджелудочной железы наблюдалось уменьшение содержания моноацилглицеролов на 20,98–62,70 % (p<0,05), диацилглицеролов – на 66,72–90,39 % (p<0,05), свободных жирных кислот – на 34,67–61,02 % (p<0,05), лизофосфолипидов – на 27,42–73,12 % (p<0,05), сфингомиелина – на 26,34–40,19 % (p<0,05), фосфатидилхолина – на 20,48–22,80 % (p<0,05), фосфатидилинозита – на 19,07 % (p<0,05), повышение уровня суммарных фосфолипидов на 31,35–69,89 % (p<0,05), холестерола – на 88,53 % (р<0,05), фосфатидилсерина – на 17,5–258,67 % (p<0,05), фосфатидилэтаноламина – на 17,25–46,27 % (p<0,05).
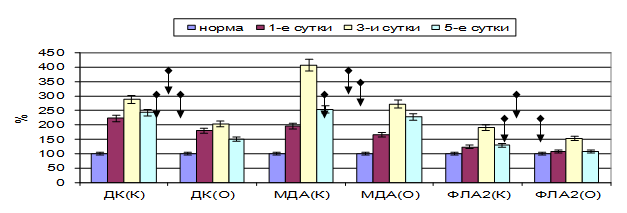
Рис. 4. Показатели перекисного окисления липидов в тканях поджелудочной железы на фоне применения этоксидола (K – контрольная группа; О – опытная группа; значения нормы приняты за 100 %)
Таким образом, анализируя полученные экспериментальные данные, отметим, что, во-первых, при использовании исследованного препарата метаболического типа действия явления ЭИ при остром панкреатите купируются быстрее, чем в контроле; во-вторых, одним из важнейших фармакодинамических эффектов, обусловливающих детоксицирующее действие препарата, является его способность купировать мембранодеструктивные явления в тканевых структурах органа поражения – поджелудочной железе, что существенно уменьшает поступление в кровоток токсических продуктов; в-третьих, мембранопротекторное действие исследованного препарата метаболического типа действия сопряжено с его способностью корригировать не только интенсивность процессов ПОЛ в тканевых структурах поджелудочной железы, но и с его депрессивным воздействием по отношению фосфолипазной активности.
Основываясь на данных, полученных в экспериментальном исследовании, можно сделать заключение, что этоксидол способствует уменьшению выраженности эндогенной интоксикации за счет способности купировать мембранодеструктивные процессы в тканевых структурах поджелудочной железы. Эти факты, на наш взгляд, имеют не только теоретическое, но и практической значение, особенно в аспекте того, что этоксидол – новое синтезированное производное 3-оксипиридина, показавшее высокую эффективность при исследованной патологии – остром панкреатите.
Выводы:
1. При экспериментальном панкреатите выраженность явлений эндогенной интоксикации находится в прямой зависимости от выраженности мембранодеструктивных процессов в тканевых структурах поджелудочной железы, липолитической активности, интенсивности процессов перекисного окисления липидов.
2. Применение при остром панкреатите этоксидола приводит к уменьшению выраженности эндотоксикоза. Об этом свидетельствует снижение индекса токсичности плазмы на 15,4–49,3 %, уровня молекул средней массы на 13,1–29,6 %, повышение эффективной концентрации альбумина на 17,9–44,8 %.
3. Одним из важных объектов реализации благотворного действия такого рода терапии является орган поражения – поджелудочная железа. Под влиянием этоксидола мембранодеструктивные явления в ней уменьшаются, снижается интенсивность процессов перекисного окисления липидов, уменьшается фосфолипазная активность.
Рецензенты:Смолькина Антонина Васильевна – доктор медицинских наук, профессор кафедры госпитальной хирургии медицинского факультета им. Т. З. Биктимирова ФГБОУ ВПО «Ульяновский государственный университет», г. Ульяновск.
Рубцов Олег Юрьевич – доктор медицинских наук, профессор кафедры факультетской хирургии ФГБОУ ВПО «Мордовский государственный университет им. Н. П. Огарёва», г. Саранск.



