В побегах вечнозеленых растений Ephedra monosperma Gmelin ex C.A. Meyer из семейства Ephedraceae обнаружен альтернативный путь превращения зеаксантина (Зеа) - его окисление с образованием фотозащитного вторичного ретрокетокаротиноида родоксантина (Rhd, 4´, 5´-didehydro-4,5´-retro-β,β-carotene-3,3´-dione) [2]. Ареал E. monosperma занимает наиболее континентальные области азиатского материка, включая Тибет и Монголию. В Якутии произрастает в южных, центральных и восточных районах [3]. Светолюбивое и засухоустойчивое растение, обладает всеми признаками крайней ксероморфности. На отдельных остепненных участках в составе сообществ является доминирующим видом, а также встречается в мертвопокровных толокнянковых сосняках. Особенностью видов эфедры является отсутствие зеленых листьев. Функцию ассимиляции несут побеги.
Целью настоящей работы является выявление динамики изменения фотохимической эффективности ФС II (фотосистемы II) и пигментного состава побегов E. monosperma при формировании морозоустойчивого состояния в условиях экстремального климата Якутии. Актуальность работы связана с проблемой устойчивости вечнозеленых растений в условиях криолитозоны.
Исследования проводили в 2008-2010 гг. в питомнике Якутского ботанического сада Института биологических проблем криолитозоны СО РАН, расположенного на второй надпойменной террасе долины р. Лены в 7 км к западу от г. Якутска (62°15´ с.ш., 129°37´ в.д.). Почвы участка слабозасоленные мерзлотно-лугово-черноземные супесчаные. Средняя температура воздуха за май-сентябрь 2009 г. составляла 14.2 ºС, сумма осадков 142 мм (среднемноголетняя величина - 161 мм) соответственно. Вегетационный период 2010 г. характеризовался средней температурой воздуха 13.5 ºС и суммой осадков 146 мм. Таким образом, исследуемые годы имели схожие погодные характеристики во время роста и развития растений при минимальных зимних температурах воздуха -46-48 ºС. В опытах использовали ассимилирующие побеги IV-V порядка и побеги первого года (VI порядок) зрелых генеративных растений. Отбор проб на пигменты осуществляли через 7-10 дней. Количественное определение хлорофиллов а и b (Хл а и b) проводили в 80%-ном ацетоновом экстракте [4; 5]. Качественный и количественный состав каротиноидов (Кар) анализировали методом ТСХ в нашей модификации [4; 5; 6]. Удельный коэффициент экстинкции E1%1cm для Rhd 2500 при 507 нм [1]. Каждый опыт состоял из трех параллельных биологических повторностей. Максимальный квантовый выход ФС II (или максимальную фотохимическую эффективность ФС II) как отношение переменной флуоресценции к максимальной: Fv/Fm = (Fm - Fo)/Fm определяли с помощью импульсного флуориметра Mini-PAM (Walz, Effeltrich, Germany) у 8-16 независимых биологических образцов [7]. Степень фотоингибирования определяли как снижение максимального квантового выхода в процентах по отношению к летнему максимальному значению Fv/Fm, определенному 10 августа 2010 г. Температуру воздуха на опытном участке регистрировали с помощью термографов DS 1922L iBitton («Dallas Semiconductor», США). В таблицах и графиках приведены средние арифметические значения и их стандартные отклонения. При определении долевого содержания индивидуальных Кар от суммы Кар относительная ошибка составила 5-6%. Все данные обрабатывались в среде электронной таблицы Microsoft Excel 2002 из пакета Microsoft Office с использованием макроса-дополнения XLSTAT-Pro. Статистическая поверка данных велась в пакете StatSoft Statistica 6.0.
Изучение содержания Хл и Кар в побегах E. monosperma показало, что их максимум наблюдается к окончанию ростовых процессов - в августе (табл. 1). В это же время отмечается минимальное содержание Лют+Зеа (лютеина и зеаксантина) - 0.24 ± 0.02 мг/гсух. массы (51.8 ± 4.3% от суммы Кар без учета Rhd), максимальный уровень (α+β)-Кар (каротинов) - 0.09 ± 0.01 мг/гсух. массы (18.5 ± 2.0%) за вегетационный сезон (рис. 1). Со второй половины августа до конца октября происходили выраженные изменения в пигментном составе (табл. 1; рис. 1), включая период вхождения в органический покой, первую и вторую фазы закаливания [8]. По наблюдениям 2009 и 2010 гг., при формировании морозоустойчивого состояния содержание Хл (a + b) в побегах уменьшается на 35-40%, а отношение Хл/Кар снижается почти в два раза по сравнению с летними значениями. К концу октября достоверно также снижается доля (α+β)-Кар до 13.6 ± 2.5% в сумме фотосинтетических Кар. При этом содержание Нео (неоксантина) остается практически постоянным. В летние месяцы в активно ассимилирующих побегах Rhd отсутствует (рис. 1). Его появление отмечается в начале сентября и по времени совпадает с началом снижения Хл и (α+β)-Кар, некоторым увеличением доли ксантофиллов (Ксан) в пуле желтых пигментов. Количество Rhd в верхних ассимилирующих побегах увеличивалось. Однако в нижних затененных частях побегов E. monosperma он отсутствовал. В течение первой фазы закаливания низкими положительными температурами (рис. 2) содержание Rhd нарастало от следовых до 19.6 мкг/гсух. массы (3.8 ± 1.2% от суммы Кар). Его максимальная концентрация (59.9 ± 16.3 мкг/гсух. массы или 10.8 ± 2.9% от суммы Кар) достигалась в начале второй фазы закаливания после 3-5 дней при установлении устойчивых отрицательных температур.
Таблица 1 - Содержание и соотношение пигментов (мг/гсух. массы) в побегах E. monosperma
|
Срок взятия проб |
Этапы развития растения |
Хл (a + b) |
Хл a/Хл b |
Сумма Кар* |
Хл/Кар |
|
конец июня-июль |
развитие и созревание семян, прекращение роста побегов в конце июля |
2.87 ± 0.27 |
3.6 |
0.46 ± 0.05 |
6.2 |
|
август |
процесс покрытия пробкой побегов, заложение почек |
2.83 ± 0.40 |
3.5 |
0.51 ± 0.06 |
5.6 |
|
сентябрь |
увеличение массы почек, 1 фаза закаливания |
2.49 ± 0.32 |
3.5 |
0.53 ± 0.04 |
4.7 |
|
октябрь |
2 фаза закаливания |
1.92 ± 0.21 |
3.5 |
0.56 ± 0.05 |
3.4 |
* - сумму Кар вычисляли с учетом содержания Rhd. Приведены усредненные данные за 2009 и 2010 гг.
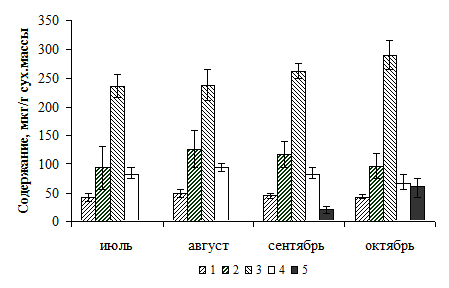
Рис. 1. Динамика каротиноидного состава в побегах Е. monosperma (2009-2010 гг.): 1 - Нео; 2 - Виo + Зea; 3 - Лют+Зеа; 4 - (α+β)-Кар; 5 - Rhd.
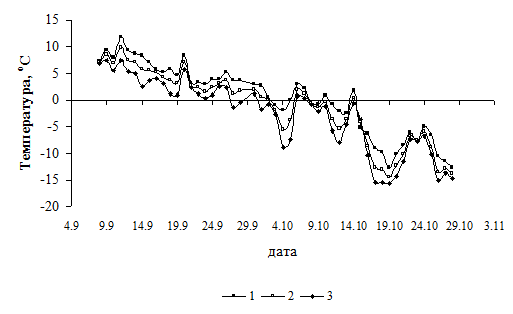
Рис. 2. Температура воздуха осенью 2010 г.: 1 - средняя температура за светлое время суток; 2, 3 - среднесуточная и ночная температура соответственно.
К концу сентября после прохождения недельного закаливания низкими положительными температурами (рис. 2) необратимое и обратимое фотоингибирование составило 17.9 и 9.1% по отношению к летнему максимальному значению Fv/Fm (рис.3). За этот период температуры были равны 3.6 ± 1.2, 2.3 ± 0.8, 1.0 ±1.3 °С в светлое время суток, за сутки, в ночное время соответственно. К началу достижения максимума содержания Rhd (к 6 октября) при наступлении слабых морозов (-3.8-5.6 °С 3-5 октября) необратимое фотоингибирование возрастало до 27.2%, обратимое до 15.7%, несмотря на кратковременное потепление до низких положительных температур 6 октября. В дальнейшем к середине октября обратимое фотоингибирование при снижении ночных температур до -5-8 °С достигало максимальных значений 26.6-27.1% (рис. 3), которое происходило в результате тушения параметров Fo и Fm (фоновой и максимальной флуоресценции Хл) с участием пигментов виолаксантинового цикла (ВЦ). В дальнейшем его глубина практически оставалась постоянной и не зависела от дальнейшего снижения температур до -40-45 °С в зимние месяцы. При -12.4-15.6 °С величина необратимого фотоингибирования составила 47.8-52.7%.
Снижение фотосинтеза в конце августа и начале сентября при вхождении в покой растения приводит к нарушению баланса между световой энергией, адсорбируемой реакционными центрами фотосистем, и энергией, потребляемой в темновых реакциях фотосинтеза. Снижение общего количества Хл (а+b) начинается задолго до заморозков на самой ранней стадии фотоингибирования ФС II и направлено на уменьшение эффективности абсорбции света ФСА на единицу площади [9]. Это способствует обеспечению фотостаза в первую фазу закаливания, а также, по-видимому, регуляции фотофизических процессов во вторую фазу закаливания при углублении степени необратимого фотоингибирования. Несмотря на снижение Хл, «избыточный» свет при неуклонном снижении температуры приводит к образованию АФК (активных форм кислорода), которые могут быть вторичными мессенджерами в образовании Rhd из Вио при его окислении [10].
Нами установлено, что клетки с красным пигментом в побеге располагаются в 2-3 ряда в паренхиме под эпидермой, с солнечной стороны, убывая и исчезая в теневой части среза побега [2]. При невысоком содержании Хл (1.4-2.5 мг/гсух. массы в период присутствия Rhd) он эффективно поглощает значительную часть фотоактивной радиации в зеленой области спектра и может образовывать эффективные ловушки излучения в широкой полосе 450-600 нм [1]. Солнечное излучение наиболее глубоко проникает в ассимилирующие ткани растений в этой области. Формирование «фотозащитного экрана» и поддержание его функционирования в неблагоприятные периоды требует минимальных затрат энергии, что позволяет обеспечить длительную фотоадаптацию реликтового растения. В отличие от ферментативных систем, функционирование «пассивного родоксантинового экрана» не зависит от понижения или колебаний температуры и может работать также эффективно в зимние месяцы, что крайне важно для вечнозеленого растения.
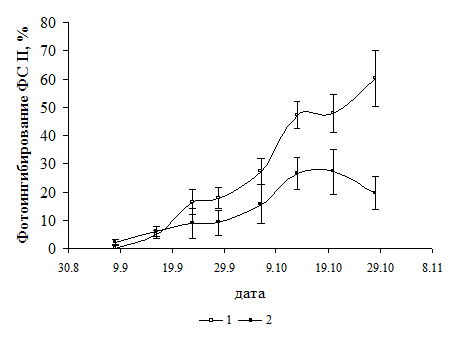
Рис. 3. Динамика фотоингибирования ФС II в побегах Е. monosperma (2010 г.): 1, 2 - необратимое, обратимое фотоингибирование. Планки погрешностей представляют ± стандартные отклонения (n = 16).
В отличие от вечнозеленых хвойных деревьев, рост фракции - Лют + Зеа - при прохождении закаливания слабо выражен. По-видимому, ее небольшое увеличение (рис. 2) происходит в основном за счет ингибирования обратной реакции ВЦ [11].
Судя по динамике обратимого фотоингибирования, Зеа начинает присутствовать круглосуточно при снижении средних ночных температур до +1.0-3.0 °С. Подъем уровня пигментов ВЦ наблюдается также во вторую фазу закаливания, что позволяет поддерживать нефотохимическое тушение избыточной световой энергии растением на достаточном уровне независимо от pН люмена при отсутствии электронного транспорта. В отличие от P. sylvestris усиление образования Лют в побегах растений E. monosperma во время закаливания не отмечается. По-видимому, Ксан усиливают различные способы нефотохимического тушения Хл [12] в оставшихся активных и дезактивированных комплексах ФС II и ФС I, в то время как образование Rhd происходит в результате трансформации хлоропластов в нефотосинтезирующие хромопласты [10].
Статья подготовлена в рамках проведения VI Съезда Российского фотобиологического общества в рамках госконтракта № 14.741.12.0157 Министерства образования и науки Российской Федерации.
Рецензенты:
- Данилова Н.С., д.б.н., профессор, зам. директора Ботанического сада Северо-Восточного федерального университета им. М.К. Амосова МоиН РФ, г. Якутск.
- Миронова Г.Е., д.б.н., профессор кафедры высокомолекулярных соединений, органической и биологический химии биолого-географического факультета Северо-Восточного федерального университета, г. Якутск.
Работа получена 23.11.2011



