В последние годы отмечается неуклонный рост числа больных желчнокаменной болезнью [1]. Одним из тяжелых осложнений этого недуга является механическая желтуха, лечение которой остается непростой задачей [2]. До сих пор нередки случаи неблагоприятных исходов лечения этой категории больных [3].
Регулярно проводимые конференции и симпозиумы, посвященные лечению механической желтухи, констатируют значительный прогресс в диагностике, тактике и применении современных методов оперативных вмешательств при этом синдроме [4].
Вместе с тем основной причиной, ухудшающей прогноз хирургического лечения больных обструктивной желтухой, является прогрессирующий эндотоксикоз с развитием тяжелой печеночно-клеточной недостаточности [5].
Миниинвазивные вмешательства на внепеченочных желчных путях отличаются эффективностью в предупреждении прогрессирования гепатодепрессии [6]. Их своевременное применение позволило решить многие задачи в лечении больных механической желтухой [7]. Однако следует признать, что до настоящего времени существенное число пациентов поступают в клинику с запущенной формой механической желтухи, и применение современных хирургических вмешательств в данных случаях не всегда успешно [8]. Это определяет необходимость в совершенствовании консервативной терапии, направленной на восстановление или препятствующей прогрессированию развития печеночной недостаточности при желтухе механического происхождения [9].
Цель исследования: при механической желтухе неопухолевого происхождения оценить в раннем послеоперационном периоде эффективность комбинированной терапии в коррекции печеночной недостаточности.
Материал и методы исследования
Клинико-лабораторные исследования проведены у 34 оперированных больных механической желтухой неопухолевого происхождения. Пациенты рандомизированы по полу и возрасту, характеру и выраженности патологии. Выделены: І группа (сравнения, n=16), в которую включены больные, получавшие стандартную терапию; ІІ группа (исследуемая, n=18) – пациенты, которым дополнительно в основное лечение включены лазерная терапия и инфузии ремаксола.
Анализируемые показатели, принятые за физиологическую норму, исследованы у здоровых лиц (n=15) обоих полов в возрасте 22–65 лет.
Клинико-лабораторные исследования проведены после получения информированного согласия пациентов.
Причинами механической желтухи являлись: холедохолетиаз – у 21 пациента (61,8%), стеноз терминального отдела холедоха – у 7 больных (20,6%) и хронический панкреатит – у 6 больных (17,6%). Больным выполнялись открытые оперативные вмешательства в объеме холецистэктомии – 23 пациентам (67,6%), внутреннего дренирования желчевыводящей системы: формирование холедоходуоденоанастомоза – 18 пациентам (52,9%) и холедохоеюноанастомоза – 5 больным (14,7%), наружного дренирования – 11 (32,4%).
Всем пациентам в раннем послеоперационном периоде проведено комплексное лечение, в которое включали инфузионный, спазмолитический, обезболивающий и иные компоненты. Больные исследуемой группы получили дополнительно лазеротерапию (накожное облучение в проекции кубитальной вены по 15 минут аппаратом «Матрикс») и ремаксол (ежедневно в виде внутривенных инфузий в объеме 400,0 мл) в течение 6 суток. При этом общий объем инфузионной терапии уменьшали на 400,0 мл.
Критерии включения: продолжительность заболевания меньше 4 суток; возраст от 30 до 65 лет. Критериями исключения являлись: длительность заболевания более 5 суток; возраст старше 65 лет или моложе 30 лет; наличие тяжелой сопутствующей патологии; применение пациентами других гепатопротекторов.
В работе использованы тесты, позволяющие оценить некоторые функциональные характеристики печени: содержание билирубина, активность трансаминаз, концентрации мочевины и креатинина, а также ряд показателей гомеостаза: интенсивность перекисного окисления липидов и фосфолипазную активность оценивали по содержанию молекулярных продуктов – диеновых коньюгатов и малонового диальдегида и активность фосфолипазы А2, выраженность эндогенной интоксикации – по содержанию молекул средней массы, индексу токсичности плазмы по альбумину и коэффициенту интоксикации.
Оценку расстройств гомеостаза производили в течение первых 6 суток после хирургических вмешательств.
Статистическая обработка полученных результатов произведена при помощи программы Statistica 12.0., оценка проведена с применением t-критерия Стьюдента.
Результаты исследования и их обсуждение
Исследованиями установлено, что у больных механической желтухой неопухолевого происхождения группы сравнения возникали выраженные нарушения со стороны функционального состояния печени и существенные расстройства гомеостаза на организменном уровне.
Клинико-лабораторные исследования показали увеличение в сыворотке крови уровня общего и прямого билирубина до 140 и 85 мкмоль/л соответственно. Отмечены увеличение активности как аланиновой, так и аспарагиновой аминотрансфераз более чем в 2,5 раза (р<0,05), уменьшение индекса де Ретиса до 0,91 (р<0,05). В крови возрастала концентрация мочевины более чем в 3 раза (р<0,05) и креатинина более чем в 2 раза (р<0,05).
Отметим, что уже при поступлении больных в клинику отмечены заметные отклонения гомеостатических показателей. В первую очередь обращало внимание существенное повышение в крови уровня токсических продуктов как гидрофильной, так и гидрофобной природы.
Так, содержание молекул средней массы повышалось более чем на 80% (р<0,05), индекс токсичности плазмы по альбумину и коэффициент интоксикации возрастали более чем в 3 раза (р<0,05) (рис. 1). Несомненно, в патогенезе синдрома эндогенной интоксикации важную роль играет не только поражение печени, но и воспалительные явления вследствие основного заболевания.
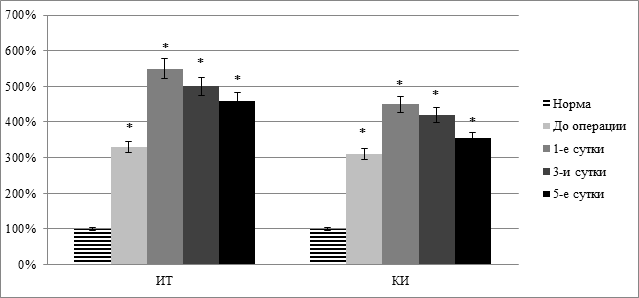
Рис. 1. Показатели индекса токсичности (ИТ) и коэффициента интоксикации (КИ) при механической желтухе в динамике
Важнейшим механизмом поражения печени наряду с известными причинами, связанными с желчным блоком, безусловно, является поражение гепатоцитов вследствие повышенной активности перекисного окисления мембранных липидов и активности фосфолипаз.
Оказалось, что содержание диеновых коньюгатов в плазме крови повышалось на 64,1% (р<0,05), малонового диальдегида – на 57,2% (р<0,05), активность фосфолипазы А2 возрастала более чем в 2,5 раза (р<0,05).
По всей видимости, в гепатодепрессии определенную роль играет и нарушение микроциркуляции, что нами зарегистрировано уже при поступлении пациентов в клинику. Так, показатель микроциркуляции снижался на 48,2% (р<0,05), индекс эффективности микроциркуляции падал на 28,3% (р<0,05) на фоне повышения индекса шунтирования на 56,1% (р<0,05).
Нами установлено, что через сутки после ликвидации блока желчи явления гепатодепрессии, судя по динамике всех исследованных показателей, увеличивались. Подтверждалось это прежде всего изменением активности аланиновой аминонотрансферазы и ростом в крови токсических продуктов.
Укажем, что на фоне восстановления желчединамики явления оксидативного стресса и активность фосфолипаз возрастали. Увеличивались и расстройства микроциркуляции. Этот факт указывает на важность этих патологических процессов в патогенезе поражения печени и после операции, с одной стороны, и определения вектора терапии по их предупреждению – с другой.
Установленный факт и определил выбор схемы гепатопротекторной терапии у больных механической желтухой неопухолевого генеза.
В исследуемой группе нами применена комплексная терапия, включающая лазерное транскутанное воздействие и инфузии ремаксола. Выбор был обусловлен тем, что низкоинтенсивное неионизирующее излучение, обладая важными положительными эффектами, имеет и высокую способность восстанавливать микроциркуляцию, а ремаксол способствует коррекции процессов липопероксидации и, как установлено нами ранее, уменьшению активности фосфолипаз.
Результаты клинико-лабораторного исследования показали, что выбор такого рода комплексной терапии был целесообразным. Оказалось, что у больных исследуемой группы отмечено меньшее поражение печени. В частности, в первые 3 суток выявлено достоверное снижение в сыворотке крови уровня общего и прямого билирубина на 17,4% и 19,2% (р<0,05) соответственно. Отмечены снижение активности аланиновой и аспарагиновой аминотрансфераз на 24,1% и 16,2% (р<0,05) соответственно, рост индекса де Ретиса. В крови снижалось содержание мочевины на 24,1% (р<0,05) и креатинина на 16,1% (р<0,05).
Заметный эффект отмечен при коррекции синдрома эндогенной интоксикации. Так, содержание молекул средней массы на фоне комплексной терапии у больных механической желтухой снижалось на 22,9% (р<0,05), индекс токсичности плазмы по альбумину и коэффициент интоксикации уменьшались соответственно на 26,1% и 32,7% (р<0,05) (рис. 2).
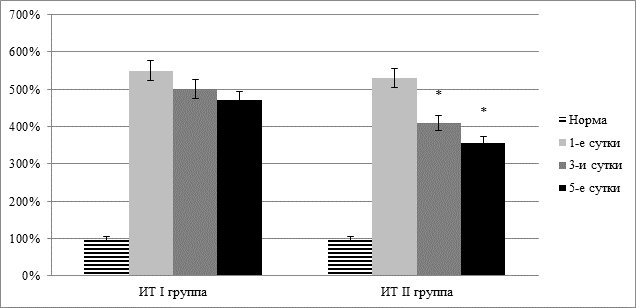
Рис. 2. Динамика индекса токсичности плазмы при механической желтухе на фоне комплексной терапии
Действенный эффект обнаружен по отношению перекисного окисления мембранных липидов и активности фосфолипаз. Оказалось, что содержание диеновых коньюгатов в плазме крови снижалось на 27,4% (р<0,05), малонового диальдегида – на 24,2% (р<0,05) (рис. 3). Зарегистрировано снижение активности и фосфолипазы А2 на 32,4% (р<0,05).
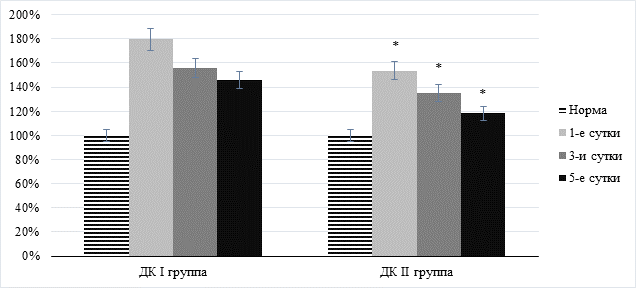
Рис. 3. Динамика содержания диеновых конъюгатов при механической желтухе на фоне комплексной терапии
На фоне проводимого комплексного лечения выявлены и меньшие нарушения микроциркуляции. Так, показатель микроциркуляции повышался на 19,8% (р<0,05), индекс эффективности микроциркуляции – на 16,1% (р<0,05), индекс шунтирования снижался на 19,5% (р<0,05).
Эффективность терапии отмечена и клинически. У больных механической желтухой неопухолевого происхождения зарегистрировано сравнительно благоприятное течение раннего послеоперационного периода, что проявилось прежде всего в уменьшении времени пребывания на 3,2 койко-дня (р<0,05). Немалую роль в этом сыграло уменьшение количества послеоперационных осложнений.
Выводы
Клинико-лабораторными исследованиями показана высокая патогенетическая эффективность комбинированной терапии. Ее способность влиять на основные триггерные механизмы сохранения гепатодепрессии в раннем послеоперационном периоде после восстановления пассажа желчи позволила сравнительно быстро уменьшить дисфункциональные явления со стороны печени, что положительно отразилось на результатах лечения этой категории больных.



