Одной из актуальных задач современной хирургии является оптимизация путей и способов хирургической помощи больным с грыжами передней брюшной стенки [1; 2]. С началом эры синтетических сетчатых протезов для дополнительного укрепления вновь сформированной передней брюшной стенки значительно уменьшилась частота рецидивов вентральных грыж, ранее достигавшая, по различным данным, от 10 до 45,5%. На сегодняшний день аллопротезирование брюшной стенки синтетическими материалами является золотым стандартом хирургического лечения вентральных грыж [3-5]. В мире за год производится около 1 миллиона герниопластик с использованием синтетических эксплантов [3; 6]. Использование последних привело к снижению частоты рецидивов до 10% и дало возможность ликвидировать обширные дефекты брюшной стенки, ранее считавшиеся некорригируемыми [1; 2; 6; 7].
Современная отечественная и зарубежная химическая промышленность выпускает синтетические протезы высокой прочности, имеющие относительную биологическую инертность [3; 5; 7]. На данный момент оптимальными протезирующими материалами являются полипропилен (ПП) и политетрафторэтилен (ПТФЭ, тефлон) [4; 8], остались ограниченно используемыми материалами нейлон, углеродное волокно, полиэстер, и оказались материалами, непригодными к протезированию передней брюшной стенки, серебряная проволока, нержавеющая сталь, поливинил, майлар, полиэтилен, фортизан, стекловолокно, рассасывающиеся протезы на основе полигликолевой кислоты и полиглактина [8; 9].
Вместе с тем основные типы протезов для герниопластики из ПТФЭ и ПП также имеют определенные недостатки: тефлон слабо фиксируется к тканям, что приводит к смещению протеза и рецидиву заболевания. ПП вызывает формирование грубой соединительно-тканной капсулы, сморщивающей герниопротез [9; 10]. Кроме того, в последние годы выяснилось, что применение синтетических материалов для герниопластики привело к появлению новых видов осложнений, ранее при данных операциях не развивавшихся. Это и миграция синтетического имплантата в брюшную полость, и спаечная кишечная непроходимость в результате адгезии кишки и сетки, и образование свищей в результате пролежня стенки кишки и эндопротеза, и образование сером в области расположения имплантата [9-11]. Поэтому остается актуальной проблема поиска пластического материала, отвечающего требованиям идеального герниопротеза, то есть имеющего не только высокую прочность, но и максимальную гистосовместимость [10; 11].
Большие надежды связаны с новейшей российской разработкой «Титановый шелк», предназначенной для пластики мягких тканей и изготовленной из титановой нити высокой степени очистки (сплав ВТ 1.00). Эндопротезы из чистого титана или его сплавов из никелида титана (НТ) отличаются высокой эластичностью, что обеспечивается специальной формой плетения металлических нитей. В ряде клиник Сибири и Зауралья, где в наибольшей степени изучили особенности его применения, до сих пор отдают предпочтение сетчатым металлическим эндопротезам из НТ перед всеми синтетическими материалами [12].
На сегодняшний день механические свойства современных полипропиленовых, металлических и композитных сетчатых протезов удовлетворяют хирургов [1-3; 12], но разработка способов снижения выраженной воспалительной реакции организма на имплантацию полипропиленовых материалов, позволяющей избежать ряда осложнений, характерных для герниопластики, остается актуальной задачей [6; 7; 9; 11].
Цель исследования. Сравнить в эксперименте на крысах характер местной пролиферативной воспалительной реакции, индуцированной инородным телом, в различные сроки после имплантации полипропиленовых и металлических сетчатых герниопротезов от различных производителей.
Материалы и методы исследования. Эксперименты выполнены на 48 крысах самцах линии «Вистар» из питомника ФГБУ «НИИЛ» Минздрава России (г. Астрахань), массой 150-170 г., распределенных случайным образом по 8 животных на 6 опытных групп (по количеству исследованных сетчатых эндопротезов). Животных содержали в виварии с естественным освещением при температуре 20-22 °С не более четырех животных в каждой клетке в одинаковых условиях на стандартном пищевом режиме в соответствии с «Международными рекомендациями по проведению медико-биологических исследований с использованием лабораторных животных».
В экспериментах исследовали облегченные сетчатые импланты последнего поколения из монофиламентного полипропилена 4 марок: Эсфил легкий («Линтекс», СПб, Россия), Эргон (ERGON EST, Италия), Optilene Mesh LP (B.Braun, Германия), Optomesh®ТhinLight («Матопат», Польша) и 1 сетчатый имплант из пористого двухслойного политетрафтороэтилена Dual-mesh (Gore-Tex, США). 6-й группе крыс имплантировали сетчатый металлический эндопротез, изготовленный из титановой нити «Титановый шелк» (ООО «НПФ ТЕМП», Екатеринбург, Россия). Массу 1 см2 каждого импланта измеряли на торсионных весах, для операции использовали стерильные фрагменты сетчатого эндопротеза квадратной формы размером 5×5 мм, то есть ¼ см2. Масса имплантированных квадратных фрагментов, измеренная на торсионных весах, для 5 синтетических эндопротезов колебалась в диапазоне 4-6 мг, а титанового шелка такой же площади составила 18±0,2 мг (табл.).
Техника операции: крысам в предварительно выстриженной межлопаточной области в асептических условиях под эфирным наркозом скальпелем производился разрез кожи до 5 мм длиной и в полученную рану в четырех разных направлениях пинцетом на глубину 1,5-2 см вводили стерильные фрагменты сетчатого эндопротеза. Операционная рана не ушивалась во избежание дополнительного влияния шовного материала на процессы воспаления и регенерации.
В послеоперационном периоде животных содержали поодиночке и на сроках 1, 3, 7 и 21 после операции выводили из эксперимента путем передозировки средства для наркоза в соответствии с Конвенцией по защите животных, используемых в эксперименте и других научных целях. Все четыре импланта одной крысы и три импланта от другого животного одной группы вместе с образовавшимися вокруг них капсулами отсепаровывали и после высушивания при 60 °С в течение 24 часов взвешивали и рассчитывали среднюю массу сухой капсулы, вычитая из нее массу исходного импланта, а четвертые импланты второй крысы с окружающей их капсулой и кожей использовали для гистологического исследования. Кусочки тканей с эндопротезом фиксировали и заливали в парафин. Срезы окрашивали гематоксилин-эозином, по Ван Гизону, по Вейгерту, импрегнировали по методу Фута. На препаратах, окрашенных гематоксилин-эозином, с помощью окуляр-микрометра измеряли в 50 участках толщину соединительнотканной капсулы в микрометрах (мкм) [9].
Результаты обработаны методом вариационной статистики при помощи пакетов программ Statistica 12.0, Stat Soft, Inc и Microsoft Excell 2003. Статистическую обработку данных проводили с применением методов описательной статистики и корреляционного анализа. Для признаков, имеющих нормальное распределение, вычисляли среднее арифметическое и ошибку: М ± m и сравнивали по t-критерию Стъюдента. Для групп признаков, отличающихся от нормального распределения, вычисляли U-критерий Манна-Уитни. Различия между выборками считали статистически значимыми при р < 0,05.
Результаты исследований и их обсуждение. Массы имплантированных фрагментов размером ¼ см2 достоверно не отличались у 4 типов сеток и составляли от 4 до 5 мг (табл.), достоверно (p<0,05) выше остальных имплантов была исходная средняя масса сетки B.Braun - 5,7±0,26 мг, а металлической сетки «Титановый шелк» - 19,0±0,58 мг. Следует отметить, что удельная масса всех сетчатых эндопротезов не соответствовала плотности, заявленной производителями хирургических сеток, и превышала ее в 2-6 раз. По нашим расчетам, среди полипропиленовых эндопротезов масса 1 см2 отечественной сетки Эсфил составляла 16,5 мг/см2 (165 г/м2), а импортных легких сетчатых эндопротезов Эргон -16,3 мг/см2 (163 г/м2), Optilene (B.Braun) - 23 мг/см2 (230 г/м2) и Optomesh - 19 мг/см2 (190 г/м2) вместо заявленных 28-36 г/м2. Масса 1 см2 двухслойной тефлоновой сетки Dual-mesh - 18 мг/см2 (180 г/м2) вместо заявленных 120 г/м2, а титанового шелка - 76 мг/см2 (760 г/м2) вместо заявленных производителем 120 г/м2.
Имплантация крысам стерильного сетчатого эндопротеза уже через сутки после операции вызывала у них пролиферативную воспалительную реакцию с формированием соединительнотканной капсулы вокруг инородного тела.
При микроскопическом изучении срезов инкапсулированных имплантов на разных сроках после операции отмечалась следующая картина, общая для всех типов сетчатых герниопротезов: под слоем подкожно-жировой клетчатки между поперечнополосатыми мышцами располагался имплант, окруженный капсулой, образованной соединительной тканью. В состав соединительной ткани входили коллагеновые, эластиновые и аргирофильные волокна, клеточные элементы преимущественно фибробластического ряда, а ближе к импланту с внутренней поверхности выявлялись гигантские клетки инородных тел и макрофаги. Вновь образованная ткань на 7-й и 21-й день была богата сосудами типа артериол, венул, капилляров. Морфологическая структура капсулы по своей толщине была неоднородной: непосредственно к импланту прилегала компактная соединительная ткань, содержащая много коллагена; по периферии капсулы располагался слой более рыхлой соединительной ткани, имеющей коллагеновые, эластические волокна и большое количество фибробластов. Импрегнацией по Футу выявлено значительное количество аргирофильных волокон, которые находились на границе и внутри ячеек сетчатого импланта и соединительнотканной капсулы, между капсулой и мышечной тканью.
Вместе с тем в строении соединительнотканной капсулы, ее клеточного состава у животных с имплантами различных типов существенных различий не обнаружено. Однако отличалась выраженность пролиферативных процессов и динамика увеличения морфометрических параметров фиброзной капсулы для различных полипропиленовых, тефлоновых и металлических сетчатых имплантов (рис., табл.).
Через 1 сутки после операции минимальные по массе соединительнотканные капсулы (6-7 мг) формировались вокруг полипропиленовой сетки Эсфил и Optomesh (табл.). Достоверно (p<0,05) более выраженные по массе капсулы (8,7±0,59 и 9,3±0,55 мг) окружали полипропиленовые импланты Эргон и B.Braun, но наиболее массивные по сравнению с Эсфил фиброзные капсулы (11,2±0,66 и 13,4±1,37 мг) образовывались в этот срок вокруг объемной тефлоновой сетки Dual-mesh и титанового шелка (p<0,05).
Фиброзная капсула минимальной толщины в 110-115 мкм на 1-е сутки после имплантации выявлена вокруг сеток Эсфил, Эргон и Optomesh (табл.). Капсула вокруг сетки B.Braun имела среднюю толщину 144±11,9 мкм (различие с Эсфил недостоверно), и только сетки Dual-mesh и титанового шелка со средней толщиной фиброзного слоя 156±13,6 и 158±13,0 мкм статистически значимо превышали толщину фиброзной капсулы вокруг сетки Эсфил (p<0,05).
Толщина стенок капсулы вокруг сетчатого импланта, измеренная под микроскопом на 50 участках, сильно варьировала в различных направлениях, что приводило к большой ошибке измерения и, как следствие, к меньшей информативности данного показателя для поиска различий в зависимости от типа синтетического импланта, чем масса сухой капсулы (табл.).
Среди всех имплантированных кусочков сеток формирование фиброзной капсулы происходило наиболее низкими темпами на протяжении всего срока наблюдения вокруг отечественного сетчатого импланта Эсфил: масса сухой периимплантной капсулы на 3-и сутки увеличилась только в 1,6 раза (с 6,3±0,38 до 10,2±0,64 мг), на 7-е сутки – до 19,7±0,81 мг, то есть почти в 2 раза по сравнению с 3-ми сутками и более чем в 3,1 раза по сравнению с 1-м днем. В дальнейшем к 21-му дню масса сухой капсулы вокруг сетки Эсфил увеличилась до 23,5±1,53 мг, однако динамика увеличения массы капсулы на 21-й день замедлялась, и по сравнению с 7-м днем масса увеличилась всего в 1,2 раза (табл., рис.).
Толщина стенок фиброзной капсулы вокруг сетки Эсфил, так же как и масса, была минимальной среди всех имплантированных сеток во все сроки исследования: 217±17,5 мкм на 3-е сутки, 413±39,2 – на 7-е и 591±56,4 – на 21-е сутки. В этой связи скорость образования фиброзной капсулы вокруг остальных сетчатых материалов оценивали в сравнении с имплантом Эсфил, вызывавшего минимальный пролиферативный воспалительный ответ.
Влияние имплантации сетчатых эндопротезов на морфометрические показатели асептической пролиферативной воспалительной реакции у крыс
|
Показатели |
Сутки |
Тип импланта |
|||||
|
Эсфил |
ERGON |
B.Braun |
Optomesh |
Dual-mesh |
Титан.ш |
||
|
Масса импланта (мг) |
4,1±0,15 |
4,1±0,17 |
5,7±0,26* |
4,8±0,20 |
4,6±0,18 |
19,0±0,58* |
|
|
Масса сухой капсулы (мг) n=7 |
1-е |
6,3±0,38 |
8,7±0,59* |
9,3±0,55* |
6,9±0,69 |
11,2±0,66* |
13,4±1,37* |
|
3-и |
10,2±0,64 |
14,1±0,81* |
17,0±1,00* |
12,2±0,72 |
15,9±1,22* |
18,5±1,71* |
|
|
7-е |
19,7±0,81 |
32,8±2,29* |
31,4±2,77 |
21,5±2,53 |
26,4±2,15 |
27,6±1,94* |
|
|
21-е |
23,5±1,53 |
38,4±2,12* |
36,1±9,3* |
27,9±2,69 |
39,9±1,60* |
30,3±1,65* |
|
|
Толщина стенок капсулы (мкм) n=50 |
1-е |
114±10,2 |
111±11,3 |
144±11,9 |
110±9,6 |
156±13,6* |
158±13,0* |
|
3-и |
217±17,5 |
234±17,6 |
283±24,5* |
269±22,6 |
295±26,0* |
309±27,2* |
|
|
7-е |
413±39,2 |
455±46,6 |
494±44,2 |
403±35,8 |
537±45,4* |
545±49,1* |
|
|
21-е |
591±56,4 |
670±71,0 |
735±68,4 |
568±53,7 |
777±69,7* |
692±60,5 |
|
Примечание: * – достоверные различия по сравнению с Эсфил (p<0,05).
Массы и толщины фиброзных капсул (табл.), а также динамика возрастания этих показателей в различные сроки после имплантации польского Optomesh практически не отличалась от Эсфил (рис.).
Вокруг итальянского сетчатого полипропиленового эндопротеза Эргон формировалась достаточно мощная фиброзная капсула следующей массы и толщины: 8,7±0,59 мг и 111±11,3 мкм на 1-е сутки; 14,1±0,81 мг и 234±17,6 мкм на 3-и сутки; 32,8±2,29 мг и 455±46,6 мкм на 7-е сутки и 32,8±2,29 мг и 670±71,0 мкм на 21-е сутки. Причем достоверно (p<0,05) на любом сроке от Эсфил отличалась только масса сухой капсулы, но не ее толщина (табл.).
Сходная динамика и интенсивное прорастание сетки соединительной тканью характерно для полипропиленового эндопротеза B.Braun, что отражает динамика увеличения массы и толщины фиброзной капсулы: на 1-е сутки она составляла 9,3±0,55 мг (p<0,05) и 144±11,9 мкм; на 3-и сутки – 17,0±1,00 мг (p<0,05) и 283±24,5 мкм (p<0,05); на 7-е сутки – 31,4±2,77 мг и 494±44,2 мкм и на 21-й день – 36,1±9,3 мг (p<0,05) и 735±68,4 мкм соответственно (табл., рис.).
Обращает на себя внимание, что максимальный рост массы фиброзной капсулы после имплантации двух полипропиленовых сеток Эргон и B.Braun наблюдается между 3 и 7 сутками после операции (рис.).
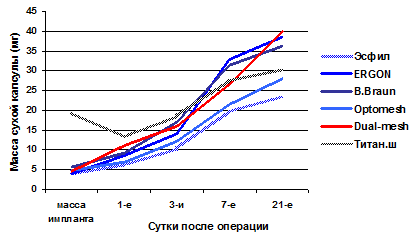
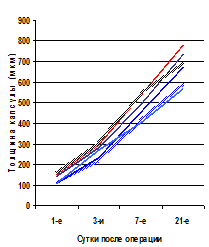
Динамика изменения массы и толщины фиброзной капсулы в различные сроки после имплантации сетчатых герниопротезов
Наибольшее прорастание фиброзной тканью и максимальную динамику пролиферативной воспалительной реакции после 7-го дня имплантации демонстрировал двухслойный тефлоновый эндопротез Dual-mesh (табл., рис.): на 1-е сутки средняя масса и толщина фиброзной капсулы составляла 11,2±0,66 мг и 156±13,6 мкм (p<0,05); на 3-и сутки – 15,9±1,22 мг и 295±26,0 мкм; на 7-е сутки – 26,4±2,15 мг и 537±45,4 мкм и на 21-й день – 39,9±1,60 мг и 777±69,7 мкм соответственно.
Имплантация титановой сетки с первых дней сопровождается мощным пролиферативным воспалением на сетчатый имплант «Титановый шелк», формирующим достоверно (p<0,05) более массивную фиброзную капсулу на 1-е сутки (13,4±1,37 мг и 158±13,0 мкм) и на 3-и сутки (18,5±1,71 мг и 309±27,2 мкм). Однако к 7-м и 21-м суткам динамика нарастания массы и толщины фиброзной капсулы снижается по сравнению с объемным эндопротезом Dual-mesh и даже полипропиленовыми Эргон и B.Braun: 27,6±1,94 мг (p<0,05) и 545±49,1 мкм (p<0,05) на 7-е сутки; 30,3±1,65 мг (p<0,05) и 692±60,5 мкм на 21-и сутки, хотя толщина капсулы продолжает достоверно увеличиваться до последнего дня наблюдений (табл., рис.).
Таким образом, тефлоновая и титановая сетки, так же как и некоторые полипропиленовые, эффективно выполняют еще одну, кроме механической, функцию: создают условия для постоянного воспаления и новообразования коллагена.
Выводы
Установлено, что минимальная фиброзная капсула формируется после имплантации отечественного полипропиленового сетчатого эндопротеза Эсфил и польского Optomesh. Из всех полипропиленовых сеток наиболее интенсивно после имплантации прорастала фиброзной тканью немецкая B.Braun и итальянская Эргон.
Более выраженная фиброзная капсула формируется после имплантации крысам сетчатых имплантов из пористого двухслойного политетрафтороэтилена Dualmesh (Gore-Tex, США) и отечественного металлического эндопротеза «Титановый шелк».
Полученные данные расходятся со свойствами эндопротезов, заявленными производителями, и этот факт следует учитывать при выборе сетчатого эндопротеза при аллопластике вентральных и паховых грыж.



