Глюкокортикоиды (GC) широко применяются при терапии лейкозов и лимфом как самостоятельный цитостатический препарат [7]. Биологические эффекты GC реализуются посредством активации глюкокортикоидного рецептора (GR) – фактора транскрипции, который регулирует экспрессию генов по двум различным механизмам. Терапевтическое действие GC реализуется через транс-репрессию – белок-белковое взаимодействие GR с факторами транскрипции, что приводит к снижению жизнеспособности опухолевых клеток. Развитие метаболических осложнений связано с запуском транс-активации, требующей связывания GR с респонсивными элементами в промоторных областях антиапоптотических генов [2, 4, 10].
За последнее десятилетие было предложено большое количество подходов по увеличению активности GC и снижению побочных эффектов от их применения. В частности, были описаны селективные агонисты глюкокортикоидного рецептора (SEGRA), которые не приводят к образованию гомодимера GR и, соответственно, запускают лишь транс-репрессорные механизмы [3, 8]. К классу SEGRA относится соединение растительного происхождения 2-(4-ацетоксифенил)-2-хлор-N-метилэтиламмоний хлорид, или CpdA. Ранее нами был продемонстрирован GR-зависимый противоопухолевый эффект CpdA in vitro и in vivo на моделях гемобластозов [1, 6]. Однако также было показано, что CpdA является нестабильной молекулой, распадающейся в водном растворе до производного азиридина, относящегося по классификации к канцерогенам класса 2Б [5, 9]. Аналоги CpdA с более стабильной структурой в литературе не описаны.
Таким образом, разработка путей химической модификации селективного модулятора GR, соединения растительного происхождения CpdA с целью увеличения стабильности и биологической активности данной молекулы, а также оценка биологических эффектов полученных соединений на модельной системе лейкозов и лимфом [1, 6] является актуальной задачей современной молекулярной биологии и экспериментальной онкологии.
Цель исследования
Целью данного исследования являлся синтез химического производного CpdA (аналога Синефрина), исследование его связывания с GR и оценка его GR-зависимых антипролиферативных и проапоптотических эффектов на модельной системе гемобластозов in vitro в сравнении с CpdA и дексаметазоном (Dex).
Материалы и методы исследования
Синтез CpdA–01. Синтез CpdA–01 был проведен по схеме, указанной на рис. 1.
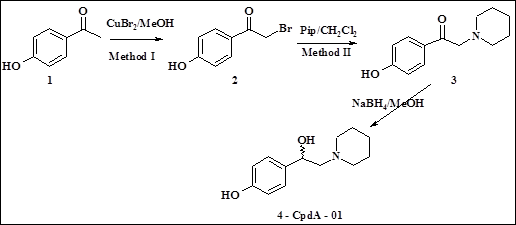
Рис. 1. Схема получения CpdA–01
Смесь ацетофенона1 (3.00 ммоль) и бромида меди (II) (7.50 ммоль) в метаноле (15 мл) перемешивали при комнатной температуре в течение ночи, затем кипятили до полного исчезновения в реакционной массе исходного кетона, вылили в ледяную воду (200 мл), экстрагировали хлористым метиленом (3×60 мл), объединённые органические фазы промыли водой (3×40 мл), профильтровали через слой (1 см) силикагеля, упарили и остаток очищали с помощью колоночной хроматографии на силикагеле (элюент петрол. эфир/этилацетат 6:1). Полученный твердый остаток (соединение 2) перекристаллизовали из смеси петролейный эфир-этилацетат. Далее смесь бромкетона2 (0.26 ммоль), пиперидина (0.55 ммоль) в абс. хлористом метилене (8 мл) перемешивали при комнатной температуре в течение 4 ч, затем – кипятили до полного исчезновения исходного бромкетона (ТСХ-контроль), вылили в ледяную воду (60 мл) и экстрагировали хлористым метиленом (3×20 мл). Объединённые органические фазы промыли водой (2×30 мл), высушили над сульфатом магния, упарили, остаток очистили с помощью колоночной хроматографии на силикагеле (элюент петрол. эфир / этилацетат/Et3N 3:1;0.05). Твердый остаток (соединение 3) перекристаллизовали из смеси петролейный этанола. Далее к охлажденному до 10 °С раствору аминокетона 3 (3.0 ммоль) в абс. метаноле (30 мл) порциями добавили боргидрид натрия (30 ммоль) и перемешивали раствор при комнатной температуре в течение 5 часов. Реакционную смесь вылили в воду (150 мл), экстрагировали этилацетатом (3×30 мл), экстракт промыли водой (50 мл) и упарили. Остаток очистили хроматографически (элюент петролейный эфир / этилацетат/Et3N 1:1:0,05), диастереомеры не были разделены. Остаток перекристаллизовали из смеси хлористый метилен-гептан. Получали 4-(1-гидрокси-2-пиперидин-1-илэтил) фенол 4. Выход 68 %. 1H ЯМР (300 МГц,DMSO-d6) 1.26-1.40 (m, 2H); 1.40-1.59 (m, 4H); 2.14-2.53 (m. 6H); 4.47-4.60 (m, 1H); 6.67 (d, 2H, J = 6.60 Гц); 7.10 (d, 2H, J = 6.60 Гц); Масс-спектр (EI, 70 eV): m/z (%) = 221.
Клеточные линии и обработка клеток. В работе использовали клетки острого лимфобластного лейкоза линии СЕМ и клетки мантийноклеточной лимфомы Granta, стабильные клеточные линии Granta-shGR и СЕМ-shGR с подавленной экспрессией GR, полученные нами ранее путем трансдукции в клетки указанных линий лентивирусных конструкций, экспрессирующий короткую шпилечную РНК к гену GR [6]. Клетки культивировали в стандартной среде RPMI-1640, содержащей 5 %-ную эмбриональную сыворотку телят и гентамицин (все реактивы «ПанЭко», Россия) (50 ед/мл) при 37 °С и в 5 %-ном СО2. Клетки обрабатывали CpdA,CpdA-01 и Dex(«Sigma-Aldrich», США).
Конкурентное связывание. Анализ связывания CpdA, CpdA-01 и Dex проводили с использованием набора для PolarScreen™ Glucocorticoid Receptor Competitor Assay (Invitrogen, США) по протоколу производителя. Вкратце, в 96-луночном черном планшете смешивали буферный раствор, содержащий рекомбинантный GR в концентрации 4 нМ, буферный раствор, содержащий 2,5 нМ флуоресцентно-меченого лиганда GR Fluormone GS1, а также водные растворы исследуемых соединений в конечных концентрациях 0,1 нМ-0,1 мМ. Далее пробы инкубировали в защищенном от света месте при комнатной температуре 4 ч. Поляризацию флуоресценции измеряли на микропланшетном ридере Infinite F500 Tecan (Tecan, Австрия) (волна возбуждения 485 нм, эмиссии – 535 нм). За концентрацию тестируемого соединения, при которой наблюдалось 50 % ингибирование связывания Fluormone GS1 (IC50), принимали ту концентрацию соединения, при которой наблюдалось уменьшение поляризации комплекса GR с Fluormone GS1 в 2 раза.
Определение антипролиферативного эффекта. Антипролиферативный эффект определяли путем прямого подсчета живых клеток. Клетки культивировали в 24-луночном планшете в присутствии исследуемых соединений или растворителя (0,1 %-ного этанола или ДМСО) с плотностью посева 50 тыс. клеток в лунке. Для дифференцировки мертвых и живых клеток использовали окрашивание трипановым синим, подсчет клеток проводили через 24 ч после обработки.
Определение уровня апоптоза. Уровень апоптоза определяли с помощью метода проточной цитофлуориметрии после окраски йодистым пропидием (PI), для чего клетки центрифугировали, осадок суспендировали в 1 мл раствора, содержавшего 5 мкг/мл PI, 0,1 % цитрата натрия и 0,3% NP-40. Полученные образцы анализировали на проточном цитофлуориметре FACSCalibur.
Статистическая обработка данных. Все эксперименты были повторены трижды. Средние значения и среднеквадратичное отклонение рассчитывали с помощью пакета программ MicrosoftExcel и сравнивали с парным двухвыборочным t-тестом Стьюдента для средних. Во всех случаях статистические критерии считали достоверными при Р<0,05.
Результаты исследования и их обсуждение
Химическое производное CpdA-01 (аналог Синефрина) является более стабильным и инертным соединением, не способным образовывать производное азиридина из-за отсутствия протона при атоме азота. Выбор стратегии синтеза (введение циклического вторичного амина взамен первичного амина) был обусловлен двумя факторами: первый из них, как было отмечено выше, связан с необходимостью исключить возможности образования азиридина [10]. Вторая причина обусловлена тем, что CpdA при гидролизе легко может давать производное Синефрина, обладающее собственным противоопухолевым эффектом.
Анализ связывания CpdA-01 с глюкокортикоидным рецептором
При исследовании связывания CpdA-01 было показано, что концентрация, при которой наблюдалось уменьшение поляризации комплекса GR с флуоресцентно-меченым лигандом Fluormone GS1 в 2 раза относительно максимума (825 mP), составило1,1 мкМ. Концентрации лигандов GR, CpdA и Dex, при которых наблюдалось 50 % ингибирование связывания Fluormone GS1, составили 0,52 мкМ и 0,67 мкМ. Таким образом, было показано, что CpdA-01 является лигандом GR и связывается с GR с аффинностью, сходной с CpdA и Dex.
Оценка противоопухолевого эффекта CpdA-01 in vitro
Антипролиферативные и проапоптотические эффекты препарата на клетки линии конкретной нозологической формы злокачественного новообразования в настоящее время определяют как противоопухолевое действие препарата in vitro. Нами были исследованы способность CpdA-01 подавлять пролиферацию клеток гемобластозов, а также индуцировать апоптоз. При изучении биологических эффектов CpdA-01 в первую очередь нами был проведен подбор его оптимальных концентраций для обработки клеток. Соединение исследовали в диапазоне концентраций 1 нм – 1мМ. Было показано, что рабочие концентрации CpdA-01 лежат в диапазоне 1–5 мкМ, что сравнимо с рабочей концентрацией дексаметазона и CpdA. В дальнейших экспериментах были использованы Dex, CpdA и CpdA-01 в концентрациях 1 мкМ. При определении антипролиферативного эффекта CpdA-01 было показано, это соединение обладает способностью подавлять пролиферацию клеток на уровне, сравнимом с Dexи CpdA. При инкубации клеток GrantacCpdA-01 в концентрации 1 мкМ доля жизнеспособных клеток составила 63,7±15,8 % после 24 ч, что сравнимо с 67,8±8,4 % живых клеток после обработки CpdA и 63,7±9,4 % – после инкубации с Dex (рис. 2), и согласуется с результатами предыдущих исследований [1, 6]. При исследовании клеток СЕМ число живых клеток после инкубации с CpdA-01 составил 65,4±3,7 % (рис. 3). Наблюдаемые для CpdA-01 эффекты были GR-зависимыми, поскольку данное соединение вызывало гибель клеток, в которым экспрессия GR была подавлена (Granta-shGR и СЕМ-shGR, рис. 2 и 3), в количестве, статистически незначимо отличимом от контроля.
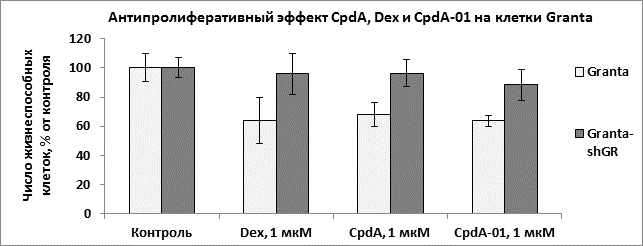
Рис. 2. Антипролиферативный эффект CpdA-01, CpdA и Dex на клетки Granta
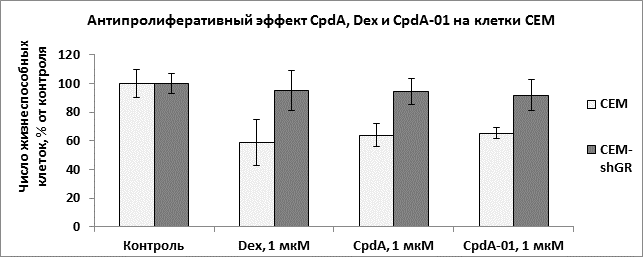
Рис. 3. Антипролиферативный эффект CpdA-01, CpdA и Dex на клетки СЕМ
Индукция апоптоза после обработки CpdA-01 наблюдалась в обеих клеточных линиях (табл. 1) и была сопоставима с уровнем апоптоза в данных клетках после обработки дексаметазоном и CpdA.
Таблица 1
Проапоптотический эффект энантиомеров CpdA в клетках СЕМ и Granta
|
Соединение, концентрация, время обработки |
% апоптотических клеток, клетки Granta |
% апоптотических клеток, клетки СЕМ |
|
Контроль, 48 ч |
3,5±0,6 |
6,7±1,4 |
|
Dex, 1 мкМ, 48 ч |
18,9±3,7 |
19,4±4,3 |
|
CpdA, 1 мкМ, 48 ч |
15,4±4,2 |
17,6±3,8 |
|
CpdA-01, 1 мкМ, 48 ч |
13,7±3,9 |
18,2±4,4 |
Таким образом, можно сделать вывод о том, что антипролиферативный эффект CpdA-01 связан с запуском апоптоза, причем CpdA-01 обладает эффектом на пролиферацию клеток лейкоза и лимфомы, сравнимым с эффектами исходной молекулы CpdA и Dex.
Заключение
В ходе данной работы было показано, что в клетках гемобластозов СЕМ и Granta производное CpdA-01 проявляет GR-зависимый антипролиферативный эффект, связанный с индукцией апоптоза в данных клетках. Таким образом, CpdA-01 является перспективным кандидатом для дальнейших исследований.
Работа выполнена при частичной поддержке грантов РФФИ №15-04-04006, 15-04-09216, 16-04-01410, а также гранта фонда Династия.



