Доброкачественная гиперплазия предстательной железы (ДГПЖ) вследствие широкой распространенности среди мужчин старшего возраста представляет собой важную медико-социальную проблему. Так, в возрастном диапазоне 51–60 лет она встречается приблизительно у 42 % мужчин, 61–70 лет – у 70 %, 81–90 лет – у 90 % [5]. Несмотря на широкомасштабное внедрение за последние десятилетия в практику хирургического лечения ДГПЖ различных малоинвазивных технологий, открытая аденомэктомия не потеряла свое значение, прежде всего, при аденомах больших размеров. В связи с высокой стоимостью оборудования, длительной кривой обучения и отсутствием рандомизированных исследований по изучению отдаленных результатов, малоинвазивные вмешательства все еще нельзя рассматривать как полноценную альтернативу открытой аденомэктомии при ДГПЖ больших размеров [12]. Поэтому не случайно в рекомендациях ведущих мировых урологических ассоциаций именно открытая операция признается основным методом лечения при больших размерах предстательной железы [7; 11]. По мнению P. Rigatti и A. Cestari [14], открытая аденомэктомия может успешно конкурировать с малоинвазивными методами хирургического лечения при условии совершенствования хирургической техники и минимизации кожного разреза наряду с использованием всех возможностей современного электрохирургического оборудования, позволяющих повысить эффективность и безопасность вмешательства.
С учетом отмеченных обстоятельств актуальным представляется оптимизация подходов к открытым методикам оперативного лечения при большом объеме ДГПЖ, чему и посвящено настоящее исследование по анализу результатов внедрения в практику модифицированной нами техники позадилонной аденомэктомии (ПАЭ).
Цель исследования
Оценка возможностей модифицированной техники ПАЭ по улучшению результатов лечения ДГПЖ больших размеров.
Материалы и методы
У 125 пациентов с ДГПЖ с объемом предстательной железы более 70 см3с 2007 по 2011 г. проведено оперативное лечение: у 83 человек выполнена ПАЭ по модифицированной технике, у 42 – чреспузырная (ЧАЭ) по традиционной технике. Характеристика пациентов в виде медианы (Me) и интерквартильного размаха [Q25%; Q75%] данных предоперационного обследования представлена в таблице 1.
Таблица 1
Сравнение групп пациентов по предоперационным данным
|
Показатель |
Me [Q25%; Q75%] |
p |
|
|
ПАЭ |
ЧАЭ |
||
|
Возраст, лет |
68 [63; 72] |
67,5 [64; 70] |
0,749 |
|
Показательшкалы IPSS, баллы |
21 [18; 24] |
21 [19; 26] |
0,271 |
|
Индекс качества жизни QOL, баллы |
5 [4; 5] |
4,5 [4; 5] |
0,857 |
|
Эректильная функция по анкете IIEF-5, баллы |
15 [13; 18] |
14 [12; 18] |
0,664 |
|
Уровень простатического специфического антигена ПСА, нг/мл |
6,3 [3,7; 10,8] |
5,6 [3,6; 9,7] |
0,703 |
|
Объем простаты, см3 |
110 [92; 131] |
120 [94; 150] |
0,262 |
|
Объем остаточной мочи, мл |
110 [70; 130] |
120 [80; 130] |
0,513 |
|
Максимальная скорость мочеиспускания, мл/с |
7,4 [5,4; 9,9] |
7,3 [5,3; 9,7] |
0,776 |
|
Средняя скорость мочеиспускания, мл/с |
3,4 [2,2; 4,1] |
3 [2,05; 4,15] |
0,585 |
Модифицированная техника ПАЭ включала следующие основные этапы: 1) рассечение капсулы предстательной железы между лигатурами, наложенными на дорзальный венозный комплекс; 2) обработка краев рассеченной капсулы в латеральных отделах с использованием аппарата «Ligasure»; 3) мобилизация узлов гиперплазии: край рассеченной капсулы в области латеральных углов разреза капсулы приподнимали и удерживали путем наложения зажима Люэра (с гемостатической и манипуляционной целью), мобилизацию узлов гиперплазии производили с использованием биполярных ножниц (без использования пальцевой диссекции); 4) узлы гиперплазии в процессе энуклеации удерживали пулевыми щипцами или зажимом Люэра; 5) в процессе выделения узлов гиперплазии осуществляли выделение и сохранение уретральной пластинки, а при возможности – сохранение простатического отдела уретры; 6) после удаления узлов гиперплазии капсула предстательной железы ушивали непрерывным однорядным швом (викрил 2/0-0).
Послеоперационный мониторинг пациентов включал обследование пациентов через 1, 3, 6, 12, 24 и 60 месяцев после вмешательства. В эти периоды проводили исследование показателя IPSS и индекса QOL, максимальной и средней скорости мочеиспускания, объема остаточной мочи и объема предстательной железы, уровня ПСА, эректильной функции по анкете IIEF-5, а также оценивали наличие различных послеоперационных осложнений.
Статистическая обработка данных проводилась с помощью пакета прикладных программ «Statisticav.17.0» производства компании «StatSoft» (США). Сравнение групп пациентов по количественным признакам производили с помощью U-критерия Манна –Уитни, по качественным признакам – критерия χ2. Динамику показателей до и после операции проводили с использованием метода Вилкоксона. При всех статистических тестах различие считали достоверным при уровне статистической значимости p<0,05.
Результаты исследования и их обсуждение
Из периоперационных результатов преимущество ПАЭ перед ЧАЭ отмечено по ряду критериев: по объему интраоперационной кровопотери и связанной с ним частоте; срокам дренирования мочевого пузыря; послеоперационному койко-дню; частоте интраоперационных и ранних послеоперационных осложнений (табл. 2).
Таблица 2
Сравнение групп по периоперационным показателям
|
Показатель |
Me [Q25%; Q75%] |
p |
|
|
ПАЭ |
ЧАЭ |
||
|
Операционное время, мин |
105 [100; 120] |
105 [95; 115] |
0,471 |
|
Объем кровопотери, мл |
250 [200; 400] |
400 [280; 450] |
0,015 |
|
Частота трансфузий, % |
2,4 |
14,3 |
<0,0001 |
|
Масса удаленной ткани предстательной железы, г |
88 [71; 107] |
93 [75; 108] |
0,256 |
|
Сроки дренирования мочевого пузыря, сутки |
7 [7; 8] |
11 [10; 13] |
<0,0001 |
|
Послеоперационный койко-день, сутки |
8 [8; 9] |
14,5 [12; 16] |
<0,0001 |
|
Частота интраоперационных и ранних послеоперационных осложнений, % |
10,8 |
31 |
<0,0001 |
Добиться минимальной кровопотери при ПАЭ удалось за счет анатомичного доступа непосредственно к предстательной железе и лучшей визуализации при выполнении всех этапов операции, что позволяло осуществлять гемостаз под полным визуальным контролем, реализуя все возможности электрохирургического оборудования. Использование аппарата «LigaSure» при модифицированной технике ПАЭ избавило от необходимости прошивания краев разреза капсулы предстательной железы, а использование биполярных ножниц при энуклеации узлов гиперплазии предстательной железы одновременно обеспечивало и функцию гемостаза. Эти обстоятельства привели не только к снижению объема кровопотери при данной операции, но и к сокращению времени выполнения вмешательства.
Одним из главных преимуществ ПАЭ является отсутствие необходимости дренирования мочевого пузыря эпицистостомой. Соответственно, сроки дренирования мочевого пузыря при ПАЭ короче и подразумевают использование только уретрального катетера. У пациентов, перенесших ЧАЭ, дренирование мочевого пузыря проводили как эпицистостомическим дренажом, так и уретральным катетером, а сроки дренирования мочевого пузыря оценивали по максимальному показателю использования одного из способов дренирования.
Важным критерием эффективности лечения служит срок послеоперационного пребывания пациента в стационаре, который является производной тяжести оперативного вмешательства и послеоперационной морбидности пациентов. Следовательно, минимальная операционная травма и меньшая морбидность пациентов после ПАЭ способствовала укорочению послеоперационных сроков реабилитации пациентов.
Наши результаты не отличаются от заключений других исследований, в которых также были отмечены преимущества ПАЭ перед ЧАЭ по периоперационным параметрам. Например, в исследовании M.F. Dall'Oglio et al. [3] выявлено, что медиана объема кровопотери при ПАЭ составила 362 мл, а при ЧАЭ – 640 мл, частота трансфузий – 3,3 и 12,5 % соответственно, обструкция уретрального катетера сгустками крови – 3,3 и 12,5 % соответственно, продолжительность ирригации мочевого пузыря – 2 и 3 дня соответственно. Однако среднее время нахождения уретрального катетера (5 дней) и стационарного периода лечения (6 дней) было одинаковым при обеих операциях. А в исследовании J.E. Bernie и J.D. Schmidt[4] было показано, что и по этим параметрам лучшие результаты характерны для ПАЭ: медиана срока катетеризации при ПАЭ составила 5 дней и при ЧАЭ – 7 дней, времени пребывания пациента в стационаре – 5 и 6 дней соответственно.
5-летние результаты оперативного лечения оценены у 75 (90,4 %) пациентов после ПАЭ и 38 (90,5 %) – после ЧАЭ. Итоговые показатели лечения в сравнении с дооперационными данными приведены в рисунке.
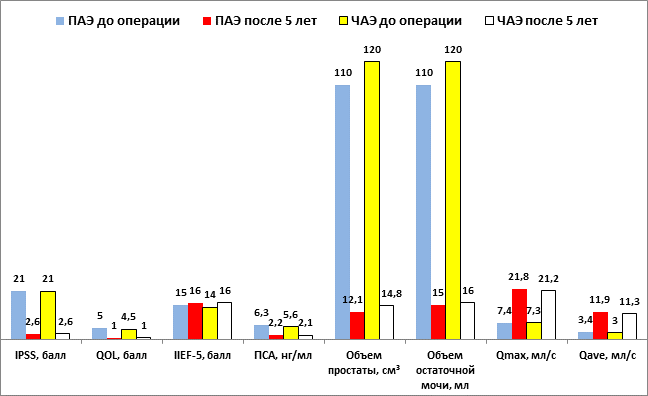
Показатели обследования до и через 5 лет после операции
После обоих вариантов операций установлено существенное уменьшение суммы баллов по шкале IPSS и индексу QOL, уровня ПСА, объема предстательной железы и остаточной мочи, увеличение максимальной и средней скорости мочеиспускания. Все эти изменения носили статистически значимый характер (p<0,05). При изучении эректильной функции достоверных изменений этого параметра при обоих методах лечения не выявлено (p>0,05). Таким образом, по степени влияния на динамику значений всех вышеуказанных показателей сравниваемые техники аденомэктомий не имели статистически значимых различий между собой. Аналогичные данные о выраженном улучшении указанных параметров после открытой аденомэктомии по сравнению с предоперационным уровнем были получены и в других исследованиях [1; 2; 6; 8; 10; 13].
Одним из основных критериев эффективности оперативного лечения служит частота поздних осложнений. Выявлено, что по данному показателю достоверно лучшие результаты были характерны для ПАЭ (табл. 3). При применении ПАЭ на протяжении 5 лет послеоперационного наблюдения не отмечено случаев таких поздних осложнений, как стриктура уретры или склероз шейки мочевого пузыря. Вероятно, достижению таких результатов способствовали следующие преимущества модифицированной техники ПАЭ: способ диссекции узлов гиперплазии с использованием электрохирургических инструментов, адекватная визуализация ложа аденомы в процессе энуклеации, сохранение задней уретральной пластинки, тщательный гемостаз под контролем глаза.
Таблица 3
Послеоперационные осложнения при 5-летнем сроке наблюдений
|
Вид осложнения |
Частота осложнения, %(число пациентов) |
p |
|
|
ПАЭ |
ЧАЭ |
||
|
Стриктура уретры |
0 |
2,6% (1/38) |
<0,0001 |
|
Склероз шейки мочевого пузыря |
0 |
5,3% (2/38) |
<0,0001 |
Выявленные нами хорошие отдаленные послеоперационные результаты ПАЭ сопоставимы с данными других исследований. К примеру, по данным J.M. Kozlowski et al. [9], частота склероза шейки мочевого пузыря после ПАЭ составляла 1–2,2 %, тогда как после ЧАЭ она составляла 3–6,9 %.
Заключение
Применение предложенной нами техники ПАЭ приводит к достоверному улучшению основных периоперационных показателей (объем интраоперационной кровопотери, частота трансфузий, сроки дренирования мочевого пузыря, сроки послеоперационного пребывания пациента в стационаре) и снижению частоты интраоперационных, ранних и поздних послеоперационных осложнений по сравнению с ЧАЭ. Полученные результаты позволяют утверждать, что модифицированная техника ПАЭ вносит существенный вклад в повышение эффективности и безопасности лечения ДГПЖ больших размеров. Это обстоятельство дает основание рекомендовать данный метод к широкому применению у пациентов указанной категории.



