Согласно современным представлениям, эндотоксикоз является сложным, многофакторным патологическим процессом, постепенно приобретающим все более универсальный характер, зависящий от основного звена – системной гипоксии тканей со всеми ее метаболическими последствиями [3].
В прогрессировании эндогенной интоксикации (ЭИ) при различных ургентных состояниях, в том числе и остром перитоните (ОП), значительную роль играет кишечник. Патологические изменения, происходящие в нем, связанные как с воспалительным процессом в брюшной полости, так и операционным вмешательством, приводят к развитию синдрома энтеральной недостаточности (СЭН), который включает в себя комплексное нарушение всех функций кишечника: моторной, секреторной, всасывательной [1, 8]. При этом частота возникновения данного синдрома на фоне ОП достаточно высока и составляет 45–85 % [6, 7].
Главными составляющими СЭН, которые способствуют прогрессированию хирургического эндотоксикоза, в частности при ОП, являются парез кишечника и повышение внутрикишечного давления, воспалительные изменения стенки тонкой кишки с нарушением в ней микроциркуляции, трофики, угнетением местного иммунитета и накоплением медиаторов воспаления, повышение проницаемости кишечной стенки на фоне изменения структуры микробной экосистемы и транслокации бактерий из просвета кишечника [8, 9]. С развитием паралитических нарушений кишечник, наряду с брюшной полостью, становится мощным дополнительным источником интоксикации, способствует ее прогрессированию, утяжелению состояния больного, нарастанию полиорганной недостаточности (ПОН) при ЭИ [2, 4].
Всесторонняя оценка эндотоксикоза позволяет четко ориентироваться в его проявлениях, своевременно прогнозировать ухудшение состояния больных и диагностировать осложнения, подбирать оптимальные программы лечения и приблизиться к опережающему характеру терапии [5]. В настоящее время известно и активно используется в практике множество методов, позволяющих оценить степень выраженности ЭИ. При этом нет четко сформулированных прогностических критериев эндотоксикоза по энтеральной недостаточности. В связи с чем целью работы явилось определение прогностических критериев эндогенной интоксикации по энтеральной недостаточности в эксперименте.
Материалы и методы исследования. Проведены опыты на 24 взрослых беспородных половозрелых собаках обоего пола, которым под тиопентал-натриевым наркозом (0,04 г/кг массы) моделировали перитонит по методу профессора А. П. Власова (1991) путем введения в брюшную полость 20 % каловой взвеси из расчета 0,5 мл/кг массы животного. Через 20–24 ч (I группа – серозный перитонит) или 42–48 ч (II группа – гнойно-фибринозный перитонит) выполняли лапаротомию, оценивали выраженность воспалительного процесса в брюшной полости и ее санировали. В контрольные сроки (1, 3, 5-е сутки) выполняли релапаротомию, судили об активности кишечной перистальтики, забирали кровь из бедренной артерии (общий кровоток) и вен брыжейки кишки (локальный кровоток). Стандартизированное ведение послеоперационного периода в первой и во второй группе включало антибактериальную (внутримышечные инъекции 2 раза в сутки раствора гентамицина из расчета 0,8 мг/кг массы) и инфузионную (внутривенные введения 5 % раствора глюкозы и 0,89 % раствора хлорида натрия из расчета 50 мл/кг массы животного) терапию.
В каждой группе оценивали активность кишечной перистальтики, интенсивность процессов перекисного окисления липидов в плазме крови общего и локального кровотока; выраженность эндотоксикоза на организменном и органном уровне, на основе чего рассчитывали индекс энтеральной недостаточности, как по количеству молекул средней массы, так и индексу токсичности и прогностический индекс энтеральной недостаточности.
Определяли выраженность эндогенной интоксикации. Содержание молекул средней массы (МСМ) в сыворотке крови измеряли на спектрофотометре СФ-46 при длине волны 250 и 280 нм (Пикуза О.И., Шакирова Л.З., 1994). Для характеристики физико-химических свойств альбумина определяли эффективную и общую концентрацию альбумина в сыворотке крови флуоресцентным методом на специализированном анализаторе АКЛ-01 «Зонд». Рассчитывали резерв связывания альбумина, индекс токсичности (ИТ) плазмы (Грызунов Ю.А., Добрецов Г.Е., 1994). Содержание малонового диальдегида (МДА) оценивали в реакции с 2-тиобарбитуровой кислотой.
Рассчитывали индекс энтеральной недостаточности в эксперименте по уровню молекул средней массы (ИЭН по МСМ):
ИЭН по МСМ = (МСМ2/МСМ1) х 100,
где МСМ2 – содержание молекул средней массы на организменном уровне,
МСМ1 – содержание молекул средней массы на органном уровне.
Определяли индекс энтеральной недостаточности в эксперименте по индексу токсичности плазмы (ИЭН по ИТП):
ИЭН по ИТП = (ИТП2/ИТП1) х 100,
где ИТП2 – индекс токсичности плазмы крови на организменном уровне,
ИТП1 – индекс токсичности плазмы крови на органном уровне.
Проводили расчет прогностического индекса энтеральной недостаточности в эксперименте (ПИЭН) по формуле:
МСМ2 + МСМ4 МДА2 + МДА4
ПИЭН = ---------------------- х -------------------- + КП;
МСМ1 + МСМ3 МДА1 + МДА3
где, МСМ1 – уровень МСМ организменного кровотока в текущий момент, МСМ2 – уровень МСМ брыжеечного кровотока в текущий момент, МСМ3 – уровень МСМ организменного кровотока в предыдущий момент, МСМ4 – уровень МСМ брыжеечного кровотока в предыдущий момент, МДА1 – уровень МДА организменного кровотока в текущий момент, МДА2 – уровень МДА брыжеечного кровотока в текущий момент, МДА 3 – уровень МДА организменного кровотока в предыдущий момент, МДА4 – уровень МДА брыжеечного кровотока в предыдущий момент, КП – коэффициент перистальтики: (КП=2 – отсутствие перистальтики; КП=1 – при слабой перистальтике (единичные кишечные шумы); КП=0 – при активной перистальтике).
Исследования проведены в соответствии с этическими требованиями к работе с экспериментальными животными («Правила проведения работ с использованием экспериментальных животных» (приказ МЗ СССР № 755 от 12.08.1987 г.) Федеральный закон «О защите животных от жестокого обращения» от 01.01.1997 г., «Об утверждении правил лабораторной практики» (приказ МЗ РФ от 19.06.2003 г. № 267) и одобрены локальным этическим комитетом.
Полученные цифровые экспериментальные данные обработаны методом вариационной статистики с использованием критерия t Стьюдента. Вычисления и построение диаграмм, отражающих динамику изученных показателей, совершали с поддержкой программы Microsoft Excel XP. Применен текстовый процессор Microsoft Word XP.
Результаты исследования и их обсуждение
Определение прогностических критериев эндотоксикоза по энтеральной недостаточности при различных формах перитонита у экспериментальных животных проводили, базируясь на сопоставлении клинических данных и результатов биохимических исследований крови.
В экспериментальной группе, где моделировали серозный перитонит, через сутки после операции в большинстве наблюдений отмечено отсутствие перистальтики кишечника, а в брюшной полости наблюдался воспалительный процесс – гиперемия и мелкоточечные кровоизлияния на париетальной брюшине, серозный выпот. Коэффициент кишечной перистальтики на данном этапе наблюдения оценивался в 1,8 балла. На 3 и 5-е сутки послеоперационного наблюдения почти у всех экспериментальных животных восстанавливалась в той или иной степени кишечная перистальтика – слабая или активная. Коэффициент кишечной перистальтики в эти сутки экспериментального исследования равнялся соответственно 0,8 и 0,3 баллов. Явления воспаления в брюшной полости стихали.
При моделировании гнойно-фибринозного перитонита на первом этапе (через сутки после операции) экспериментального исследования у всех животных наблюдалось отсутствие кишечной перистальтики (коэффициент кишечной перистальтики оценивался в 2,0 балла), выраженные воспалительные процессы в брюшной полости – гнойно-фибринозный выпот с наложениями фибрина на петлях кишки, париетальная брюшина была ярко гиперемирована, инфильтрирована с множественными кровоизлияниями. В одном наблюдении отмечено начало формирования нескольких межкишечных абсцессов. На 3-и сутки после санации брюшной полости у половины животных восстановления кишечной перистальтики не было, а в других случаях – она была слабая (коэффициент кишечной перистальтики равнялся 1,5 балла). Процессы воспаления в брюшной полости стихали, однако сохранялись кровоизлияния, инфильтрация и гиперемия париетальной брюшины, наложения фибрина на петлях кишок, серозно-фибринозный выпот. Во всех наблюдениях в брюшной полости наблюдался в той или иной степени выраженности спаечный процесс. В двух случаях формировались межкишечные абсцессы. На конечном этапе (5-е сутки после операции) послеоперационного наблюдения у всех животных кишечная перистальтика восстанавливалась, однако лишь в одном случае она была активная, в остальных – слабая (коэффициент кишечной перистальтики достигал 0,8 балла). Явления воспаления в брюшной полости стихали, но выявлялся спаечный процесс, который в одном опыте был выраженным. В одном наблюдении отмечены множественные межкишечные абсцессы с небольшим количеством серозного выпота в брюшной полости.
Индекс энтеральной недостаточности определяли по уровню гидрофильных и гидрофобных продуктов ЭИ в плазме крови общего и локального кровотока. При моделировании серозного перитонита индекс энтеральной недостаточности по молекулам средней массы увеличивался с нормального значения в 4,3 раза (p<0,05), а по индексу токсичности – в 2,9 раза (p<0,05). Через сутки после операции эти показатели продолжали нарастать и были выше нормы соответственно в 4,9 и 3,5 раза (p<0,05). На 3-и сутки наблюдения отмечено их снижение, хотя они были повышены в 3,9 и 3,0 раза (p<0,05). На конечном этапе (5-е сутки после операции) исследования нормализации их не наблюдалось, и они достоверно превосходили норму в 2,9 и 2,5 раза (таблица).
Аналогичная картина определялась и при подсчете индекса энтеральной недостаточности по молекулам средней массы и по индексу токсичности у экспериментальных животных при гнойно-фибринозном перитоните. При этом выявленные патологические изменения были не только выражены в большей степени, чем при серозном перитоните, но и выявлена тенденция к постоянному нарастанию значения индекса энтеральной недостаточности на всем протяжении послеоперационного периода, тогда как в первой группе опытов наблюдался его регресс.
Так, на этапе перитонита индекс энтеральной недостаточности, определяемый по количеству гидрофильных продуктов эндотоксикоза, увеличивался в 9,3 раза (p<0,05), на следующих этапах (1-е, 3-и и 5-е сутки) наблюдения он уже превосходил норму в 10,8, 13,5 и 15,1 раза (p<0,05). Подобная динамика изменения индекса энтеральной недостаточности выявлялась и при подсчете данного показателя по содержанию гидрофобных продуктов эндотоксикоза. При перитоните он был достоверно выше нормы в 3,6 раза, через сутки после операции – в 4,9 раза, через 3-е суток – в 6,4 раза и через 5 суток – в 7,0 раз (рис. 1).
Индекс энтеральной недостаточности и прогностический индекс энтеральной недостаточности при различных формах перитонита (M±m, n=12)
|
Показатель |
Норма |
Перитонит (до операции) |
Этапы послеоперационного наблюдения |
||
|
1-е сутки |
3-и сутки |
5-е сутки |
|||
|
Серозный перитонит |
|||||
|
Индекс энтеральной недостаточности по уровню молекул средней массы, усл. ед. |
3,39± 0,20 |
14,71± 0,48* |
16,45± 0,58* |
13,27± 0,30* |
9,71± 0,30* |
|
Индекс энтеральной недостаточности по индексу токсичности, усл. ед. |
6,90± 0,22 |
20,04± 0,45* |
23,87± 0,58* |
20,81± 0,50 |
16,93± 0,47* |
|
Прогностический индекс энтеральной недостаточности, усл. ед. |
2,69± 0,18 |
3,40± 0,21# |
2,35± 0,15# |
1,89± 0,12# |
|
|
Гнойно-фибринозный перитонит |
|||||
|
Индекс энтеральной недостаточности по уровню молекул средней массы, усл. ед. |
3,39± 0,20 |
31,68± 0,92* |
36,53± 1,05* |
45,87± 0,79* |
51,37± 1,09* |
|
Индекс энтеральной недостаточности по индексу токсичности, усл. ед. |
6,90± 0,22 |
25,07± 0,56* |
33,63± 0,45* |
44,01± 0,61* |
48,04± 1,01* |
|
Прогностический индекс энтеральной недостаточности, усл. ед. |
3,44± 0,16 |
3,96± 0,14# |
4,51± 0,16# |
5,42± 0,19# |
|
Примечание: # – достоверность разницы между показателями предыдущего и данного этапа исследования при p<0,05.
При проведении сравнительного анализа выраженности индекса энтеральной недостаточности при серозном и гнойно-фибринозном перитоните оказалось, что на всех стадиях экспериментального исследования при второй форме острого воспаления брюшины его значения были выше относительно первой формы – в 1,3–5,3 раза (p<0,05).
Определение прогностического индекса энтеральной недостаточности, рассчитанного по содержанию гидрофильных продуктов эндогенной интоксикации, уровню ТБК-активных продуктов в плазме крови общего и локального кровотока и коэффициенту кишечной перистальтики выявило следующее (рис. 2).
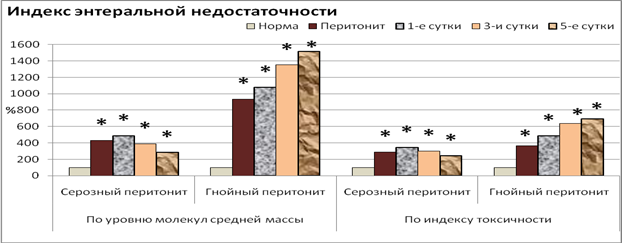
Рис. 1. Изменение индекса энтеральной недостаточности при различных формах перитонита
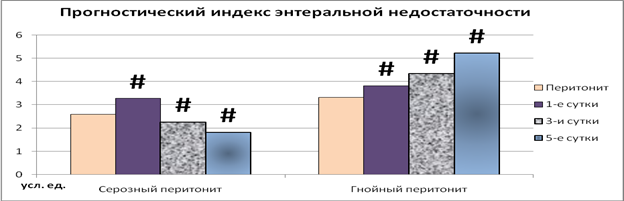
Рис. 2. Колебание прогностического индекса энтеральной недостаточности при различных формах перитонита; # – достоверность разницы между показателями предыдущего и данного этапа исследования при p<0,05
При серозном перитоните на этапе острого воспаления брюшины данный индекс равнялся 2,6 усл. ед. Через сутки после операции он увеличивался по сравнению с предыдущим этапом исследования на 26,1 % (p<0,05), через 3-е суток – данный показатель уменьшался относительно предыдущего этапа на 31,0 % (p<0,05) и через 5 суток после операции он был ниже предыдущего этапа на 19,4 % (p<0,05).
При гнойно-фибринозном перитоните наблюдалась иная динамика изменения прогностического индекса энтеральной недостаточности. На всем протяжении послеоперационного наблюдения отмечено нарастание его значения по сравнению с предшествующим этапом. Так, через сутки после операции этот показатель увеличивался по сравнению предыдущим (перитонит) на 15,3 % (p<0,05), через 3-е суток – (относительно 1-х суток) на 13,9 % (p<0,05) и на 5-е сутки – (при соотнесении с 3-ми сутками) на 20,3 % (p<0,05).
Заключение. Экспериментальные исследования свидетельствуют, что при моделировании острого перитонита независимо от морфологической формы у всех экспериментальных животных развивается энтеральная недостаточность, более выраженная при гнойно-фибринозном перитоните. Это подтверждается индексом энтеральной недостаточности, рассчитанным по количеству гидрофильных и гидрофобных продуктов эндотоксикоза в плазме крови общего и локального кровотока. При проведении стандартизированного послеоперационного ведения через сутки после операции при серозном перитоните энтеральная недостаточность нарастает. На следующих (3-и и 5-е сутки) этапах наблюдения явления энтеральной недостаточности уменьшаются, что подтверждается, прежде всего, восстановлением кишечной перистальтики. Об этом же свидетельствует и прогностический индекс недостаточности кишечника. В то же время при гнойно-фибринозном перитоните явления энтеральной недостаточности, несмотря на проведение стандартизированной терапии, купируются не столь быстро. Хотя постепенно отмечено восстановление функции кишечника, что подтверждается коэффициентом кишечной перистальтики, однако индекс энтеральной недостаточности и прогностический индекс энтеральной недостаточности продолжают увеличиваться, что свидетельствует не только о тяжести острого воспаления в брюшной полости и о неблагоприятной динамике патологического процесса в целом, но и позволяет продемонстрировать новые прогностические критерии ЭИ по энтеральной недостаточности при остром перитоните.



