Для клетки в состоянии стресса характерна перестройка метаболических и физиологических процессов, которые должны приводить к адаптации растительного организма к изменившимся условиям [6,7].
Исследовалось влияние токсического хрома (VI) на рост, содержание хлорофилла и активность каталазы растения пшеницы. Заметное увеличение активности каталазы наблюдали в побегах при обработке хрома (VI) [9]. Авторами [2] исследовалась роль каталазы в ответе дрожжей на окислительный стресс, индуцированный пероксидом водорода в культурах, находящиеся в середине экпоненциалной фазы роста. Показано, что в этих условиях при отсутствии цитозольной и пероксисомной форм каталазы жизнеспособность клеток дрожжей при обработке пероксидом водорода существенно уменьшается. При действии 0,5 мМ Н2О2 в течение 30 минут в клетках дрожжей возрастает активность обеих каталаз [2]. Однофакторный УФ-В и комбинированный (УФ-В и кислый дождь) стресс оказывали различное влияние на активность каталазы и фотосинтез у рапса. УФ-излучение и кислый дождь повышали активность каталазы, снижали содержание хлорофилла, интенсивность нетто-фотосинтеза. Хотя тенденции изменений были одинаковы при однофакторном и комбинированном стрессе, степень изменений была различна. Ингибиторные эффекты комбинированного стресса были сильнее и по-разному влияли на каждый из показателей. В отношении активности каталазы проявлялись аддитивные эффекты, а в отношении фотосинтеза - синергические [8].
Данная работа посвящена регистрации индукционных кривых замедленной флуоресценции, биосинтеза каротиноидов и каталазной активности в клетках Dunaliella, выращенных при различных хронических дозах УФ-С и УФ-В излучения в интенсивной культуре и обработанных различными их острыми дозами.
Материалы и методы
Объектом исследования служила зеленая галофильная одноклеточная водоросль Dunaliella salina IPPAS D-294.
Водоросли выращивали при 27оС в фотореакторах (250 мл), из обычного (контрольные суспензии) и кварцевого (опытные суспензии) стекла, на установке для выращивания культур одноклеточных водорослей «УВКВ» [1]. Минеральная среда содержала (г/л): NaCI - 87,5 (1,5 М) ; KNO3 -5,0; KH2PO4-1,25; MgSO4 -50; FeSO4-0,009 раствор микроэлементов, 1 мл/л. Суспензию клеток в фотореакторах круглосуточно освещали белым светом люминесцентных ламп (16 Вт/м2), и непрерывно продували воздушной смесью (воздух + 1,5% СO2).
В качестве источника УФ-С излучения была использована бактерицидная лампа БУВ-30. По 25 мл клеточной суспензии (оптическая плотность D=0,8) переносили в кварцевую емкость, которая охватывает поверхность УФ лампы, и облучали в затемненном боксе острой дозой УФ-С излучения.
Источником УФ-В излучения служила ртутная лампа СВД-120, снабженная светофильтром УФС-2. Хроническое УФ-С, УФ-В облучение клеток проводили круглосуточно, с помощью часового механизма. Клетки выращивали в течение 24 часов, в интенсивно-накопительном режиме культивирования.
Темп роста культуры определяли периодическим подсчетом числа клеток в камере Горяева под микроскопом или нефелометрическим измерением оптической плотности суспензии на КФК-2.
Клеточную суспензию, подготовленную к измерению содержания пигментов, каталазной активности и замедленной флуоресценции, доводили до 106 кл/мл (оптическая плотность D=0,8).
Содержание пигментов в клеточных экстрактах (100% ацетон) измеряли на спектрофотометре СФ-46 и рассчитывали на основании коэффициентов Ветштейна [3].
Регистрацию замедленной флуоресценции (ЗФ) в миллисекундном диапазоне проводили на квантометрической установке с фосфороскопом.
Для измерения каталазной активности клеток, суспензию осаждали центрифугированием (3000 об/мин). Осадок переносили в ступку с 0,5 г СаСО3, добавляли 5 мл дистиллированной воды и растирали до однородной массы. После этого полученную массу количественно переносили в стакан емкостью 50 мл до метки и настаивали при периодическом взбалтывании 3-4 часа. В течение этого времени идет экстракция фермента из растительного материала. После настаивания суспензию фильтровали в сухой стакан. Активность каталазы измеряли газометрическим методом, который основан на определении объема кислорода после прибавления к водному экстракту из растений, содержащему каталазу, перекиси водорода [5].
Результаты и обсуждение
На рисунке 1, представлены результаты изучения зависимости жизнеспособности, количества синтезированных каротиноидов и каталазной активности в клетках Dunaliella от хронических доз УФ-С излучения в интенсивной культуре. Как видно из рисунка, кривая доза-эффект описывается одновершинной кривой, с максимумом в интервале 5-10 сек/час хронических доз УФ-С излучения (рис.1,1). Ранее нами была показана [4] стимуляция клеточного деления при действии хронически малых доз УФ-С излучения на популяцию клеток микроводорослей. Увеличение хронической дозы УФ-С излучения выше 10 сек/час приводит к снижению жизнеспособности популяции клеток Dunaliella, и при хронической дозе 20 сек/час наблюдается подавление роста, которое составляет 80% от контроля. Измерение количества каротиноидов в клетках показали, что биосинтез последних при облучении снижается до 78% по отношению к контрольным популяциям (рис.1,2). Каталазная активность клеток в этих условиях по мере увеличения хронических доз УФ-С излучения повышается (рис.1,3).

Рис. 1. Зависимость жизнеспособности водорослей (1), количества синтезированных каротиноидов (2) и каталазной активности (3) в клетках Dunaliella от хронических доз УФ-С излучения.
Так, при хронически малых дозах 5 сек/час, наблюдается плато с постепенным увеличением каталазной активности в последующих хронических дозах УФ-С облучения. Измерение индукционных кривых замедленной флуоресценции хлорофилла клеток Dunaliella показало, что амплитуда индукционного максимума Ам (рис.2,1) ЗФ с увеличением острой дозы УФ-С излучения уменьшается. Так, при острой дозе (60 сек.) подавление индукционного максимума составляет 80% от контроля. Стационарный уровень Iст индукционной кривой ЗФ хлорофилла с повышением острой дозы УФ-С излучения увеличивается (рис.2,2). При острой дозе (60 сек.) превышение величины Iст составляет 30% от контрольного стационарного уровня. Параметр Ам/Iст, характеризующий энергизацию фотосинтетических мембран, с увеличением острой дозы снижается (рис.2,3) и составляет 63% от контрольной величины. При постановке опытов по влиянию УФ-С лучей на непрерывно растущие культуры учитывались некоторые специфические особенности действия малых доз на клеточную популяцию. При малых мощностях дозы было обнаружено стимуляция деления и некоторое увеличение каталазной активности клеток. Изучение специфических особенностей влияния острых доз УФ-С излучения на каталазную активность клеток, позволило получить информацию о сильном угнетающем его действии. На рисунке 3, представлены данные зависимости каталазной активности в клетках от острой дозы УФ-С излучения. Как видно из рисунка, острые дозы УФ-С излучения подавляют каталазную активность клеток.
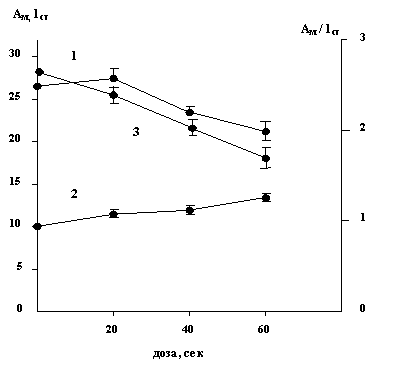
Рис. 2. Зависимость амплитуды индукционного максимума Ам (1), стационарного уровня Iст (2) и параметра Ам/Iст (3) замедленной флуоресценции хлорофилла клеток Dunaliella от острых доз УФ-С излучения
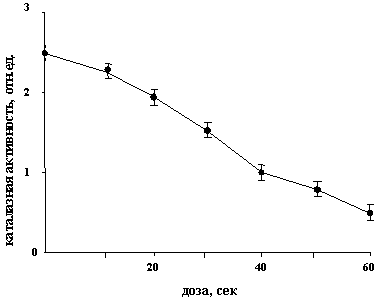
Рис. 3. Зависимость каталазной активности в клетках Dunaliella от острой дозы УФ-С излучения
На рисунке 4, представлены результаты изучения зависимости жизнеспособности, количества синтезированных каротиноидов и каталазной активности в клетках Dunaliella от хронических доз УФ-В излучения в интенсивной культуре.
На кривой зависимости доза-эффект наблюдается некоторая устойчивость популяции клеток микроводорослей (рис.4,1). Увеличение дозы УФ-В излучения мало влияет на выживаемость популяции, так при хронической дозе 1080 сек/час она составляет 95% от контроля. Причем биосинтез каротиноидов с увеличением хронической дозы УФ-В излучения повышается (рис.4,2). Повышение количества каротиноидов в клетках, связано с их защитной функцией фотосинтетического аппарата при УФ-В облучении. Максимальное количество их синтезируется, при хронической дозе 210 сек/час, с увеличением продолжительности облучения биосинтез каротиноидов уменьшается. При хронической дозе 1080 сек/час их количества на 10% выше, чем в контрольных клетках. Каталазная активность в клетках с увеличением хронической дозы УФ-В излучения повышается (рис.4,3). Только при хронической дозе 1080 сек/час, каталазная активность снижается до уровня 105% от контрольной величины. Подавление первичных реакций фотосинтеза при острой дозе УФ-В излучения сказывается на индукционных кривых замедленной флуоресценции хлорофилла клеток.

Рис. 4. Зависимость жизнеспособности водорослей (1), количества синтезированных каротиноидов (2) и каталазной активности (3) в клетках Dunaliella от хронических доз УФ-В излучения
На рисунке 5 представлена, зависимость параметров индукционной кривой ЗФ от острой дозы УФ-В излучения. Как видно, амплитуда индукционного максимума Ам спонтанно повышается, и максимальная ее величина наблюдается при 15 минутном облучении, а затем плавно снижается и устанавливается чуть выше контрольного уровня (рис.5,1). Стационарный уровень Iст индукционной кривой ЗФ с увеличением острой дозы после некоторого плато, возрастает и устанавливается на значениях превышающих контрольные в 2 раза (рис.5,2). Причем, параметр, характеризующий энергизацию фотосинтетических мембран Ам/Iст снижается (рис.5,3). Это снижение говорит о подавлении первичных реакций фотосинтеза и фотосинтетической активности клеток.
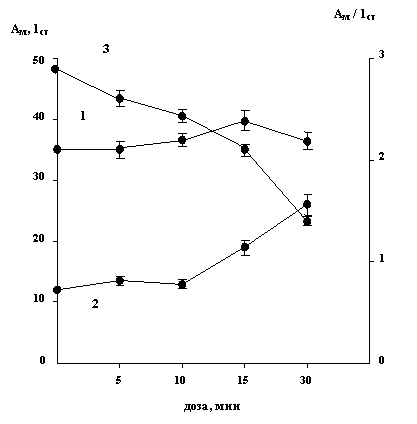
Рис. 5. Зависимость амплитуды индукционного максимума Ам (1), стационарного уровня Iст (2) и параметра Ам/Iст (3) замедленной флуоресценции хлорофилла клеток Dunaliella от острых доз УФ-В излучения

Рис. 6. Зависимость каталазной активности в клетках Dunaliella от острой дозы УФ-В излучения
Каталазная активность в клетках облученных острой дозой УФ-В света, описывается одновершинной кривой (рис.6). Так, при острой дозе УФ-В излучения 10 минут наблюдается максимальная каталазная активность, затем по мере увеличения продолжительности облучения ее активность несколько подавляется. Несмотря на снижение каталазной активности в клетках облученных при высоких дозах УФ-В света, ее активность выше, чем в контрольных суспензиях.
Таким образом, на основании полученных данных, можно сказать следующее, ЗФ позволяет получить уникальную информацию о величине электрохимического протонного градиента на мембране тилакоида в целой клетке. УФ-С и УФ-В излучение, препятствует образованию электрохимического градиента протонов на мембране, что в свою очередь вызывает соответственно подавление электронного транспорта в реакционных центрах фотосистемы II и параметра Ам/Icт замедленной флуоресценции. Влияние острых доз УФ излучения на клетки Dunaliella показали, что каталазная активность при определенных дозах УФ-В излучения возрастает, повышая уровень защитной антиоксидантной активности водоросли, а затем с увеличением продолжительности облучения снижается. Жесткие УФ-С лучи подавляют каталазную активность уже при малых дозах и не дают антиоксидантной системе реализации компенсаторных механизмов защиты. В ответ на действие хронических доз УФ излучения активируются системы неспецифической защиты организма, компонентами которой в основном являются низкомолекулярные антиоксидантные системы (каротиноиды) водоросли и оксидазные ферменты (каталаза и др.). Данные полученные в работе не оставляют сомнения в том, что реактивность и устойчивость любой биологической системы в ответ на УФ излучение зависит от интенсивности и продолжительности их действия.
СПИСОК ЛИТЕРАТУРЫ:
- Али-заде Г.И., Абдуллаев Х.Д., Наджафов М.Г. // Известия БГУ, серия естественных наук, 1999, № 2, стр.80-85.
- Байляк М.М., Семчишин Г.М., Лущак В.И. // Укр. биохим. журнал, 2006, т.78, № 2, стр.79-85
- Гавриленко В.Ф., Ладыгина М.Е., Хандобина Л.М. // Большой практикум по физиологии растений, М. «Высшая школа», 1975, 392 с.
- Магеррамов А.М., Гусейнова А.Р., Али-заде Г.И. и др. //Доклады НАН Азербайджана, 2003, N3-4, стр.172-177
- Плешков Б.П. // Практикум по биохимии растений, М., 1976, 255 с.
- Liang Сhan-juan, Shi Da-gang. // Res. Arid.Areas, 2006, V.24, N3, p.108-110
- Liang Сhan-juan, Xu Qing, Tao Wen-yi et all. // J. Agro. Environ. Sci., 2004, V.23, N 4, p.642-645
- Wang Li-hong, Huang Xiao-hua // Environ. Sci., 2005, V. 26, N6, p.123-125
- Mohanty M., Jena H., Patra H. // Indian J. Agr. Biochem., 2005, V.18, N1, p.25-29



